в) температуры;
г) давления.
8 В уравнении Ильковича:
![]()
а) Ig; 1) скорость вытекания ртути из капилляра
б) n; 2) концентрация деполяризатора
в) д; 3) число электронов
г) m; 4) время жизни капли
д) t; 5) предельный диффузный ток
е) C. 6) коэффициент диффузии
9 В полярографии качественной характеристикой присутствующего иона металла в растворе является … .
а) высота полягрофической волны;
б) потенциал полуволны;
в) величина предельного тока;
г) число электронов участвующих в восстановлении иона металла.
10 Высота полягрофической волны, характеризующая предельный ток, прямо пропорциональна … .
а) числу ионов различных металлов в растворе;
б) концентрации ионов металла в растворе;
в) числу электронов, участвующих в восстановлении ионов металла;
г) скорости диффузии ионов металла к поверхности ртутного катода.
11 Для количественных полягрофических определений используют … .
а) метод калибровочной кривой;
б) метод стандарта;
в) метод разбавления;
г) метод добавок.
12 Метод анализа, основанный на измерении количества электричества, затраченного на электродную реакцию, называется … .
а) кондуктометрией;
б) амперометрией;
в) потенциометрией;
г) кулонометрией.
13 В формуле объединенных законов Фарадея:
![]() :
:
а) m; 1) число электронов, участвующих в реакции;
б) M; 2) масса определяемого вещества;
в) Q; 3) постоянная Фарадея;
г) n; 4) количество электричества;
д) F. 5) молярная масса.
14 Масса цинка, выделявшегося на катоде в ходе кулонометрического анализа при количестве пропущенного электричества 600 Кл, равна … г.
а) 0,1016;
б) 0,4064;
в) 0,2032;
г) 0,0508.
15 Равновесная концентрация равна … моль/л, если потенциал серебряного электрода в растворе соли серебра составляет 0,434 В относительно СВЭ (![]() ).
).
а) ![]()
б) ![]()
в) ![]()
г) ![]()
16 Для выделения 10 г меди из раствора CuSO4 при силе тока 10 А необходимо затратить … Кл (выход по току 100 %).
а) ![]()
б) ![]()
в) ![]()
г) ![]()
17 Концентрация раствора K2Cr2O7, на титрование 25 мл которого электрогенерированными ионами Fe (II) затрачено 1800 с при силе тока 200 mА, равна … моль/л.
а) 0,0249;
б) 0,0498;
в) 0,1000;
г) 0,0025.
2.7.3 Хроматография
1 Отношение концентраций вещества в подвижной и неподвижной фазах в хроматографическом анализе называется … .
а) коэффициентом удержания;
б) коэффициентом ёмкости;
в) коэффициентом распределения;
г) фактором разделения.
2 Сумма времени пребывания веществ в подвижной фазе и времени пребывания в неподвижной фазе называется … .
а) временем задержки;
б) временем удерживания;
в) временем разделения;
г) периодом адсорбции.
3 В уравнении:
![]() , где
, где
а) VR; 1) время удерживания;
б) F; 2) удерживаемый объём;
в) tR. 3) объёмная скорость потока подвижной фазы.
4 В уравнении:
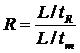 , где
, где
а) R; 1) время пребывания вещества в подвижной фазе;
б) L; 2) длина колонки;
в) tR; 3) коэффициент удерживания;
г) tm. 4) время удерживания.
5 В формуле:
![]() , где
, где
а) H; 1) высота, эквивалентная теоретической тарелке;
б) L; 2) число теоретических тарелок;
в) N. 3) длина колонки.
6 Соответствие названия и сущности метода количественного анализа в хроматографии
а) метод абсолютной калибровки; 1) введение в анализируемый образец известного количества стандартного соединения и расчёт по полученной хроматограмме;
б) метод внутренней 2) построение градуировочного графика по
нормализации; серии стандартных смесей;
в) метод внутреннего стандарта. 3) суммирование площадей пиков всех компонентов смеси на хроматограмме, принимая эту сумму за 100 % и проводя дальнейшие расчёты по коэффициенту чувствительности детектора к этим компонентам.
7 При пропускании раствора, содержащего ионы Ag+, Pb2+, Hg+2, через хроматографическую колонку с ионообменником, содержащим ионы I–, получены три зоны, соответствующие ионам:
а) оранжево-красная; 1) AgI
б) светло-желтая; 2) PbI2
в) тёмно-желтая. 3) HgI2
8 Способы осуществления адсорбционной хроматографии:
а) фронтальная;
б) вытеснительная;
в) удерживающая;
г) элюентная.
9 Коэффициент распределения в распределительной хроматографии зависит от … .
а) размера хроматографической колонки;
б) природы анализируемого вещества;
в) температуры;
г) природы растворителя.
10 Реакция ионного обмена органических катионов:
а) ![]()
б) ![]()
в) ![]()
г) ![]()
СЛОВАРЬ ТЕРМИНОВ И ПОНЯТИЙ
Основные теоретические положения аналитической химии
Активность иона – доля ионов вещества, которая проявляет себя в действии.
Аналитическая химия – наука об определении химического состава веществ и, отчасти, их химического строения.
Аналитический сигнал – физическая величина, функционально связанная с содержанием компонента.
Буферная ёмкость – число моль-эквивалентов сильной кислоты или щёлочи, которые нужно добавить к 1 литру буферного раствора, чтобы изменить величину pH на единицу.
Буферный раствор – раствор, содержащий протолитическую равновесную систему, способную поддерживать практически постоянное значение pH при разбавлении небольших количеств кислоты или щёлочи.
Гидролиз солей – протолитический процесс взаимодействия ионов солей с молекулами воды, в результате которого образуются малодиссоциирующие молекулы или ионы.
Задачи аналитической химии как области знания: решение общих вопросов анализа (например, развитие его метрологии); разработка аналитических методов; решение конкретных задач анализа (например, создание аналитической химии пестицидов).
Закон действующих масс: скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.
Ионная сила раствора – величина, которая зависит от концентраций и зарядов всех ионов, находящихся в растворе, и является мерой электростатического взаимодействия между ними.
Истинные растворы – гомогенные системы с размером частиц на уровне 10–10–10–9 м.
Качественный анализ решает вопрос о том, какие компоненты включает анализируемый объект.
Кислотными буферными системами называются растворы, содержащие слабую кислоту донор протона) и соль этой кислоты (акцептор протона).
Количественный анализ даёт сведения о количественном содержании всех или отдельных компонентов.
Коллоидные растворы – гетерогенные системы с размером частиц на уровне 10–9–10–6 м.
Константа диссоциации электролита – отношение произведения концентраций ионов в растворе слабого электролита к концентрации его недиссоциированной части.
Концентрация раствора – величина, измеряемая количеством растворённого вещества в определённом объёме или масс раствора (иногда растворителя).
Концентрирование – операция (процесс), в результате которой повышается отношение концентрации или количества микрокомпонентов к концентрации или количеству макрокомпонента.
Коэффициент активности иона – показывает, во сколько раз активность иона отличается от его истинной концентрации в растворе сильного электролита.
Массовая доля – отношение массы растворённого вещества к массе раствора, умноженное на 100 %.
Метод анализа – достаточно универсальный и теоретически обоснованный способ определения состава безотносительно к определяемому компоненту и (обычно) к анализируемому объекту.
Метод градуировочного графика: строится график в координатах «аналитический сигнал – содержание определяемого компонента с использованием образцов сравнения с различным и точно известным содержанием исследуемого компонента», по которому находят искомое содержание компонента по градуировочному графику.
Метод контрольного опыта («холостого опыта»): через все стадии химического анализа проводится проба, не содержащая определяемого компонента.
Метод стандартов: измеряют величины аналитических сигналов в образце сравнения с известным содержанием компонента и в анализируемой пробе.
Методика анализа – подробное описание анализа данного объекта с использованием выбранного метода.
Моляльная концентрация – отношение количества растворённого вещества к массе растворителя.
Молярная концентрация – отношение количества растворённого вещества к объёму раствора.
Нормальность – число эквивалентов в 1 л раствора.
Основными буферными системами называются растворы, содержащие слабое основание (акцептор протона) и соль этого основания (донор протона).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
