РОСЖЕЛДОР
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«Ростовский государственный университет путей сообщения»
(ФГБОУ ВПО РГУПС)

С. А. Воляник, М. А. Савенкова, Ю. Ф. Мигаль
РЕПЕТИЦИОННЫЕ ТЕСТЫ
ПО АНАЛИТИЧЕСКОЙ ХИМИИ
И ФИЗИКО-ХИМИЧЕСКИМ
МЕТОДАМ АНАЛИЗА
Учебное пособие
Ростов-на-Дону
2011
УДК 54(07) + 06
Воляник, С. А.
Репетиционные тесты по аналитической химии и физико-химическим методам анализа : учебное пособие / С. А. Воляник, М. А. Савенкова, Ю. Ф. Мигаль ; Рост. гос. ун-т путей сообщения. – Ростов н/Д, 2011. – 92 с. Библиогр. : 10 назв.
Учебное пособие составлено в соответствии с программой по аналитической химии и физико-химическим методам анализа для специальности «Инженерная защита окружающей среды» и предназначено для подготовки студентов этой специальности к тестовой аттестации.
В учебном пособии в краткой и доступной форме рассмотрены демонстрационные варианты тестов по основным разделам теории качественного и количественного анализа, алгоритмы решения тестовых заданий, а также репетиционные тесты, которые позволят студентам самостоятельно подготовиться и успешно сдать тест-экзамен.
Рецензенты: зав. кафедрой химии и экологии, д-р техн. наук, профессор
А. Н. Королев (ТИ ЮФУ в г. Таганроге);
канд. техн. наук, доц. Г. Н. Соколова (РГУПС)
© Ростовский государственный университет
![]() путей сообщения, 2011
путей сообщения, 2011
ВВЕДЕНИЕ
Тестовые задания, предложенные для самостоятельной работы студентов, разделены на основные темы, составляющие общий курс «Аналитическая химия и физико-химические методы анализа», который включает в себя:
– аналитические свойства веществ, типы и характеристики аналитических реакций, виды анализа, методы разделения и концентрирования веществ;
– качественный анализ: систематический и дробный, групповые реагенты, качественный анализ катионов и анионов;
– количественный анализ: весовой и объёмный;
– физико-химические и физические методы анализа
В каждом из приведённых разделов содержатся демонстрационные тестовые задания, решение которых сопровождается пояснением основных понятий и законов, необходимых для правильного поиска верного ответа. Разнообразен уровень тестовых заданий: от простого «узнавания» до трудоёмких многоуровневых тестов, в которых требуются не только знания теоретических основ курса, но и умения быстрых расчётов, установления правильных, соответственных логических выводов и написания верных ответов.
Сложный для усвоения теоретический материал представлен в настоящем пособии в виде таблиц и схем. Словарь терминов и понятий, а также перечень рекомендуемой литературы облегчат студентам самоподготовку к тестированию и углублённому изучению данного курса.
Раздел I. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ АНАЛИТИЧЕСКОЙ ХИМИИ
Аналитическая химия – это наука о методах и средствах определения химического состава веществ и материалов.
Главное содержание теории химических методов анализа составляет химическая реакция – средство получения информации о химическом составе вещества, используемая для целей качественного и количественного анализа. Аналитическими называются химические реакции, которые сопровождаются каким-либо внешним эффектом (изменением окраски, выпадением осадка, выделением газа и т. д.) и служат для разделения, обнаружения и количественного определения элементов, ионов, молекул. Важное значение имеют тип аналитической реакции, условия и способы её проведения.
Таблица 1
Аналитические реакции и требования к ним
Тип аналитических реакций | Требования к аналитическим реакциям | Условия проведения аналитических реакций |
1 Кислотно-основное взаимодействие 2 Редокс-реакция 3 Реакция комплексообразования 4 Реакция осаждения | 1 Реакции должны протекать быстро, количественно стехиометрично 2 Реакции должны быть необратимыми 3 Реакции должны сопровождаться аналитическим эффектом (изменение окраски, выпадение осадка, выделение газа и т. д.) 4 Реакции должны иметь высокую чувствительность и специфичность | 1 Соблюдение pH среды. 2 Наличие достаточной для обнаружения концентрации ионов. 3 Температурный режим |
Большинство аналитических реакций – избирательные (селективные), т. к. в ходе этих реакций имеют место схожие аналитические эффекты для нескольких ионов.
Специфическими называются реакции, позволяющие обнаружить данный ион в присутствии других ионов.
Чувствительность аналитических реакций описывается следующими понятиями.
Таблица 2
Основные характеристики аналитических реакций
Название | Характеристика |
Минимальная концентрация | Показывает, при какой предельно минимальной концентрации определяемого иона в растворе данная реакция ещё возможна для обнаружения в определённом объёме исследуемого раствора |
Открываемый минимум | Наименьшая масса определяемого иона, которая может быть обнаружена с помощью данной реакции в наименьшем объёме исследуемого раствора |
Предельное разбавление | Наибольшее разбавление раствора, содержащего 1 г определяемого иона, при котором ещё заметна данная реакция (выпадение осадка, выделение газа, изменение окраски) |
Демо-тест 1
Чувствительность аналитической реакции тем больше, чем…
а) меньше открываемый минимум;
б) больше открываемый минимум;
в) меньше минимальная концентрация;
г) больше предельное разбавление;
д) меньше предельное разбавление.
Чувствительность – одно из важнейших требований к аналитическим реакциям – можно повысить, если увеличить концентрацию определяемого иона, например: выпариванием сильноразбавленного раствора, изменением температуры, pH среды раствора. Но, конечно, чем меньше масса определяемого иона, а следовательно, ниже определяемая минимальная концентрация иона в растворе, тем чувствительнее реакция. Т. к. с разбавлением раствора концентрация иона уменьшается, то чувствительность такой реакции также будет повышаться. Вывод: верными являются ответы: а), в), г).
Кислотно-основные, или протолитические, реакции – это реакции между кислотами и основаниями. Согласно теории Бренстеда – Лоури (1923 г.) кислоты способны отдавать протон, являясь донорами протонов. Это могут быть как молекулы, так и ионы:
Hclo4 ⇆H+ + ClO4–
NH4+ ⇆ H+ + NH3
H2PO4 ⇆H+ + HPO![]()
Основания – вещества, способные присоединять протоны (акцепторы протонов):
СlO4– + H+ ⇆ HClO4
OH– + H+ ⇆ H2O
NH3 + H+ ⇆ NH4–
HPO42– + H+ ⇆ H2PO4–
По положению теории Бренстеда – Лоури при взаимодействии кислоты и основания (реакция протолиза) образуются сопряжённые кислотно-основные пары:
Кислота 1 + Основание 1 = Кислота 2 + Основание 2
Например: HClO4 + H2O ⇆ H3O+ + ClO4–
Демо-тест 2
Согласно теории Бренстеда – Лоури CH3COOH (разб.), H2SO4, HCl являются растворителями:
а) протогенными;
б) протофильными;
в) апротонными;
д) амфипротными.
Молекулярные жидкости классифицируют по способности принимать или отдавать протоны следующим образом (табл. 3).
Таблица 3
Классификация растворителей
№ п/п | Тип растворителя | Характер | Примеры |
1 | Протогенный | Кислотный | HF, HSO4 |
2 | Амфипротный | Как кислотный, так и основной | H2O |
3 | Протофильный | Основной | Тетраметилмочевина, амины |
4 | Апротонный | Нейтральный | Ацетонитрил, бензол |
Приведённые кислоты являются протогенными растворителями, т. к. способны отдавать протон. Вывод: верный ответ а).
Внешние факторы, влияющие на силу протолитов, определяются характером среды, условиями проведения реакции (ионная сила растворителя, температура и т. д.).
Ионная сила рассчитывается:
I = 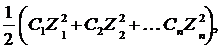
где I – ионная сила;
С1, С2, … Сn – молярные концентрации присутствующих в растворителе ионов;
Z1, Z2, … Zn – заряды ионов.
Буферная система – это раствор, состоящий из слабой кислоты (или основания) и её (его) соли, pH которого не изменяется при разбавлении водой или добавлении небольших количеств сильных кислот или оснований.
Например: CH3COOH + CH3COONa – ацетатный буфер (pH ≈ 4,74);
NaH2PO4 + Na2HPO4 – фосфатный буфер (pH ≈ 6,6);
NaHCO3 + Na2CO3 – карбонатный буфер (pH ≈ 9,93).
Буферная ёмкость (П) определяется числом молей эквивалентов сильной кислоты или основания, добавление которых изменяет pH буферной системы на единицу:
П = 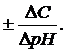
Согласно теории кислот и оснований Льюиса кислоты – вещества, способные присоединять пару неподеленных электронов от основания, а основания – вещества, способные отдавать неподеленную электронную пару.
Например: Cl3Br + : NH3 = Cl3Br : NH3

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
