· Дипикриламин [C6H2(NO2)3]NH (реактив Полуэктова) образует с ионом K+ мелкокристаллический оранжево-красный осадок.
· 8-Оксихинолин C9H6NOH из аммиачных растворов солей магния выделяет зеленовато-жёлтый кристаллический осадок Mg(C9H6NO)2. Является также реактивом на большое число других ионов.
· Ализарин C14H6)2(OH)2 даёт с гидроксидом алюминия малорастворимое соединение ярко-красного цвета, называемое «алюминиевым лаком».
· Бензидин C12H8(NH2)2, окисляясь ионами хрома (VI) или марганца (VII), даёт соединения синего цвета.
· Дифениламин (C6H5)2NH окисляется ионами NO![]() с образованием продукта интенсивно синего цвета. Аналогично действуют на него некоторые другие окислители.
с образованием продукта интенсивно синего цвета. Аналогично действуют на него некоторые другие окислители.
· Стильбазо C26H26O10N6S2 является реактивом на катион алюминия, с которым при pH 5,5 даёт розовую окраску (предложен В. И. Кузнецовым).
· Арсеназо C16H11O11N2S2AsNa2 даёт с катионом алюминия и некоторыми другими ионами фиолетовое окрашивание различных оттенков (предложен В. И. Кузнецовым).
· Диэтилдитиофосфорная кислота (C2H5O)2 – реактив, предложенный А. И. Бусевым для выполнения цветных реакций на катионы меди, висмута и ряда других металлов.
· Диэтилдитиокарбаминат натрия (C2H5)2NCS2Na используется как реагент на катионы меди (II) и никеля (II).
· Магнезон ИРЕА C16H10O5N2SCINa в присутствии катионов магния изменяет сине-фиолетовую окраску на ярко-красную (при pH 9,8–11,2).
· Родамин Б C24H21N2O3Cl в присутствии хлоридного комплекса сурьмы (V) изменяет розовую окраску на синюю или фиолетовую.
· Нитрон (C6H5)3CN4CH из уксуснокислых растворов осаждает нитрат-ион в виде игольчатых кристаллов.
Существуют две группы методов количественного анализа: химические и физико-химические. К химическим методам количественного анализа относятся гравиметрия (весовой метод) и титриметрия (объёмный метод).
Гравиметрическим анализом называют метод, основанный на точном измерении массы определяемого компонента пробы, выделенного в виде соединения определённого состава.
Последовательность проведения гравиметрического анализа:
отбор средней пробы → взвешивание навески → растворение навески →
→ осаждение определяемого вещества осадителем → отделение осадка
фильтрованием → промывание осадка → прокаливание осадка → взвешивание гравиметрической формы → вычисление результата.
Расчёт содержания определяемого компонента в пробе осуществляется по формуле:
![]()
где m – масса прокалённого осадка, г;
F – аналитический множитель;
a – масса навески исследуемой пробы, г.
Аналитический множитель – соотношение молекулярной (атомной) массы определяемого вещества (элемента) к молекулярной массе прокалённого осадка (весовой формы).
Демо-тест 8
Аналитический множитель F при определении Ba в виде BaSO4 равен … (A(Ba) = 137, A (S) = 32, A (О) = 16).
а) 0,3875;
б) 0,5887;
в) 0,6409;
г) 0,8352.
Аналитический фактор F при гравиметрическом определении бария в виде сульфата бария вычисляется по формуле:
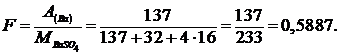
Вывод: верный ответ б).
Демо-тест 9
Содержание хлора в образце технического хлорида натрия, при гравиметрическом анализе 2,0000 г которого с помощью AgNO3 получили 4,6880 г весовой формы AgCl, составляет … % (A(Cl) = 35,5, A(Ag) = 108).
а) 98,73;
б) 64,54;
в) 28,95;
г) 57,98.
Содержание хлора рассчитывается по формуле:
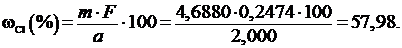
Масса навески NaCl a = 2,0000 г.
Масса весовой формы AgCl m = 4,6880.
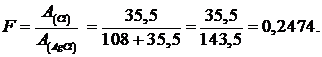
![]()
Вывод: верный ответ г).
Демо-тест 10
Объём 0,25М раствора (NH4)2C2O4, необходимого для полного осаждения Ca2+ из раствора, содержащего 0,7700 г Ca(NO3)2, равен … мл. (Для полного осаждения взять 1,5-кратный избыток осадителя, M![]() = 124, M
= 124, M![]() = 164.)
= 164.)
а) 21,3;
б) 42,6;
в) 12,2;
г) 26,4.
Расчёт объёма осадителя оксалата аммония (0,25M (NH4)2C2O4) производится исходя из уравнения реакции:
Ca(NO3)2 + (NH4)2C2O4 → CaC2O4↓ + 2NH4NO3
164 г Ca(NO3)2 – 124 NH4NO3
0,7700 г Ca(NO3)2 – х NH4NO3
х = ![]()
Расчёт объёма 0,25М (NH4)2С2O4.
В 1000 мл 0,25М раствора (NH4)2C2O4 содержится 0,25 · 164 г вещества.
В х мл 0,25М раствора (NH4)2C2O4 содержится 0,5822 г вещества.
х = ![]()
Взяв 1,5 избыток, получаем:
![]()
Вывод: верный ответ а).
Титриметрический метод анализа основан на измерении объёма раствора титранта, затраченного на реакцию с определяемым веществом. Титрантом (стандартным раствором) называется раствор реагента с точно известной концентрацией.
Титрированием называют процесс постепенного добавления небольших порций титранта к исследуемому раствору. Момент реакции, при котором количество добавленного титранта эквивалентно количеству определяемого вещества в исследуемом растворе, называется точкой эквивалентности.
Точку эквивалентности фиксируют визуально (по изменению окраски) индикатора, добавленного в анализируемый раствор, или инструментально (по резкому изменению физико-химического параметра: потенциала индикаторного электрода, электропроводности раствора, оптической плотности и т. д.).
В основе расчётов в титриметрии лежит закон эквивалентов, согласно которому вещества реагируют между собой прямо пропорционально их химическим эквивалентам.
Пусть а моль вещества А взаимодействует c b моль вещества B:
аА + вВ → продукты.
Факторы эквивалентности fэкв(А) и fэкв(B) рассчитываются следующим образом:
![]()
![]()
где ![]()
![]() – нормальные концентрации растворов А и В;
– нормальные концентрации растворов А и В;
V(A), V(B) – объёмы растворов А и В.
Титр – число граммов растворённого вещества, содержащегося в 1 мл раствора, – рассчитывается по формуле:
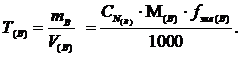
Титр связан с нормальной концентрацией титранта В:
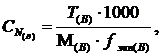
где М(В) – молекулярная масса эквивалента вещества В.
m(A) = ![]() · V(B) · M(A) · fэкв(А).
· V(B) · M(A) · fэкв(А).
Для перерасчёта из моль в моль:
m(A) = 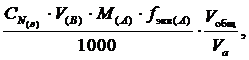
где ![]() – называется фактором разбавления.
– называется фактором разбавления.
Этот фактор используют, когда для титрования берут не весь объём анализируемого раствора А (Vобщ), а только его часть (Vа), называемую аликвотой.
Если известен титр В, то получается:
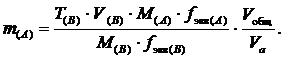
При серийных анализах полезно знать титр по определяемому веществу ТВ/А, который показывает, с какой массой (г) анализируемого вещества А реагирует 1 см3 титранта В:
ТВ/А = 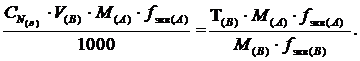
Демо-тест 11
Титр Т![]() равен … , если NaOH титруют 0,5н раствором серной кислоты (M(NaOH) = 40).
равен … , если NaOH титруют 0,5н раствором серной кислоты (M(NaOH) = 40).
а) 0,02000;
б) 0,01000;
в) 0,01250;
г) 0,04000.
Т![]() =
= 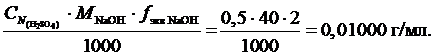
fэкв(NaOH) = 2 (т. к. NaOH и H2SO4 реагируют 2 : 1).
Вывод: верный ответ г).
Демо-тест 12
В 500 мл раствора H2SO4 на титрование 25 мл которого затрачено 26,15 мл 0,1н раствора NaOH, содержится … г серной кислоты (M![]() = 98):
= 98):
а) 2,5627;
б) 0,1281;
в)5,1254;
г) 2,9614.
Масса H2SO4 рассчитывается по формуле:
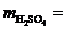
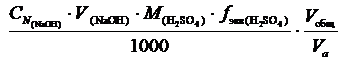 =
=
= ![]()
Вывод: верный ответ а).
В титриметрическом методе можно использовать любую аналитическую реакцию (кислотно-основное взаимодействие, комплексообразование, редокс-реакцию, реакцию осаждения).
Таблица 15
Примеры титрантов и индикаторов в различных методах титрования
Метод титрования | Примеры титрантов | Инициаторные системы |
1 Кислотно-основное титрование | Сильная кислота (H2SO4, HCl, HNO3) Сильное основание (KOH, NaOH) | Метилоранж Фенолфталеин Лакмус |
2 Комплексометрическое титрование | ЭДТА | Эриохром чёрный Т Мурексид |
3 Редоксометрическое титрование | KMnO4 I2 Na2S2O3 · 5H2O | – Крахмал |
Окончание табл. 15

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
