г) ![]()
10 Навеска ![]() , взятая для получения осадка BaSO4 массой 0,2000 г, равна … г (А(Ba) = 137, A(Cr) = 35,5, А(S) = 32, A(O) = 26).
, взятая для получения осадка BaSO4 массой 0,2000 г, равна … г (А(Ba) = 137, A(Cr) = 35,5, А(S) = 32, A(O) = 26).
11 Навеска CaCl2, взятая для получения осадка CaCO3 массой 0,1500 г, равна … г (А(Сa) = 40, A(Cr) = 35,5, А(С) = 12, A(O) = 16).
12 Объем 2М раствора аммиака 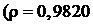 г/мл), взятого в 1,5-кратном избытке, необходимый для осаждения 0,7000 г Fe(NO3)3, равен … мл.
г/мл), взятого в 1,5-кратном избытке, необходимый для осаждения 0,7000 г Fe(NO3)3, равен … мл.
а) 4,3;
б) 6,5;
в) 8,2;
г) 3,5.
13 Навеска ![]() , взятая для определения в ней хлора осаждением AgNO3 в виде осадка AgCl массой 0,5212 г, равна … г (A(Mg) = 23, A(Ag) = 108, A(Cl) = 35,5, A(O) = 16, A(H) = 1)
, взятая для определения в ней хлора осаждением AgNO3 в виде осадка AgCl массой 0,5212 г, равна … г (A(Mg) = 23, A(Ag) = 108, A(Cl) = 35,5, A(O) = 16, A(H) = 1)
а) 0,3214;
б) 0,2107;
в) 0,4215;
г) 0,3699.
14 Массовую долю определяемого компонента рассчитывают по формуле 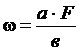 , где
, где
а) ![]() ; 1) массовая доля;
; 1) массовая доля;
б) а; 2) масса осажденной формы;
в) F; 3) масса навески;
г) в. 4) гравиметрический фактор;
5) масса гравиметрической формы.
15 Объём 1М раствора H2SO4, необходимый для осаждения Ba+2, если навеска ![]() составляет 0,2500 г, равен … мл.
составляет 0,2500 г, равен … мл.
а) 2,0;
б) 1,5;
в) 3;
г) 1.
2.6.2 Титриметрия
1 Титриметрия – метод количественного анализа, основанный на … .
а) измерении количества титранта, израсходованного на реакцию с определяемым веществом;
б) измерении объема растворителя, израсходованного на растворение определяемого вещества;
в) измерении объёма растворителя, необходимого для полного растворения навески определяемого вещества;
г) измерении рН раствора, полученного при растворении навески определяемого вещества в растворителе.
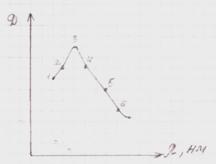
2 На графике представлена кривая титрования
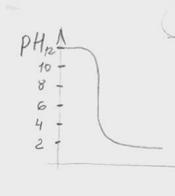
а) сильной кислоты сильным основанием;
б) слабой кислоты сильным основанием;
в) сильного основания сильной кислотой;
г) слабого основания сильной кислотой.
3 Титрантом в редоксометрическом титровании является:
а) ЭДТА;
б) AgNO3;
в) CH3COOH;
г) KMnO4.
4 Раствор ЭДТА – титрант:
а) в ацидиметрии;
б) в комплексонометрии;
в) в алкалиметрии;
г) в аргенометрии.
5 Кривая титрования
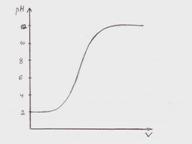
а) сильного основания сильной кислотой;
б) слабого основания сильной кислотой;
в) сильной кислоты сильным основанием;
г) слабой кислоты сильным основанием.
6 Кислотно-основные индикаторы – это … .
а) дифениламин;
б) эриохром черный Т;
в) фенолфталеин;
г) лакмус.
7 При титровании 0,001н раствора ZnSO4 раствором ЭДТА той же концентрации (рН = 9,5) используют индикатор … .
а) эриохром черный Т;
б) дифенилбензидин;
в) метилоранж;
г) фенолфталеин.
8 Фактор эквивалентности тетрабората натрия в реакции Na2B4O7 + 2HCl + + 5H2O = 4B(OH)3 + 2NaCl равен … .
а) 1;
б) 1/2;
в) 1/5;
г) 2/5.
9 Факторы эквивалентности ионов CN– и MnO![]() в реакции CN– + 2MnO
в реакции CN– + 2MnO![]() + + 2OH– + 2OH– = 2MnO
+ + 2OH– + 2OH– = 2MnO![]() + CNO– + H2O равны, соответственно:
+ CNO– + H2O равны, соответственно:
а) 1/2 и 1;
б) 1 и 1/2;
в) 1/2 и 1/2;
г) 1 и 1.
10 Содержание NaCl (мг/мл) в растворе, на титрование 30,00 мл которого потребовалось 15,60 мл 0,1000 М раствора AgNO3, равно … (М(NaCl) = 58,44).
а) 4,12;
б) 2,52;
в) 3,04;
г) 3,75.
11 При титровании 0,01 М раствора HCl 0,01 М NaOH использовали фенолфталеин (рТ = 9,0). Погрешность титрования равна … .
а) 0,2;
б) –2;
в) 0,1;
г) –1.
12 Для титрования 0,3636 г глицина H2NCH2COOH в ледяной уксусной кислоте потребуется … мл 0,1063М раствора HClO4 (M(H2NCH2COOH) = 75).
а) 45,61;
б) 44,28;
в) 46,12;
г) 42,67.
13 Нормальность раствора КОН, на титрование 20 мл которого пошло 18,7 мл раствора HCl (Т HCl = 0,001432г/мл), равна … .
а) 0,03668;
б) 0,03562;
в) 0,01227;
г) 0,04415.
14 В 250 мл раствора хлорида натрия, на титрование 10 мл которого ушло 12,5 мл 0,05 н раствора AgNO3, содержится … г NaCl.
а) 0,8522;
б) 0,5412;
в) 0,8725;
г) 0,6415.
15 Титр Т (HCl/Na2CO3) равен …, если Т (HCl) = 0,03650 г/мл (M(HCl) = 36,5, M(Na2CO3) = 106).
2.7 Физико-химические методы анализа
2.7.1 Оптические методы анализа
1 Методы, основанные на установлении взаимосвязи между составом анализируемого вещества и его оптическими свойствами, называются … методами.
а) оптическими;
б) электрохимическими;
в) хроматографическими;
г) тепловыми.
2 Соответствие оптического метода и изучаемого состава:
а) колориметрический; 1) способность атомов каждого элемента в определенных условиях испускать волны определенной длины
б) нефелометрический; 2) способность атомов поглощать излучение определенной длины волны
в) рефрактометрический; 3) способность дисперсий твердых веществ рассеивать часть светового потока
г) эмиссионный. 4) способность молекул различных веществ по-разному преломлять свет
3 Молекулярная рефракция рассчитывается:
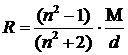 , где
, где
а) n; 1) диаметр частиц
б) M; 2) плотность
в) d. 3) показатель преломления
4) молекулярная масса вещества
4 Согласно закону Бугера – Ламберта – Бера
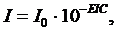 где
где
а) I; 1) молярный коэффициент светопоглощения
б) I0; 2) молярная концентрация раствора
в) E; 3) интенсивность света, прошедшего через раствор
г) l; 4) толщина слоя раствора
д) C. 5) интенсивность падающего света
5 Десятичный логарифм отношения интенсивности падающего света к интенсивности света, прошедшего через раствор, называется … .
а) молярным коэффициентом светопоглощения;
б) диэлектрической проницаемостью;
в) оптической плотностью;
г) коэффициентом светорассеяния.
6 Определение концентрации суспензии осуществляют методом … .
а) колориметрии;
б) рефрактометрии;
в) турбидиметрии;
г) нефелометрии.
7 При значении оптической плотности раствора NiSO4 равном 0,6, его концентрация равна … моль/л.
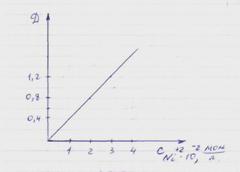
а) ![]() ;
;
б) ![]()
в) ![]()
г) ![]()
8 В эмиссионном спектральном анализе можно определить металл в сплаве … .
а) качественно; 1) по наличию в спектре полосы
б) количественно. 2) по интенсивности полосы
9 Номер рабочего светофильтра в фотоколориметрическом анализе … .
10 Зависимость оптической плотности анализируемого раствора от концентрации … .
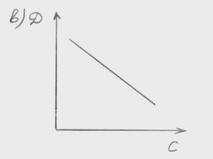
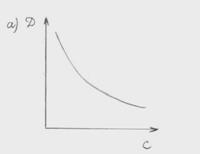
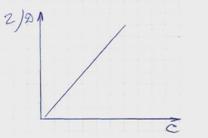
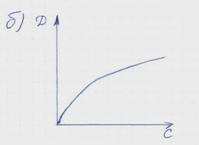
2.7.2 Электрохимические методы
1 К электрохимическим методам анализа относятся … .
а) кондуктометрия;
б) титриметрия;
в) кулонометрия;
г) полярография;
д) гравиметрия;
е) потенциометрия;
ж) спектрофотометрия.
2 Соответствие метода и измеряемого параметра:
а) полярография; 1) электродный потенциал
б) кондуктометрия; 2) количество электричества, израсходованного
на электролиз
в) кулонометрия; 3) электропроводность раствора
г) потенциометрия; 4) масса осадка, выделившегося на электроде
при электролизе
д) электрогравиметрия. 5) ток поляризации катода
3 В кондуктометрии электропроводность раствора зависит от … .
а) размеров электролитической ячейки;
б) концентрации электролита;
в) природы электролита;
г) объема электролита;
д) размеров и расположения электродов.
4 В формуле ![]()
а) a; 1) расстояние между электродами
б) x; 2) толщина электродов
в) S; 3) удельная электропроводность
г) d. 4) площадь электродов
5) электропроводность
6) степень электролитической диссоциации
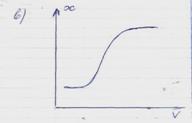
5 Кривая кондуктометрического титрования BaCl2 стандартным раствором Na2SO4:



6 В потенциометрии индикаторным электродом служит … .
а) ртутный;
б) стеклянный;
в) водородный;
г) хлорсеребряный.
7 Потенциал индикаторного электрода зависит от … .
а) рН раствора;
б) концентрации определяемых ионов;

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
