а) Cs+, Cd+, Y+3, Ce+4;
б) Cs+, Rb+, K+, Na+;
в) Mg+2, Ca+2, Sr+2, Ba+2;
г) Cu+2, Zn+2, Ga+3, Ge+4.
2.2 Аналитические реакции
2.2.1 Общие характеристики аналитических реакций
1 Требования к аналитическим реакциям … .
а) протекать быстро;
б) быть обратимой;
в) сопровождаться выпадением осадка, изменением окраски, выделением газа;
г) быть необратимой;
д) протекать при любых значениях рН;
е) быть высокочувствительной.
2 Наименьшая масса определяемого иона, которая может быть обнаружена с помощью данной реакции в наименьшем объеме исследуемого раствора называется … .
а) минимальной концентрацией;
б) отрываемым минимумом;
в) предельным разбавлением;
г) минимальным разбавлением.
3 Минимальной концентрацией, отрываемым минимумом и пределом разбавления характеризуется … аналитической реакции:
а) специфичность;
б) селективность;
в) чувствительность;
г) среди ответов нет верного.
4 Условия проведения аналитических реакций … .
а) соблюдение температурного режима;
б) соблюдение рН среды;
в) необратимость;
г) продолжительность во времени;
д) высокие концентрации реагирующих веществ;
е) наличие внешних эффектов.
5 Аналитическая реакция, позволяющая обнаружить ион в присутствии других ионов, называется … .
а) селективной реакцией;
б) групповой реакцией;
в) специфической реакцией;
г) среди ответов нет верного.
6 Реакция, в ходе которой несколько одновременно присутствующих ионов дают сходные внешние эффекты, называется … .
а) высокочувствительной;
б) специфической;
в) селективной;
г) среди ответов нет верного.
2.2.2 Кислотно-основные реакции
1 Согласно протолитической теории Бренстеда – Лоури кислота является ……..
а) акцептором протонов;
б) донором протонов;
в) и донором, и акцептором протонов;
г) нет верного ответа.
2 Вода выполняет роль кислоты в реакции … .
а) H2O + HF « F - + H3O+;
б) H2O + H2SO4 « H3O+ + HSO![]() ;
;
в) H2O + NH3 « H3O+ + HSO![]() ;
;
г) H2O + CH3COOH « CH3COO - + H3O+.
3 Согласно теории Льюиса основание является … .
а) акцептором пары электронов;
б) донором пары электронов;
в) и донором и акцептором электронной пары;
г) нет правильного ответа.
4 Соответствие кислоты и сопряженного с ней основания по теории Бренстеда – Лоури … .
а) H3O+; 1) OH–; 5) NH3.
б) NH4+; 2) CH3COO–;
в) CH3COOH; 3) H2O;
г) HClO4; 4) ClO![]() ;
;
5 Согласно теории Льюиса BCl3 является … .
а) основанием;
б) кислотой;
в) донором электронной пары;
г) акцептором электронной пары.
6 Ионная сила 0,05н раствора HCl равна … .
а) 0,05;
б) 0,01;
в) 0,1;
г) 0,2.
7 Ионная сила 0,01М раствора нитрата кальция равна... .
а) 0,01;
б) 0,02;
в) 0,03;
г) 0,05.
8 Ионная сила 0,0164 М раствора сульфата калия равна … .
а) 0,01;
б) 0,05;
в) 0,02;
г) 0,03.
9 Водородный показатель 0,05н раствора соляной кислоты равен … (![]() )
)
а) 1,5;
б) 1,2;
в) 1,4;
г) 2,0.
10 Водородный показатель 0,01М раствора гидроксида аммония равен (![]() ).
).
а) 5,4;
б) 9,3;
в) 10,5;
г) 11,2.
11 Раствор, содержащий протолитически равновесную систему, способную поддерживать постоянное значение рН при разбавлении или добавлении небольших количеств кислоты или щелочи, – это … раствор.
12 Буферный раствор – это … .
а) CH3COOK + CH3COONa;
б) NH4OH + NH4Cl;
в) NH4OH + HCl;
г) H3PO4 + NH4Cl.
13 Число моль-эквивалентов сильной кислоты или щелочи, которые нужно добавить к одному литру буферного раствора, чтобы изменить величину рН на единицу, – называется … .
а) буферной системой;
б) концентрацией буферного раствора;
в) буферной емкостью;
г) буферным коэффициентом.
14 Буферная ёмкость рассчитывается по формуле … .
а) 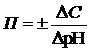 ;
;
б) 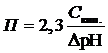 ;
;
в) ![]() ;
;
г) 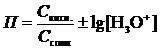 .
.
15 Согласно теории Бренстеда – Лоури вода является … растворителем.
а) протогенным;
б) апротонным;
в) амфипротным;
г) протофильным.
2.2.3 Редокс-реакции
1 В реакции SnCl2 + 2FeCl3 « SnCl4 + 2FeCl2 FeCl3 является … .
2 В редокс-реакциях азот в молекуле аммиака является … .
3 В редокс-реакциях галогены в молекулах галогеноводородов являются … .
4 Реальный редокс-потенциал рассчитывается по уравнениям:
а) 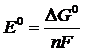 ;
;
б) ![]() ;
;
в) 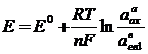 ;
;
г) 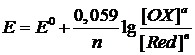 .
.
5 Величина реального редокс-потенциала системы MnO![]() + 8H+ + 5e = Mn+2 + + 4H2O при рН = 1 равна … В
+ 8H+ + 5e = Mn+2 + + 4H2O при рН = 1 равна … В ![]()
а) 1,59;
б) 1,42;
в) 1,15;
г) 1,85.
6 Формальный редокс-потенциал системы NO-2 + 2H+ + e « NO + H2O при рН = 1 равен … (![]()
а) 0,96;
б) 1,02;
в) 1,08;
г) 1,16.
7 Величина реального редокс-потенциала системы MnO![]() + 8H+ +5e = Mn+2 + + 4H2O при рН=5 равна ………В
+ 8H+ +5e = Mn+2 + + 4H2O при рН=5 равна ………В ![]()
а) 1,14;
б) 1,64;
в) 1,24;
г) 1,04.
8 Формальный редокс-потенциал полуреакции 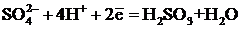 при рН = 1 равен … В
при рН = 1 равен … В ![]()
а) 0,05;
б) 0,12;
в) 0,07;
г) 0,03.
9 Окислить Fe(II) до Fe(III) можно галогеном …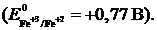
а) F2 ![]()
б) Cl2 ![]()
в) Br2 ![]()
г) I2 ![]()
10 Логарифм константы равновесия реакции 2SO![]() + 2NO
+ 2NO![]() + 4H+ = 2SO
+ 4H+ = 2SO![]() + 2NO + 2H2O равен …
+ 2NO + 2H2O равен … 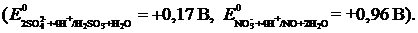
а) 70,35;
б) 74,24;
в) 80,34;
г) 82,15.
11 Наибольшего значения реальный редокс-потенциал системы
Cr2O![]() + 14H+ + 6e = 2Cr+3 + 7H2O
+ 14H+ + 6e = 2Cr+3 + 7H2O
достигнет при значении рН, равном … .
а) 0,5;
б) 2;
в) 5;
г) 10.
12 Логарифм константы равновесия реакции 2MnO![]() + 5HNO2 + H+ « 2Mn+2 + 5NO
+ 5HNO2 + H+ « 2Mn+2 + 5NO![]() + 3H2O равен …
+ 3H2O равен … 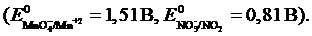
а) 60,12;
б) 59,32;
в) 48,54;
г) 27,15.
2.2.4 Реакции комплексообразования
1 В соединении Na3[Co(NO2)6]:
а) Na+; 1) ион-комплексообразователь;
б) Co+3; 2) лиганд;
в) NO![]() ; 3) ион внешней сферы;
; 3) ион внешней сферы;
г) [Co(NO2)6]3-. 4) внутренняя сфера.
2 К анионным комплексам относятся ………
а) [Cu(NH3)4]2+;
б) [Ni(CO)4];
в) [Zn(CN)4]2–;
г) [Ni(H2O)4]2+;
д) [Pt(NH3)2Cl2];
е) [Co(NO2)6]3–.
3 К аква-комплексам относятся … .
а) [PtCl3(NH3)3]Br;
б) [Cu(H2O)4]SO4;
в) [Zn(NH3)4]Cl2;
г) K2[PtCl4].
4 Общая константа нестойкости Fe(SCN)3 имеет вид … .
а) 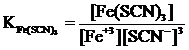 ;
;
б) 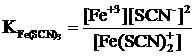 ;
;
в) 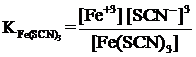
г) 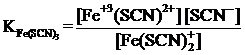 .
.
5 Наиболее устойчивый комплекс образует ЭДТА с катионом … (bму – константа устойчивости комплекса).
а) Al+3; 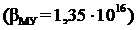 ;
;
б) Ca+2; 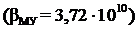 ;
;
в) Cu+2; 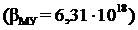 ;
;
г) Mg+2. 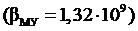 .
.
6 Наиболее устойчивый аммиачный комплекс – это … (b1 – константа устойчивости по первой ступени)
а)![]() ;
;

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
