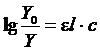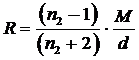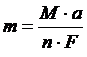4 Осадительное титрование | AgNO3 | Фиксирование конечной точки титрования по методам Гей-Люссака, Мора, Фольгарда, Фаянса |
Физико-химические методы анализа (ФХМА) основаны на проведении химических реакций, конец которых определяется по изменению какого-либо свойства анализируемого вещества с помощью приборов. Поэтому они ещё называются инструментальными. В аналитической практике используются также и физические инструментальные методы анализа (радиометрические, масс-спектрометрические, ЭПР, ЯМР и др.).
Спектрометрические методы анализа основаны на взаимодействии электромагнитного излучения с веществом. К ним относятся:
– эмиссионный спектральный анализ, основанный на изучении спектров излучения, или эмиссионных спектров, различных веществ;
– абсорбционный спектральный анализ, основанный на изучении спектров поглощения анализируемых веществ. К нему относятся:
1) спектрофотометрия (изучает поглощение анализируемым веществом света с определённой длиной волны);
2) фотометрия (изучает поглощение анализируемым веществом нестрого монохроматического света);
3) колориметрия (изучает поглощение света окрашенными растворами в видимой области спектра);
4) нефелометрия (изучает интенсивность света, рассеянного твёрдыми частицами суспензий);
5) турбидиметрия (измерение количества света, поглощённого неокрашенными суспензиями);
– люминесцентная спектроскопия, основанная на изучении свечения исследуемого объекта, возникающего под действием УФ-лучей.
Электрохимические методы анализа основаны на изучении и использовании процессов, протекающих на поверхности электрода или в приэлектродном пространстве.
Аналитическим сигналом в этих методах является электрический параметр (потенциал, сила тока, электропроводность), который зависит от концентрации определяемого вещества.
Различают прямые и косвенные электрохимические методы. В прямых методах используют зависимость электрического параметра от концентрации, в косвенных – этот параметр измеряют для нахождения конечной точки титрования (точки эквивалентности) определяемого компонента титрантом.
Таблица 16
Классификация электрохимических методов
Название электрохимического метода | Основан на измерении параметра (обозначение, ед. измерения) |
1 Потенциометрия | Потенциал индикаторного электрода Е, В |
2 Кондуктометрия | Удельная электропроводность раствора χ (каппа), См ∙ см |
3 Электрогравиметрия | Масса вещества, выделившегося на электроде при электролизе m, г |
4 Кулонометрия | Количество электричества, прошедшее через систему, Q, кл |
5 Вольтамперометрия (полярография) | Сила тока I, мкА (ток поляризации ртутного катода) |
Хроматография – физико-химический метод разделения компонентов сложных смесей газов, жидкостей или растворённых веществ, основанный на использовании сорбционных процессов в динамических условиях.
Хроматографические методы классифицируются по различным характеристикам (табл. 17).
Таблица 17
Классификация хроматографических методов
Характеристика | Классификация |
1 По агрегатному состоянию разделяемой смеси | – газовая; –жидкостная; –газожидкостная |
2 По механизму разделения | – адсорбционная; – распределительная; – ионообменная; – осадочная; – окислительно-восстановительная; – адсорбционно-комплексообразова-тельная |
3 По форме проведения процесса | – колоночная; – капиллярная; – плоскостная (бумажная, тонкослойная, мембранная) |
Таблица 18
Законы, лежащие в основе некоторых физико-химических методов анализа
Уравнение закона Бугера – Ламберта – Бера |
|
Уравнение молекулярной рефракции |
|
Уравнение Ильковича |
|
Уравнение Фарадея |
|
Уравнение для расчёта электропроводности |
|
Окончание табл. 18
Уравнение для расчёта удерживаемого объёма |
|
Уравнение для расчёта коэффициента удерживания |
|
Уравнение для расчёта высоты, эквивалентной теоретической тарелке |
|
Раздел II. РЕПЕТИЦИОННЫЕ ТЕСТЫ
2.1 Аналитические свойства веществ
2.1.1 Физические и химические свойства веществ
1 К физическим свойствам веществ относятся … .
а) агрегатное состояние;
б) кислотно-основные свойства;
в) окислительно-восстановительные;
г) цвет;
д) показатель преломления.
2 Фазовый переход характеризуется … .
а) температурой плавления;
б) температурой кипения;
в) температурой вспышки;
г) температурой возгонки.
3 В точке М вещество находится в агрегатном состоянии … .
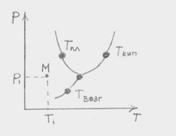
а) жидком;
б) твердом;
в) газообразном;
г) плазменном.
4 Температура кипения зависит от … .
а) давления
б) цвета вещества
в) степени чистоты вещества
г) показателя преломления
5 Цвет вещества, воспринимаемый глазом, обусловлен … .
а) взаимодействием электромагнитных колебаний с молекулами вещества;
б) избирательным поглощением и отражением веществом световой энергии определенной длины волны;
в) воздействием светового потока, прошедшего через вещество или отраженного от него, на сетчатку глаза;
г) нет верного ответа.
6 Характеристиками агрегатного состояния, используемыми в аналитических целях, являются … .
а) плотность;
б) температура затвердевания;
в) показатель преломления;
г) цвет.
7 Появление или изменение окраски неорганических и органических веществ обусловлены … .
а) степенью окисления;
б) ионизацией молекул при изменении рН среды;
в) наличием хромофорных групп в молекулах;
г) нет верного ответа.
8 Ион марганца (II) водной среде имеет … окраску.
а) фиолетово-малиновую;
б) желтую;
в) красно-оранжевую;
г) не имеет окраски.
9 Цвет органических молекул обусловлен наличием хромофорных групп:
а) CH3 ¾;
б) 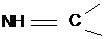 ;
;
в) NO2 ¾;
г) С3Н7.
10 Максимальная концентрация растворенного вещества в определенном объёме растворителя или раствора при данной температуре называется … этого вещества.
11 Соответствие концентрации и её сущности:
а) массовая доля; 1) количество граммов растворенного вещества в 1 мл раствора;
б) молярная; 2) количество моль растворенного вещества в 1 л раствора;
в) нормальная; 3) количество граммов растворенного вещества в 100 г раствора;
г) титр. 4) количество моль-эквивалентов растворенного вещества в 1 л
раствора.
12 При растворении вещество подвергается ряду физико-химических процессов:
а) электролизу;
б) диффузии;
в) диссоциации;
г) сольватации;
д) адсорбции.
13 К протофильным растворителям относятся молекулярные жидкости … .
а) бензол;
б) серная кислота;
в) тетраметилмочевина;
г) вода.
14 К амфипротным растворителям относятся молекулярные жидкости … .
а) метанол;
б) ацетонитрил;
в) ледяная уксусная кислота;
г) вода.
15 Обменные реакции между составными частями растворителя и растворенного вещества, приводящие к образованию слабодиссоциирующих или малорастворимых соединений, называются … .
16 Сильные окислители … .
а) NO![]() ;
;
б) Cr2O![]() ;
;
в) I– ;
г) MnO![]() ;
;
д) S2–;
е) BrO![]() .
.
17 Сильные восстановители … .
а) NO![]() ;
;
б) Cr2O![]() ;
;
в) I–;
г) MnO![]() ;
;
д) S2–;
е) BrO![]() .
.
18 Наибольшей окислительной способностью обладает ион … .
а) Cs+;
б) Cd+;
в) Y+3;
г) Ge+4;
д) V+5.
19 Справедливо утверждение: «С увеличением положительных зарядов ионов в периодах слева направо возрастают … и …»:
а) прочность комплексных соединений;
б) восстановительные свойства ионов;
в) атомные радиусы;
г) окислительные свойства ионов.
20 Основной характер оксидов и гидроксидов металлов усиливается в ряду … .

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)