На примере цианогенов интересно рассмотреть биохимическую адаптацию фитофагов к токсинам. У некоторых животных (овец, крупного рогатого скота) детоксикация цианида происходит следующим образом. Его превращает в тиоцианат фермент роданеза:
![]()
Сера поступает из p-меркаптопирувата (HSCH2CОCО2H), который превращается в пируват.
![Рис. 8. Токсичные и репеллентные для насекомых вещества растений [Jacobson, 1982] 1 - цианогенные гликозиды; 2 - (Е)-5-оцименон (ocimenone); 3 - линалоол (linalool); 4, а, б - пиретрины (pyrethrins); 5 - никотин (nicotine); 6 - анабазин (anabasine); 7- пеллиторин (pellitorine, изобутиламид декановой кислоты); 8 - спилантол (spilanthol) или аффинин (afiinin); 9 - эхинацеин (echinacein) или ?-саншоол (sanshool) (неогеркулин, neoherculin); 10 - анациклин (anacycline); 11 - лимонен (Ишопепе); 12 - госсипол (gossypol); 13 - 2-тридеканон *(2-tridecanone); 14 - ротенон (rotenone)](/text/80/389/images/image002_69.jpg)
Рис. 8. Токсичные и репеллентные для насекомых вещества растений [Jacobson, 1982] 1 - цианогенные гликозиды; 2 - (Е)-5-оцименон (ocimenone); 3 - линалоол (linalool); 4, а, б - пиретрины (pyrethrins); 5 - никотин (nicotine); 6 - анабазин (anabasine); 7- пеллиторин (pellitorine, изобутиламид декановой кислоты); 8 - спилантол (spilanthol) или аффинин (afiinin); 9 - эхинацеин (echinacein) или α-саншоол (sanshool) (неогеркулин, neoherculin); 10 - анациклин (anacycline); 11 - лимонен (Ишопепе); 12 - госсипол (gossypol); 13 - 2-тридеканон *(2-tridecanone); 14 - ротенон (rotenone)
Аналогичным образом при отравлении человека цианидом ему внутривенно вводят тиосульфат.
GN - + Na2S2О3 → CNS - + Na2SО3.
Цианогены имеются у центральноамериканских видов акаций, не образующих мутуализма с муравьями (некоторые другие виды акаций живут под патронажем муравьев, защищающих их от атаки других растительноядных насекомых).
Образование синильной кислоты в качестве защитного средства описано не только у растений, но также и у животных, например у многоножек (защита от нападений муравьев), у некоторых бабочек с предупреждающей окраской.
Глюкози-нолаты (glucosinolates, более 90). Встречаются у растений 10 семейств, в том числе Brassicaceae (синигрин). Токсичность связана с выделением изотиоцианатов (горчичных масел). Кроме того, что изотиоцианаты токсичны, они могут подвергаться дальнейшему превращению с образованием соответствующих тиоцианатов;
R - N = C = S ↔ R - S - C = N,
где R - алкил или бензил.
Последние у млекопитающих вызывают заболевание - гипертироидизм. Глюкозинолаты токсичны и для насекомых, и для крупного рогатого скота.
Изобутиламиды ненасыщенных алифатических кислот. Выделены из растений семейств сложноцветных и рутовых. Примерами являются (см. рис. 8): пеллиторин из корней Anacyclus pyrethrum DC.; спилантол (аффинин) из стебля Spilanthes oleracea Jacq. и из корней Heliopsis longipes (A. Gray) Blake, а также Н. scabra Dunal.; эхинацеин (другие названия - α-саншоол и неохеркулин) из корней Echinacea angustifolia DC., плодов и корней Zanthoxylum piperitum DC. и коры Z. clava-herculis L.; анациклин из корней Anacyclus pyrethrum DC. [Jacobson, 1982].
Алкалоиды (по-видимому, более 7000-8000). Найдены у растений многих семейств. Токсичные свойства растений, содержащих алколоиды, известны очень давно. Весьма гетерогенный класс веществ включает наряду с прочими следующие группы.
1. Производные пиридина и пиперидина. Примеры - н-холиномиметик никотин (из Nicotiana spp.), анабазин (открыт в среднеазиатском растении Anabasis aphylla L.; также содержится в Nicotiana spp.). Оба алкалоида применялись как инсектициды. Еще пример - кониин из болиголова Conium maculatum L. (рис. 9) (считается, что им был отравлен Сократ).
2. Производные пирролидина и тропана. Примеры - стахидрин, гигрин, кокаин, гиосциамин, м-холиноблокатор атропин (из красавки Atropa belladonna L.) .
3. Производные хинолина и изохинолина. Примеры - морфин, кодеин (из опийного мака Papaver somniferum L.), тубокурарин (блокатор н-холинорецепторов скелетных мышц; один из многих алкалоидов некоторых видов яда кураре), пеллотин, норлауданозолин, барберин.
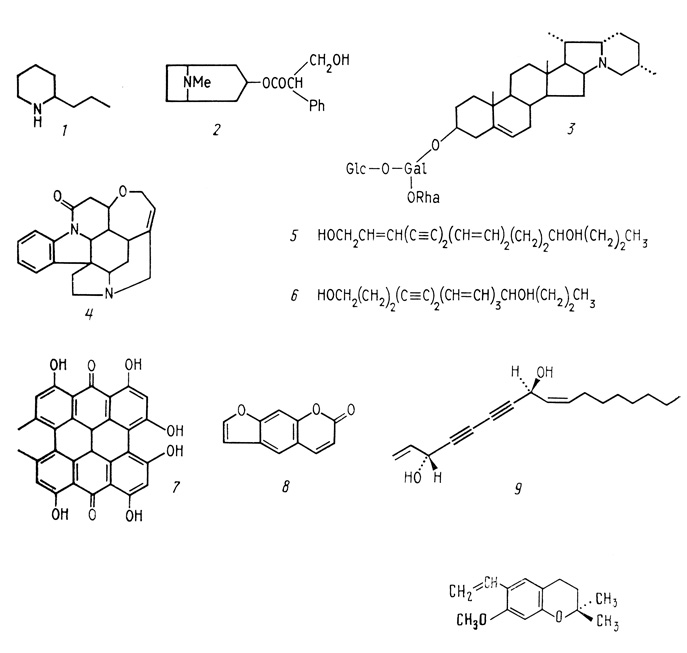 азотнесодержащие токсичные вещества: 5- энантетоксин (oenanthetoxin) Oenanthe crocata L.; 6 - цикутоксин cicutoxin) (Cicuta virosa L.); 7 - гиперицин (hypericin) Hypericum perforatum L.; 8 - псорален (psoralene) из листьев и стеблей зонтичных [Harborne, 1982]; 9 - фалькариндиол (falcarindiol) моркови -фактор устойчивости растений против нематод и фитоалексин - против грибных паразитов [Stadler, Buser, 1984]; 10 - 6-винил- 7-метокси-2,2- диметилхромен (6-vinyl-7-metoxy-2,2-dimethylchromene) из масла Hemizonia fitchii A. Gray (Asteraceae) [Klocke et al., 1985]" width="687 height=653" height="653""/>
азотнесодержащие токсичные вещества: 5- энантетоксин (oenanthetoxin) Oenanthe crocata L.; 6 - цикутоксин cicutoxin) (Cicuta virosa L.); 7 - гиперицин (hypericin) Hypericum perforatum L.; 8 - псорален (psoralene) из листьев и стеблей зонтичных [Harborne, 1982]; 9 - фалькариндиол (falcarindiol) моркови -фактор устойчивости растений против нематод и фитоалексин - против грибных паразитов [Stadler, Buser, 1984]; 10 - 6-винил- 7-метокси-2,2- диметилхромен (6-vinyl-7-metoxy-2,2-dimethylchromene) из масла Hemizonia fitchii A. Gray (Asteraceae) [Klocke et al., 1985]" width="687 height=653" height="653""/>
Рис. 9. Вещества растений, токсичные для фитофагов 1 - кониин (coniine) Conium maculatum L. (Umbelliferae); 2 - атропин (atropine) Atropa belladonna L. (Solanaceae); 3 - соланин (solanine) картофеля Solanum tuberosum L, j 4 - стрихнин (strychnine) Strychnos nuxvomica (Loganiaceae), азотнесодержащие токсичные вещества: 5- энантетоксин (oenanthetoxin) Oenanthe crocata L.; 6 - цикутоксин cicutoxin) (Cicuta virosa L.); 7 - гиперицин (hypericin) Hypericum perforatum L.; 8 - псорален (psoralene) из листьев и стеблей зонтичных [Harborne, 1982]; 9 - фалькариндиол (falcarindiol) моркови - фактор устойчивости растений против нематод и фитоалексин - против грибных паразитов [Stadler, Buser, 1984]; 10 - 6-винил - 7-метокси-2,2- диметилхромен (6-vinyl-7-metoxy-2,2-dimethylchromene) из масла Hemizonia fitchii A. Gray (Asteraceae) [Klocke et al., 1985]
4. Производные индола. Примеры - стрихнин (из Strychnos mix-vomica), хинамин (из хинного дерева Cinchona spp.), виндолин (из Vinca sp.), серпентин (из Rauwolfia serpentina Benth. et Kurz.), свыше 60 алкалоидов яда кураре.
5. Производные пурина: кофеин, теобромин и др.
6. Стероидные алколоиды. Примеры - соланин (из картофеля Salanum tuberosum L., см. рис. 9), а-томатин (из томата). Есть данные, что соланин может вызывать тератогенез у млекопитающих и снижать выживаемость потомства особей, получавших достаточно большую дозу соланина.
![Рис. 10. Судьба пирролизидиновых алкалоидов в организме фитофагов А - в организме млекопитающих. Природный алкалоид (J) подвергается гидролизу с образованием ретронецина (retronecine) (2), который дегидратируется с образованием опасного токсина пиррола-1 (pyrrole-1) (3); последний связывается в печени; Б - в организме некоторых видов бабочек. Природный алкалоид подвергается гидролизу с образованием ретронецина (2), а затем пиррола-2 (4) и пиррола-3 (5), которые накапливаются в особом парном органе (hair pencils), расположенном латерально на конце брюшка самца (описаны у данаид) [Harborne, 1982]](/text/80/389/images/image004_40.jpg)
Рис. 10. Судьба пирролизидиновых алкалоидов в организме фитофагов А - в организме млекопитающих. Природный алкалоид (J) подвергается гидролизу с образованием ретронецина (retronecine) (2), который дегидратируется с образованием опасного токсина пиррола-1 (pyrrole-1) (3); последний связывается в печени; Б - в организме некоторых видов бабочек. Природный алкалоид подвергается гидролизу с образованием ретронецина (2), а затем пиррола-2 (4) и пиррола-3 (5), которые накапливаются в особом парном органе (hair pencils), расположенном латерально на конце брюшка самца (описаны у данаид) [Harborne, 1982]
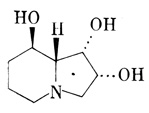
Рис. 11. Индолизидиновый алкалоид свайнсонин (swainsonine)
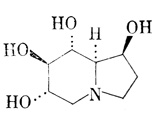
Рис. 12. Индолизидиновый алкалоид кастаноспермин (castanospermin)
7. Производные имидазола, например высокотоксичный м-холиномиметик (мускариномиметик) пилокарпин (из Pilocarpus pinna - tifolius Jaborandi, Южная Америка), применяемый в медицине при глаукоме.
8. Ациклические алкалоидные амины: эфедрин, антимитотические токсины колхицин и колхамин (из безвременника Colchicum spp.) и др. Колхамин применяется для лечения рака кожи.
9. Аконитовые алкалоиды, например обладающий курареподоб - ной активностью метилликаконитин (из живокости Delphinium spp.), используемый в медицине, и другие алкалоиды.
10. Пирролизидиновые алкалоиды (например, [Robins, 1985]). Некоторые бабочки, среди которых не менее 24 видов Danainae, [Ackery, Vane-Wright, 1984] используют пирролизидиновые алкалоиды для синтеза феромонов (см. разд. 5.1.1). Например, самцы бабочек данаид посещают растения из семейств бурачниковых и сложноцветных для получения этих алкалоидов. Из них в организме самцов вырабатываются ароматические вещества, привлекающие самок, например пиррол-2 и пиррол-3 (рис. 10).
Пирролизидиновые (и некоторые другие) алкалоиды накапливаются некоторыми растительноядными насекомыми. Накопление токсинов растений показано для более чем полутора сотен видов насекомых (чешуекрылые, сетчатокрылые, клопы, жуки, двукрылые, прямокрылые). Есть данные, что накапливаемые токсины защищают насекомых от хищников, как позвоночных, так и беспозвоночных, например пауков [Keith, 1984].
Накапливаться в насекомых могут и другие алкалоиды. Так, совка Heliothis zea способна накапливать алкалоид томата α-томатин, получаемый с пищей при кормлении на растениях томата. Этот алкалоид защищает ее от паразитоида Hyposoter exiguae (Viereck) (Hymenoptera), который используется как средство биологической борьбы с совкой [Campbell, Duffey, 1981]. Это же алкалоид, α-томатин, действует как моллюскоцид, убивая переносчика шистозомоза моллюска Biomphalaria glabrata при концентрации всего 4 млн-1 [Hostettmann et al., 1982].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



