Приведем другие примеры алкалоидов. В растениях найдены алкалоиды, которые близки по своей структуре некоторым сахарам [Fellows, 1987] и вследствие этого ингибируют ферменты, участвующие в метаболизме углеводов. Некоторые токсичные алкалоиды, такие, как свайнсоннн (swainsonine) из Swainsona sp. (рис. 11) и кастаноспермин (castanospermine) из Castanospermum australe
A. Cunn (рис. 12), проявили себе как перспективные вещества для исследования и лечения некоторых видов рака.
Дополнительная информация о токсичных или фагорепеллентных алкалоидах дана в работах [Robins, 1985; Pelletier, 1987].
Быстрое накопление новой информации об алкалоидах растений характеризует тот факт, что за 1 год выделяют одних только новых пирролизидиновых алкалоидов около 15 [Robins, 1985], апорфиноидных (aporphinoid) алкалоидов свыше 20 [Shamma, Guinaudeau, 1985]. Думается, что общее число ежегодно выделяемых новых алкалоидов растений по меньшей мере на порядок выше.
Пептиды. Примерами токсичных пептидов могут служить вискотоксин из омелы белой Viscnm album, а также некоторые токсины грибов (см. гл. 3).
Белки. Примерами токсичных белков являются лектины. В семенах африканского растения Abrus precatorius L. (сем. бобовые) содержится абрин (abrin). Летальная доза его для человека около 0,5 мг. Семена ярко окрашены, используются африканцами для изготовления украшений, и случаи отравления ими действительно зарегистрированы.
В семенах клещевины Ricinus communis L. содержится токсичный рицин (ricin).
Содержащиеся в семенах покрытосеменных другие лектины также могут быть токсичны для фитофагов (например, [Liener et al., 1986]). В семенах сои Glycine max (L.) Merr. и ряда других растений найдены белки - ингибиторы протеаз. Они могут снижать пищевую ценность семян для фитофагов.
Накапливаются новые данные о содержащих азот токсинах растений (табл. 17).
Токсины растений, не содержащие азот. В эту разнообразную группу токсинов входят соединения, относящиеся к различным по химизму классам веществ: гликозиды, сапонины, терненоиды, флавоноиды, хиноны, полиацетилены (полиины), пиретрины и др.
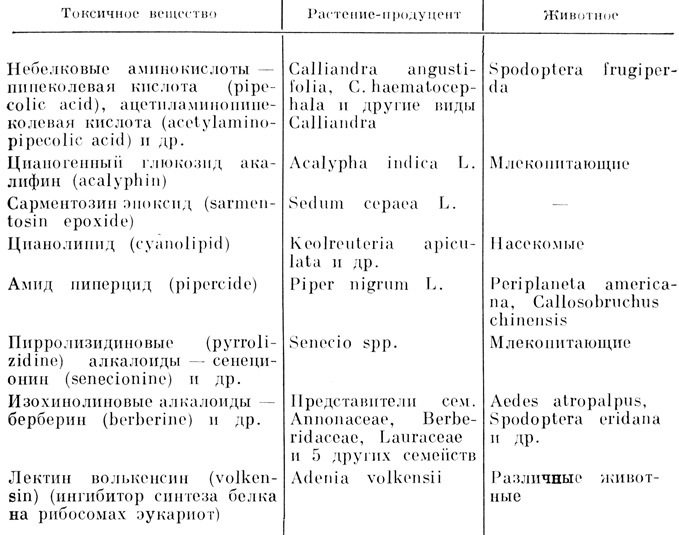
Таблица 17. Некоторые азотсодержащие вещества растений, токсичные для животных-фитофагов
А. Группа негликозидных токсинов. Простейшим примером может служить монофторуксусная кислота CH2FCО2H. Она встречается в некоторых южноафриканских растениях, например Dichapetalnm cymosum Engl. Этот яд ингибирует цикл Кребса. Для человека летальная доза 2-5 мг/кг веса тела.
Еще одним простым по структуре, но эффективным токсином оказался 2-тридекапон. Его пары высокотоксичны для тлей Aphis gossypii Glover, а также личинок табачного бражника Mandnca sexta (L.) и совок Heliothis zea (Boddie) [Jacobson, 1982]. Содержание 2-тридеканона в диком виде томата Lycopersicon hirsutum f. glabratum С. H. Mull, примерно в 70 раз превышает его концентрацию в тканях культивируемого томата L. esculentum Mill.
Большой группой веществ, среди которых есть токсичные (но чаще антифидантные и репеллеитные, см. разд. 4.1.3.) соединения, являются терненоиды (табл. 18). К ним относятся монотернены (более 1100), сесквитерпены (более 1300), дитерпены (более 1100).
Терпеноидные альдегиды, в том числе госсипол, участвуют в создании резистентности растений к нематодам [Hedin et al., 1984].
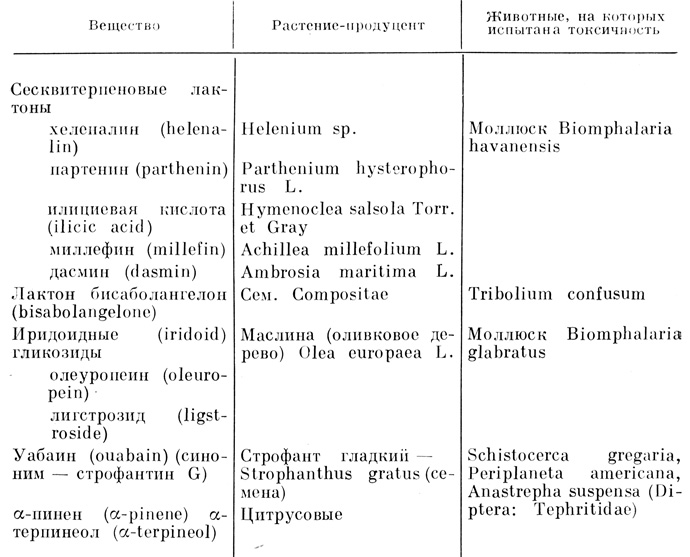
Таблица 18. Некоторые не содержащие азота вещества растений, токсичные для животных
К токсичным терпеиоидам относится целый ряд веществ, в том числе сапонины. Примером последних служит медикагеновая кислота из листьев Medicago sativa L. (люцерна). Она токсична для насекомых и рыб.
Терпен лимонен оказался эффективным инсектицидом против жуков Callosobruchus pliasecoli Gyli. (Taylor, Vickery, 1974; см. [Jacobson, 1982]).
Весьма интересная группа токсинов - многообразные форболовые эфиры растений семейств Euphorbiaceae и Thymelaeaceae. Эти вещества вызывают отравление выпасаемых домашних животных; они широко применяются при исследовании канцерогенеза. Биологическому действию форболовых эфиров посвящена большая литература.
Были обнаружены новые токсичные дитерпеновые эфиры в невысоком кустарниковом растении Pimelea prostrata Willd. (сем. Thymelaeaceae), эндемике Новой Зеландии. Эти вещества делают пимелею токсичной для домашнего скота. Среди этих токсичных веществ найдены производные тиглиана, дафнана и 1-а-алкил - дафнана. Вещества последней группы проявили себя как промоторы (promotors) раковой опухоли [Zayed et al., 1982]. Некоторые из этих веществ и близкие им по структуре соединения найдены у других растений из того же семейства, например в корнях не отропического кустарника Daphnopsis racemosa Griseb. [Adolf, Hecker, 1982].
Флавоноиды (более 1500-1600) широко распространены среди покрытосеменных, голосеменных папоротников и мхов; обладают чрезвычайно разнообразной биологической активностью. Многие флавоноиды представляют интерес с медицинской и ветеринарной точки зрения.
Представить флавоноидов - ротенон из корней Derris, Теphrosia и Lonchocarpus (сем. бобовые), токсичный для насекомых и рыб, ингибирует цепь переноса электронов в митохондриях и используется как пестицид; ротенон применяется в биохимии при исследовании биоэнергетики митохондрий. Ряд токсичных флавоноидов (например, рутин) выделен из томатов Lycopersicon esculenlnm Mill.; показана их токсичность для одного из вредителей томатов - совки Heliothis zea (Boddie).
Xиноны (более 550). Представитель хинонов - гиперицин из листьев зверобоя Hypericum perforatum, токсичный для млекопитающих.
Полиины, или полиацетилены (по-видимому, более 1700), встречаются у покрытосеменных (в том числе сем. Apiaceae и Asteraceae), а также у грибов. Некоторые из них токсичны и несут несколько экологических функций как аллелопатические вещества, стимуляторы овинозиции, фитоалексины.
Представители полиацетиленов - цикутотоксин из корней Cicuta virosa L. и энантетоксин из корней Oenanthe crocata L. (оба растения из сем. зонтичных), токсичные для млекопитающих.
Простые фенолы (более 200-220) обычны в растениях, имеют выраженную биологическую активность и несут, по-видимому, одновременно несколько экологических функций. Часто имеют антимикробную, антифидантную, аллелопатическую активность.
Среди других токсичных метаболитов растений обнаружены w-алкилфенолы, выделенные из латиноамериканского (Бразилия, Парагвай) лекарственного растения Schinus terebiiithifolius Raddi (Anacardiaceae) [Skopp et al., 1987]. Эти же вещества являются продуктами биодеградации в биосфере загрязняющих веществ, попадающих в экосистемы в составе некоторых детергентов. Ранее считалось, что к-алкилфенолы - типично антропогенные вещества. Теперь они обнаружены и как биогенные соединения.
Пиретрины (pyrethrins). Эти производные циклопропапкарбоновой кислоты из Chrysanthemum cinearifollum Vis. Известны инсектицидными свойствами с глубокой древности, когда применяли порошок из размолотых цветков растения-продуцента. Природная смесь пиретрииов состоит из шести веществ, представленных сложными эфирами хризантемовой или пиретриповой кислоты и алициклических кетоспиртов: пиретролона, жасмолопа и цинеролона [Мельников, 1987]. Экологически интересно, что ииретрипы - пример природных токсинов, в структуре которых запрограммирована способность быстро разлагаться в окружающей среде, т. е. та экологическая безвредность, к которой не всегда успешно стремятся создатели синтетических пестицидов. Под действием света боковая цепь хризантемовой кислоты окисляется с образованием нетоксичных соединений. Кроме того, спиртовая часть молекулы также имеет низкую фотохимическую стабильность и окисляется кислородом воздуха с утратой токсичных свойств.
Ценность пиретринов не только в том, что они применялись как инсектициды, но и в том, что они послужили моделью для синтеза в промышленных масштабах большого числа пестицидов - синтетических аналогов пиретринов (пиретроидов). Наиболее важный среди них - аллетрин и свыше 20 других препаратов [Мельников, 1987].
Растения могут поглощать и накапливать в своих тканях микотоксины, вырабатываемые почвенными грибами, и эти микотоксины становятся защитой от фитофагов.
Так, растение южноамериканской саванны Baccharis caridifolia DC. из сем. сложноцветных (называемое в Бразилии mio-mio, в Аргентине - romerillo) накапливает в своих тканях микотоксины из группы макроциклических трихотеценов (trichothecenes), которые, по-видимому, продуцирует почвенный гриб Myrothecimn verrucaria [Habermehl et al., 1985]. Среди девяти трихотеценов, найденных в тканях этого растения, описаны два новых токсина - миофито - цены (miophytocenes) А и В. Эти токсины имеют практическое значение, так как вызывают отравление пасущегося скота.
Среди микотоксинов экологически интересны и афлатоксины - афлатоксин В и другие, образуемые, например, грибом Aspergillus, flavus. Последний пример имеет прямое отношение к высшим растениям, поскольку этот гриб растет на арахисе - Arachis hypogea и других растениях. Можно предполагать, что растение благодаря наличию на них грибов может снижать пресс со стороны животных-фитофагов.
Б. Гликозиды и их экологическое значение для насекомых. Сердечные гликозиды (карденолиды, cardenolides) - ряд соединений, которые имеют стероидную структуру и обладают кардиотонической активностью. Их примерами служат дигитоксин, дигоксип, строфантин G (уабаин), олеандрин и многие другие. Они ингибируют мембранные АТФазы, оказывают мощное воздействие на обмен К+, Na+ и Са+ и на многие физиологические процессы.
Эти защитные вещества растений обладают большой мощью: об этом говорит, например, тот факт, что передозировка лекарств с сердечными гликозидами может привести к смерти пациента.
Гликозиды участвуют в следующей интересной системе взаимоотношений между растениями и животными [Rothschild, 1972; Harborne, 1982].
1. Ряд видов растений, например ваточник Asclepias curassavica L. и другие представители этого рода (сем. ластовневых Asclepiadaceae), а также олеандр Nerium oleander L. (сем. кутровых Ароcynaceae), образуют сердечные гликозиды, служащие пассивной; защитой от фитофагов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



