б) Cu(OH)2 + H2SO4 =; г) Ba(OH)2 + H4P2O7 =;
в) Ca(OH)2 + H3PO4 =; е) Mg(OH)2 + H4SiO4 =.
При окислении фосфора было израсходовано 16 г кислорода. Полученный фосфорный ангидрид растворили в 50 см3 25 %-ного раствора гидроксида натрия, плотностью 1,28 г/см3. Какая соль при этом образовалась и какова ее массовая доля в растворе? Какой из следующих гидроксидов обладает наиболее основным характером и почему: Ga(OH)3, In(OH)3 или Tl(OH)3?Вариант 13
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:а) P→P2O5→H3PO4→Ca3(PO4)2 →CaHPO4→Ca(H2PO4)2;
б) KNO3→O2→CO2→O2→H2O→O2→P2O5.
Сколько граммов сернистого газа выделится при взаимодействии 6,4 г меди с концентрированной серной кислотой. Составьте формулы нормальных и кислых солей угольной и мышьяковистой кислот и металлов калия и кальция.Вариант 14
Как получить ортофосфорную кислоту из ее кальциевой соли Ca3(PO4)2? Хлорид меди CuCl2 из оксида меди CuO? Какое количество серы выпадет в осадок при пропускании 11,2 л сероводорода (н. у.) через раствор, содержащий 41 г сернистой кислоты? Написать эмпирические и графические формулы следующих кислых солей: а) гидросульфида бария; б) гидрокарбоната лития; в) гидроортоарсената алюминия.Вариант 15
Напишите молекулярные и ионные уравнения реакций следующих превращений:а) Fe → FeSO4 → Fe(OH)2 → Fe(OH)3 → Fe2(SO4)3;
б) Fe → Fe2O3 → FeCl3 → Fe(OH)3 → K[Fe(OH)4].
Вариант 16
Составьте молекулярные и ионные уравнения реакций растворения гидроксида хрома(III) в растворах серной кислоты и гидроксида натрия. Сколько граммов Na[Cr(OH)4] образуется, если в реакцию вступило 32 г гидроксида натрия? Какими физическими свойствами обладают кислоты? Какие индикаторы вы знаете, и как кислоты изменяют цвет индикаторов? Напишите схемы образования молекул следующих соединений: а) CaS, FeCl2, Al2O3, CsF; б) BaO, Rb2S, AlF3, KBr.Вариант 17
Напишите в полной и сокращенной ионной формах уравнения следующих реакций:а) Ca(NO3)2 + K2CO3 →; б) Na2SiO3 + Ba(OH)2 →;
б) Fe(OH)2 + HNO3 →; г) AlCl3 + AgNO3 →;
в) MgCO3 + HCl →.
2. Оксид углерода можно получить при взаимодействии углерода с оксидом железа(III). Составьте уравнения реакции и вычислите, сколько литров оксида углерода(II) образуется из оксида железа(III) массой 80 г?
3. Переведите сульфат магния в основную и кислую соли, а гидрокарбонат железа и сульфит гидроксокальция в нормальные соли.
Вариант 18
Исходя из предложенных оксидов получите гидроксиды и дайте им название: CrO3, Ta2O5, MoO3, NiO, P2O5, Sb2O3, OsO4, Cl2O7. Укажите, к какому типу гидроксидов относится каждый из них. Составьте уравнения реакций для следующих превращений: фосфор → фосфорный ангидрид → фосфорная кислота → дигидрофосфат аммония → фосфат аммония. При взаимодействии избытка сульфата калия с раствором нитрата свинца(II) образовался осадок массой 9,09 г. Сколько граммов нитрата свинца(II) содержалось в растворе?Вариант 19
Составьте формулы средних и основных солей железа(III) с серной и азотной кислотами. Дайте им названия. Сколько Mn3O4 можно получить из 10 кг MnO2? Сколько кислорода выделиться при этом? Составьте уравнения реакций между соответствующими кислотами и основаниями, приводящих к образованию следующих солей: Ni(NO3)2, NaHCO3, Na2HPO4, K2S, K2HAsO3, CaHPO4. Дайте названия данным солям.Вариант 20
Составьте уравнения реакций получения кислых солей сернистой кислоты и металлов калия и кальция. Запишите формулы следующих кислот: йодистоводородной, метафосфористой, сернистой, ортокремниевой, метавольфрамовой, метахромовой, ортоалюминиевой, хлорной и хлороводородной. В какой массе воды следует растворить 8,5 г иодида калия, чтобы каждый грамм полученного раствора содержал 0,05 г иодид-ионов?Вариант 21
Могут ли взаимодействовать друг с другом: ZnO и FeO, K2O и Al2O3, Na2O и MgO, CO2 и BaO, N2O5 и Fe2O3, Cl2O7 и Al2O3, SO3 и N2O5, P2O5 и K2O. Напишите уравнения возможных реакций, дайте соответствующие названия полученным соединениям. Сколько молей азотной кислоты пойдет на нейтрализацию 11,1 г гидроксида кальция? Напишите эмпирические и графические формулы следующих основных солей: нитрата дигидроксомагния, сульфата гидроксоцинка, хлорида гидроксожелеза(III).Вариант 22
Запишите уравнения реакций, показывающих амфотерный характер оксидов бария, цинка, олова, алюминия и хрома. Напишите уравнения образования основных солей из следующих веществ: а) гидроксида магния и соляной кислоты; б) гидроксида меди(II) и серной кислоты; в) гидроксида кальция и фосфорной кислоты; г) гидроксида железа(III) и сернистой кислоты. Напишите графические формулы полученных солей. Оксид магния массой 15 г обработали раствором, содержащим 28 г серной кислоты. Сколько граммов соли образовалось?Вариант 23
Напишите графические формулы следующих оксидов: Cr2O3, SiO2, N2O5, SO3, Mn2O7, MnO3, OsO4. Какое количество цинка и 20 %-ной серной кислоты потребуется для получения 56 л водорода? Допишите недостающие соединения в уравнениях химических реакций:а) Na2O + ⋅⋅⋅⋅⋅⋅=⋅⋅⋅⋅⋅⋅⋅⋅+ H2O; б) KOH + ⋅⋅⋅⋅⋅ = ⋅⋅⋅⋅⋅⋅⋅ + H2O;
б) ⋅⋅⋅⋅⋅+ SO2 = ⋅⋅⋅⋅⋅⋅⋅; г) H2SO4 + ⋅⋅⋅⋅⋅= ⋅⋅⋅⋅ + H2O;
в) SiO2 + CaO = ⋅⋅⋅⋅⋅; е) ZnS + ⋅⋅⋅⋅⋅⋅⋅⋅= Zn(HS)2 +.
Вариант 24
Сколько граммов водорода можно получить при взаимодействии железа массой 11,2 г с соляной кислотой. Допишите недостающие соединения в уравнениях реакций:а) Zn(NO3)2 + ⋅⋅⋅⋅⋅⋅⋅ = ZnOHNO3; б) ZnSO4 + ⋅⋅⋅⋅⋅⋅⋅= Zn(HSO3)2 +;
б) Cu(HCO3)2 + ⋅⋅⋅⋅⋅= ⋅⋅⋅⋅⋅⋅⋅+ H2O; г) FeOHSO4 + ⋅⋅⋅⋅⋅= ⋅⋅⋅⋅⋅⋅+ H2O.
3. Какие из перечисленных оксидов можно растворить в соляной кислоте, а какие в гидроксиде натрия: Rb2O, BiO, CaO, CuO, Al2O3, SO3 N2O5. Напишите уравнения возможных реакций и названия полученных веществ.
Вариант 25
Исходя из предложенных оксидов получите гидроксиды, укажите к какому типу гидроксидов они относятся: оксид калия, оксид бериллия, оксид магния, оксид хрома(III), оксид хрома(VI), оксид тантала(V), оксид никеля, оксид алюминия(III), оксид молибдена (VI). Смешали 7,3 г хлороводорода с 4 г аммиака. Сколько граммов хлорида аммония образуется? Избыток какого газа и в каком количестве останется после реакции? Написать формулы следующих солей (приведя для каждой из них другое название): сернокислый магний, азотнокислый алюминий, хлорнокислый алюминий, хлорноватокислый алюминий, сернокислое железо-окисное, марганцовокислый калий.2. ХИМИЧЕСКИЙ ЭКВИВАЛЕНТ
Эквивалентом элемента называется такое его количество, которое присоединяет или замещает в химических реакциях 1 моль атомов водорода или Ѕ моль атомов кислорода.
Пример 1. Определите эквивалент и эквивалентные массы элементов в соединениях с водородом: H2O, HCl, PH3.
Решение. Эквивалент есть количество вещества и выражается в молях.
Э = 1/В моль,
где Э – эквивалент элемента;
В – валентность элемента.
В указанных соединениях эквивалент кислорода равен 1/2 моль, эквивалент хлора равен 1 моль, а эквивалент фосфора 1/3 моль.
Масса одного эквивалента элемента, выраженная в граммах, называется его эквивалентной массой (mэ).
mэ = М/В г/моль,
где М – молярная масса атома элемента;
mэ(О) = 16/2 = 8 г/моль;
mэ(Cl) = 35,5/1 = 35,5 г/моль;
mэ(Р) = 30,9/3 = 10,3 г/моль.
Пример 2. Определите эквивалентные массы следующих соединений: CO2, H2SO4, Cu(OH)2, MgCl2.
Решение. Эквивалентные массы сложных веществ вычисляют по следующим формулам: mэ(оксида) = 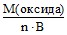 ,
,
где М – молярная масса оксида;
n – число атомов элемента в оксиде;
В – валентность элемента.
mэ (кислоты) = М (кислоты)/основность кислоты;
mэ (основания) = М (основания)/кислотность основания;
mэ (соли) = М (соли)/n⋅В;
где n – число атомов металла;
В − валентность металла.
mэ(CO2) = 44/1⋅ 4 = 11 г/моль; mэ(H2SO4) = 98/2 = 49 г/моль;
mэ(Cu(OH)2) = 98/2 = 49 г/моль; mэ(MgCl2) = 95/2 = 47,5 г/моль.
Пример 3. На нейтрализацию кислоты массой 2,18 г израсходовано KOH массой 2,49 г. Определите эквивалентную массу кислоты.
Решение. Эквивалентную массу KOH рассчитаем по формуле:
mэ(KOH) = М(KOH)/кислотность = 56/1 = 56 г/моль.
Эквивалентную массы кислоты определим исходя из закона эквивалентов: m(KOH)/m(кислоты) = mэ(KOH)/mэ(кислоты)
![]() =
= ![]()
![]() =
= ![]() = 49 г/моль
= 49 г/моль
Пример 4. Определите массу металла, вступившего в реакцию с кислотой, если при этом выделился водород объёмом 260 мл при нормальных условиях. Эквивалентная масса металла mэ(Ме) = 9 г/моль.
Решение. Согласно закону эквивалентов массы (объёмы) реагирующих друг с другом веществ пропорциональны их эквивалентным массам (объёмам).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 |



