Вариант 22
При взаимодействии ортофосфорной кислоты со щелочью образовалось соль Na2HPO4. Найти для этой реакции эквивалентную массу ортофосфорной кислоты. В состав метана входит 25 % водорода и 75 % углерода. Чему равна эквивалентная масса углерода. Вычислите эквивалент металла и его оксида, зная, что 0,304 г металла вытесняет из кислоты 0,282л кислорода (н. у.).Вариант 23
Определите эквивалентную массу гидроксида магния в реакциях:а) Mg(OH)2 + HBr = MgOHBr +H2O;
б) Mg(OH)2 + 2HBr = MgBr2 + 2 H2O.
2. При восстановлении 1,506 г оксида олова водородом образовалось 0,36 г воды. Определите эквивалентную массу олова и его валентность. Напишите формулу оксида олова.
3. Какой объём водорода (н. у.) выделится при взаимодействии 3,6 г металла с кислотой, эквивалентная масса которого равна 12 г/моль?
Вариант 24
Определите эквивалентные массы следующих солей: NaNO2, Cr2(SO4)3, CH3COOH, MgOHNO3, LiHSO4. Эквивалентная масса металла равна 56,2 г/моль. Вычислите процентное содержание этого металла в его оксиде. При взаимодействии 3,182 г галогена израсходовано 140,4 мл кислорода (н. у.). Вычислите эквивалент галогена и назовите его.Вариант 25
3. СТРОЕНИЕ АТОМА
Пример 1. Напишите электронные формулы атомов углерода и серы и формулы соединений их с кислородом и водородом.
Решение. Электронная формула атома углерода 6С 1s22s22p2, он имеет четыре валентных электрона, для него характерны степени окисления +2, +4, –4 (до восьмиэлектронного внешнего уровня не достает 4 электрона). С+2О – оксид углерода(II), С+4O2 – оксид углерода(IV), C-4H4 – метан. Электронная формула атома серы 16S 1s22s2p63s23p4. Для серы характерны степени окисления –2, +4, +6. S+4O2 – оксид серы(IV), S+6O3 – оксид серы(VI), H2S–2 – гидрид серы (II).
Пример 2. Изобразите электронные и электронно-графические формулы атомов 5В и 21Sc. Укажите валентные электроны. К какому семейству относятся атомы данных элементов?
Решение. Электронная формула атома бора 5В 1s22s22p1
валентные электроны
Ответ: бор относится к р – элементам
21Sc 1s22s22p63s23p63d14s2
Ответ: скандий относится к d-элементам.
Пример 3. Рассчитайте среднюю массу атома хлора.
Решение. Молярная масса атома хлора равна 35,45 г ⋅ моль-1. 1 моль любого вещества содержит 6,02 · 10 23 (число Авогадро, NА) структурных единиц, например, атомов.
6,02 · 1023 атомов хлора имеют массу 35,45 г
1 атом >>>>>>>>>>>>>>>> Х
Х=![]()
Ответ: mCl = 5,89⋅10 –23 г.
Пример 4. Рассчитайте радиус атома магния ![]() Mg=1,74 г ⋅ см -3.
Mg=1,74 г ⋅ см -3.
Решение. В твердом состоянии атомы многих металлов образуют так называемую плотнейшую упаковку. В плотнейшей упаковке атомы (шары) занимают 74 % объема. Объем одного атома V= 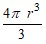 , один моль атомов (NА) имеет объем Vмоль =
, один моль атомов (NА) имеет объем Vмоль = 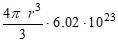 см 3. Этот объем составляет 74 % молярного объема Vмоль. Отсюда
см 3. Этот объем составляет 74 % молярного объема Vмоль. Отсюда ![]() = 0,74Vмоль = 0,74⋅
= 0,74Vмоль = 0,74⋅![]() , где АMg – молярная масса магния.
, где АMg – молярная масса магния.
АMg = 24,3 г ∙ моль-1. r = 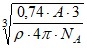
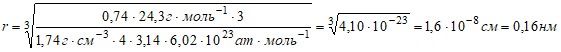
Ответ: rMg = 0,16 нм.
Пример 5. Из какого числа атомов состоят 1г и 1 см3 магния?
Решение. 6,02⋅1023 атомов магния имеют массу 24,3 г
Х >>>>>>>>>>>>>>>>>>>>>> 1г
Х = ![]()
Плотность магния с = 1,74 г ⋅ см –3, следовательно, 1 см 3 имеет массу 1,74 г.
6,02⋅10 23 атомов магния имеют массу 24,3 г
Y >>>>>>>>>>>>>>>>>>>>>>>>> 1,74 г
Y = ![]()
Ответ: n1 = 2,48 ⋅ 10 22 ат; n2 = 4,31 ⋅ 10 22 ат.
Вариант 1
Напишите электронные формулы атомов с зарядом ядра 8 и 19. Составьте графические схемы заполнения электронами валентных орбиталей этих атомов. Почему у элементов седьмой группы марганца преобладают металлические свойства, а у хлора – неметаллические? Ответ мотивируйте, исходя из электронного строения атома этих элементов. Напишите формулы высших оксидов элементов и соответствующих им гидроксидов. Рассчитайте среднюю массу атомов циркония и гафния.Вариант 2
Какие орбитали атома заполняются электронами раньше 4d или 5s; 6s или 5p? Почему? Составьте электронную формулу атома элемента, порядковый номер которого 21. Почему у элементов пятой группы ванадия преобладают металлические свойства, а у фосфора – неметаллические? Ответ мотивируйте, исходя из электронного строения атома этих элементов. Напишите формулы высших оксидов элементов и соответствующих им гидроксидов. Рассчитайте среднюю массу атомов водорода и селена.Вариант 3
Составьте электронные формулы атомов элементов с порядковыми номерами 8 и 25. Какие электроны этих атомов являются валентными? Какую низшую степень окисления проявляют сера и азот. Почему? Составьте формулы соединений кальция с атомами данных элементов в этой степени окисления и назовите их. Рассчитайте среднюю массу и размер атома железа. сFe = 7,8 г·см –3.Вариант 4
Составьте электронные формулы атомов элементов с порядковыми номерами 13 и 22. К какому электронному семейству относится каждый из этих элементов? Какие степени окисления может проявлять атом марганца? Ответ мотивируйте, исходя из электронного строения атома. Напишите формулы соответствующих оксидов и гидроксидов. Пылинка алюминия имеет массу 10 –8 г. Из какого числа атомов она состоит. сAl = 2,7 г · см –3.Вариант 5
Напишите электронно-графическую формулу атома серы в состоянии, предшествующем образованию ею соединения SF6. Какие степени окисления может проявлять атом хрома. Ответ мотивируйте, исходя из электронного строения атома. Напишите формулы соединений, соответствующих этим степеням окисления, назовите их. Рассчитайте среднюю массу атомов циркония и гафния.Вариант 6
Составьте электронные формулы атомов элементов с порядковыми номерами 15 и 25. К какому электронному семейству относится каждый из этих элементов? Какие степени окисления может проявлять атом селена? Ответ мотивируйте, исходя из электронного строения атома. Напишите формулы соединений, соответствующих этим степеням окисления, назовите их. Рассчитайте среднюю массу и размер атома кальция.сСa =1,54 г · см –3.
Вариант 7
Запишите электронные формулы атомов с зарядом ядра 9 и 20. Составьте графические схемы заполнения электронами валентных орбиталей этих атомов. Какие степени окисления может проявлять атом титана? Ответ мотивируйте, исходя из электронного строения атома. Напишите формулы соединений, соответствующих этим степеням окисления, назовите их. Рассчитайте среднюю массу и размер атома кобальта. сСо = 8,84 г · см –3.Вариант 8
Определите положение атома элемента в периодической системе по его электронной формуле: 2s22p3; 3s23p5; 4s23d8. Какие степени окисления может проявлять атом железа? Ответ мотивируйте, исходя из электронного строения атома. Напишите формулы соответствующих оксидов и гидроксидов. Из какого числа атомов состоят 2 г и 1 см 3 никеля.сNi = 8,9 г · см –3.
Вариант 9
Составьте электронные формулы атомов элементов с порядковыми номерами 11 и 22. К какому электронному семейству относится каждый из этих элементов? Составьте формулы оксидов и гидроксидов атомов элементов третьего периода, отвечающие их высшей степени окисления. Как изменяются кислотно-основные свойства этих соединений? Рассчитайте среднюю массу атомов цинка и кадмия.Вариант 10
Определите положение атома элемента в периодической системе по его электронной формуле: 2s22p5; 3s23p2; 4s23d10. Какие степени окисления может проявлять атом водорода? Ответ мотивируйте, исходя из электронного строения атома. Напишите формулы соединений, соответствующих этим степеням окисления, назовите их. Рассчитайте среднюю массу атомов натрия и цезия.Вариант 11
Составьте электронные формулы атомов элементов с порядковыми номерами 17 и 25. К какому электронному семейству относится каждый из этих элементов? Какие степени окисления может проявлять атом серы? Ответ мотивируйте, исходя из электронного строения атома. Напишите формулы соединений, соответствующие этим степеням окисления, назовите их. Рассчитайте среднюю массу и размер атома серебра.сAg=10,5 г ∙ см –3.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 |



