Таблица 3 - Отрицательные логарифмы концентрационных и термодинамических ступенчатых констант кислотной диссоциации
pKai | Димер янтарной кислоты, 298К; I=1,0 Наши данные | Иминодиянтарная кислота [110], 298К; I=0,8 | Этилендиаминодиянтар-ная кислота [110], 298К; I=1,0 |
рKa1 | 3,381 | 3,16 ± 0,20 | 3,03 ± 0,07 [110] 3,28 [111] |
рKa2 | 3,983 | 2,89 ± 0,12 | 3,88 ± 0,05 [110] 3.81 [111] |
рKa3 | 4,611 | 4,49 ± 0,10 | 6,89 ± 0,04 [110] 6,65 [111] |
рKa4 | 5,213 | 11,42 ± 0,08 | 10,03 ± 0,03 [110] 10,10 [111] |
Для обоснования существования лимонной кислоты в водных растворах в виде димеров нами был проведён анализ механизма её ионизации.
Кривая титрования раствора лимонной кислоты, полученная методом потенциометрического титрования с кулонометрической генерацией основания, представлена на рисунке 21.
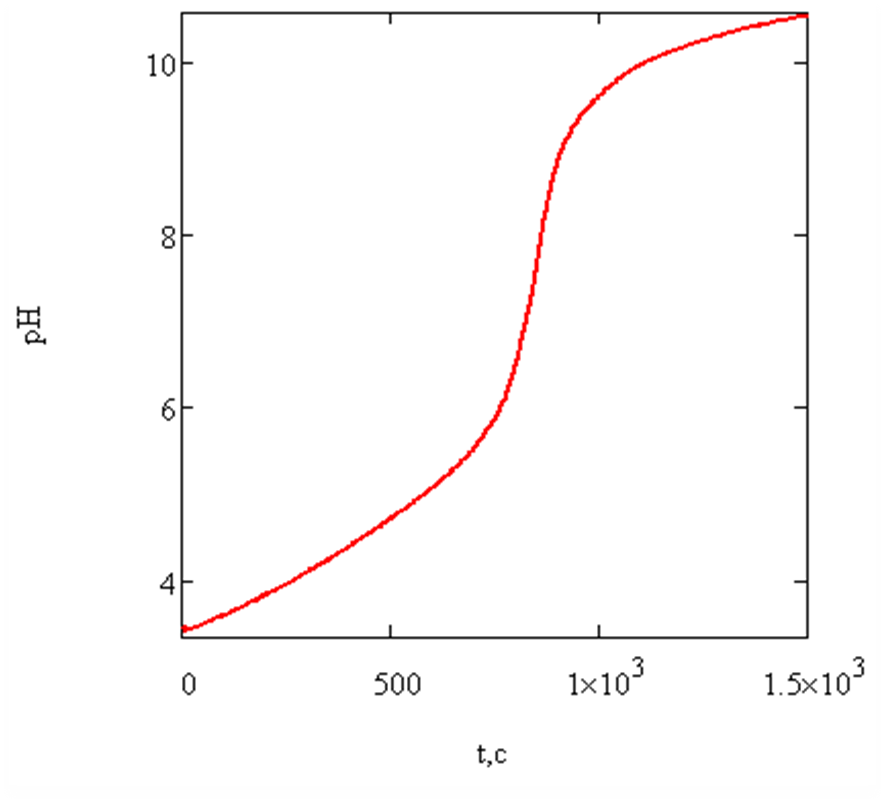
Рисунок 21 – Кривая зависимости изменения pH от времени электролиза.
Титрование 50 см3 6,025∙10–4 моль/дм3 лимонной кислоты в 1,0 моль/дм3 растворе KCl, током i =10 мА
Из кривой титрования лимонной кислоты на рисунке 21 видно, что изменение рН от времени электролиза (t, с), (t – эквивалентно добавлению щёлочи), представляет собой гладкую, монотонно возрастающую функцию, на которой не наблюдается никаких скачков. Лимонная кислота является трёхосновной и судя по литературным данным по константам диссоциации [112] должно наблюдаться хотя бы два скачка титрования, если протоны титруются последовательно. Однако их нет даже при титровании достаточно концентрированных растворов (с < 0.1 моль/дм3).
Для объяснения этого эффекта нами была предложена модель, основанная на том, что лимонная кислота в растворах находится в димерной форме. Структурная формула димера лимонной кислоты, построенная с помощью программы HyperChem, изображена на рисунке 22.
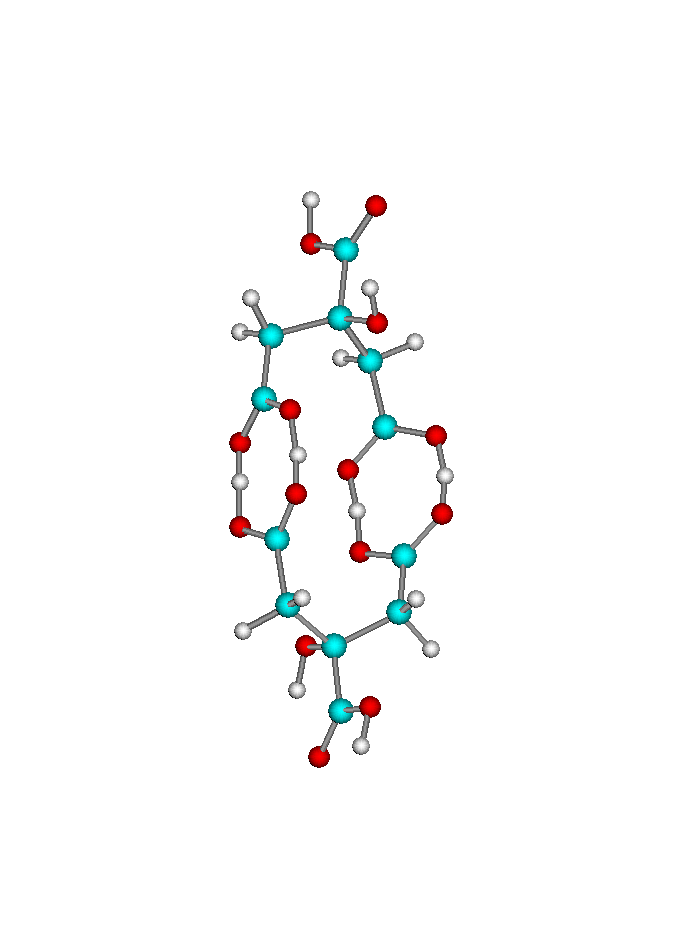
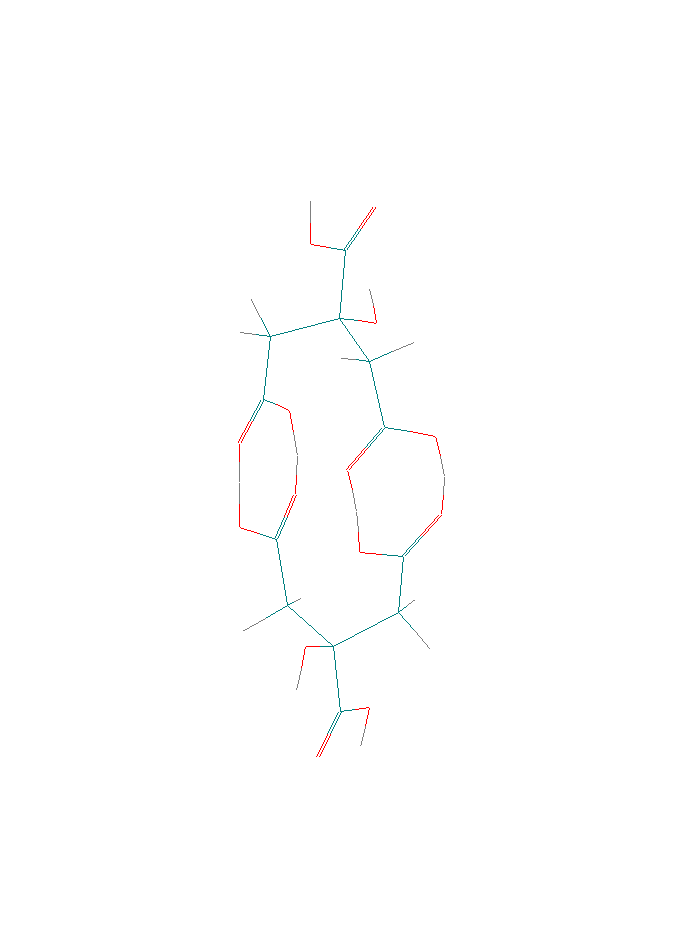
Рисунок 22 - Структурная формула димера лимонной кислоты
Эта модель может быть описана следующими уравнениями.
Материальный баланс по частицам кислоты, рассчитан по формуле (19):
c/2 = [H6A2] + [H5A2]– + [H4A2]2– + [H3A2]3– + [H2A2]4–+ [HA2]5– + [A2]6–; ( 19)
По формуле (20) рассчитаем условие электронейтральности:
[H]+ + [Na]+–Kw/[H]+ = B; ( 20)
Далее, для упрощения выводов, заряды частиц и квадратные скобки опущены.
Выражения для последовательных констант диссоциации:
Ka1 = H·H5A2/H6A2;
Ka2 = H·H4A2/H5A2;
Ka3 = H·H3A2/H4A2;
Ka4 = H·H2A2/H3A2;
Ka5 = H·HA2/H2A2;
Ka6 = H·A2/HA2.
Объединяя приведённые уравнения получим выражения (21) и (22):
A2 = c/2{H6/Ka1-6 + H5/Ka2-6 + H4/Ka3-6 +H3/Ka4-6 +H2/Ka5-6 + H/Ka6 + 1}; ( 21)
A2 = B/{H5/Ka2-6 + 2H4/Ka3-6 +3H3/Ka4-6 +4H2/Ka5-6 + 5H/Ka6 + 6}. ( 22)
Пусть Y = 2B/c, тогда совместное решение уравнений (21) и (22) приводится к виду (23):
{H5/Ka2-6 + 2H4/Ka3-6 +...+ 5H/Ka6 + 6} = Y{H6/Ka1-6 + H5/Ka2-6 + H4/Ka3-6 +
+ H3/Ka4-6 + H2/Ka5-6 +H/Ka6 + 1}; ( 23)
Анализ уравнения (23) в точках Y=1; Y=2; Y=3; Y=4; Y=5; показал, что
Ka1Ka2= H12; Ka2Ka3= H22; Ka3Ka4 = H32; ( 24)
Ka1 Ka6 = Ka2 Ka5 = Ka3Ka4= H32 = a2; ( 25)
Для сопоставления предложенной модели с экспериментом, по данным рисунке 21 была построена зависимость рН от Y, приведённая рисунке 23. На этом рисунке крестиками отмечены точки координаты, которых приведены в таблице 4. По данным значениям рН с помощью матрицы, вид которой приведён на рисунке были получены следующие величины констант (таблица 5) по двум кривым титрования.
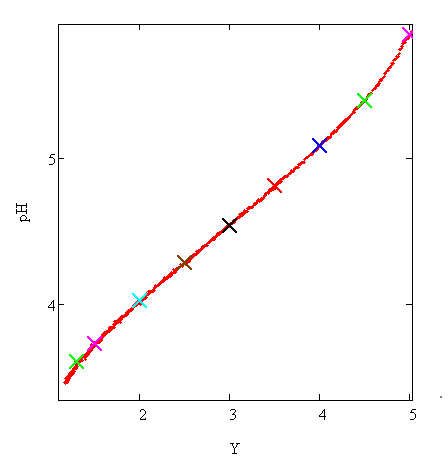
Рисунок 23 - Данные для проверки уравнения (23) и его решений (по данным рисунка 21)
Таблица 4 - Координаты точек, отмеченных на рисунке 23
Y | 1 | 1,3 | 1,5 | 2 | 2,5 | 3 | 3,5 | 4 | 4,5 | 5 |
рН | 3,2904 | 3,601 | 3,728 | 4,019 | 4,28 | 4,54 | 4,81 | 5,085 | 5,3989 | 5,8518 |
Используя данные таблицы 4 и подставляя их в уравнение (23) были получены шесть уравнений с координатами при Y=1,5; 2; 3; 3,5; 4 и 4,5. На основе этих уравнений была получена матрица, решение которой позволило найти последовательные константы ионизации димерной формы лимонной кислоты, значения которых приведены в таблице 5.
Таблица 5 - Константы ионизации лимонной кислоты
(c = 6,025∙10–4 моль/дм3; кулонометрическое определение на фоне 1,0 моль/дм3 KCl)
Константы ионизации, моль/дм3 | Прямое определение | Обратное определение* | Среднее значение | Относительная ошибка,% |
Ka1 | 1,94∙10–3 | 1,51∙10–3 | 1,72∙10–3 | 12 |
Ka2 | 1,33∙10–4 | 1,13∙10–4 | 1,23∙10–4 | 08 |
Ka3 | 6,75∙10–5 | 7,14∙10–5 | 6,94∙10–5 | 03 |
Ka4 | 1,17∙10–5 | 1,23∙10–5 | 1,20∙10–5 | 03 |
Ka5 | 7,38∙10–6 | 6,23∙10–6 | 6,81∙10–6 | 08 |
Ka6 | 5,50∙10–7 | 4,30∙10–7 | 4,90∙10–7 | 12 |
*Обратное определение проводили по формуле (25).
Для подтверждения предложенной в уравнении (23) математической модели по полученным значениям констант были рассчитаны соответствующие произведения между ними, которые сопоставлены с условиями (24) и (25) (таблица 6). По соотношению между парами текущих значений констант диссоциации рассчитаны изменения энергии Гиббса при последовательной диссоциации протонов лимонной кислоты (таблица 6).
Таблица 6 – Проверка решения уравнения (23) и условий (24) и (25)
ДG=RTln(Kai/ Ka(i+1)) | ||||||
Ka1 Ka2 | 2.121∙10–7 |
| 2.625∙10–7 | Ka1/ Ka2 | 14.011 | 6.541кДж |
Ka2 Ka3 | 8.545∙10–9 |
| 9.162∙10–9 | Ka2/ Ka3 | 1.772 | 1.418 кДж |
Ka3 Ka4 | 8.326∙10–10 |
| 8.318∙10–10 | Ka3/Ka4 | 5.791 | 4.352 кДж |
Ka4Ka5 | 8.163∙10–11 |
| 6.761∙10–11 | Ka4/Ka5 | 1.761 | 1.402 кДж |
Продолжение таблицы 6
Ka5 Ka6 | 3.338∙10–12 |
| 1.979∙10–12 | Ka5/Ka6 | 13.886 | 6.519 кДж |
Ka1 Ka6 | 8.453∙10–10 |
| 8.318∙10–10 | |||
Ka2 Ka5 | 8.378∙10–10 |
| 8.318∙10–10 | |||
Ka3 Ka4 | 8.326∙10–10 |
| 8.318∙10–10 |
Как видно из таблицы 6, экспериментальные данные хорошо описываются предложенной математической моделью, что говорит о существовании лимонной кислоты и её анионных форм в виде димеров.
Довольно небольшим изменением энергии Гиббса в системе при переходе от одной ступени диссоциации к другой, а также наличием шести констант диссоциации объясняется монотонный вид зависимости pH от t на рисунке 21.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



