Для дополнительной проверки на основании полученных констант были построены кривые распределения частиц [H6A2], [H5A2]–, [H4A2]2– , [H3A2]3–,+ [H2A2]4–,[HA2]5– , [A2]6– (рисунок 24) по уравнениям (21) и (22). Димерная форма аниона [A2]6– лимонной кислоты не распадается на мономеры, так как скорее всего образует прочную связь с водой.
На рисунке 24 сплошной линией обозначен расчёт по уравнению (22), а точками по уравнению (21), как видно, эти значения практически совпадают, что дополнительно подтверждает предположенную нами модель.
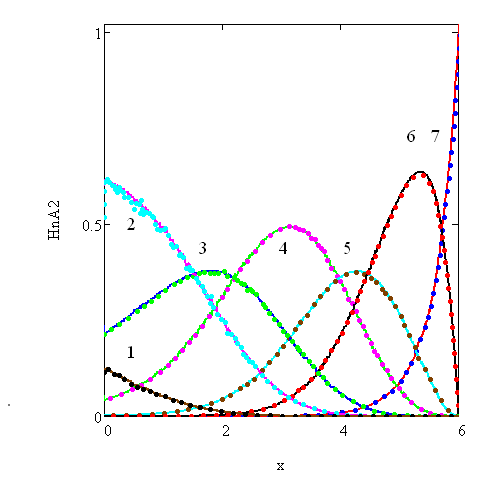
Рисунок 24 - Кривые изменения относительной концентраций димерных форм лимонной кислоты в процессе титрования.
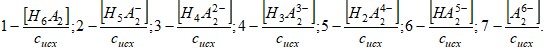
Оценку достоверности результатов полученных по этим кривым проводили по уравнению (26)
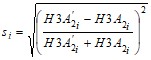 , ( 26)
, ( 26)
где ![]() - дисперсия между парой текущих значений.
- дисперсия между парой текущих значений.
Зависимость ![]() от
от ![]() (степени нейтрализации в текущий момент времени) показана на рисунке 25.
(степени нейтрализации в текущий момент времени) показана на рисунке 25.
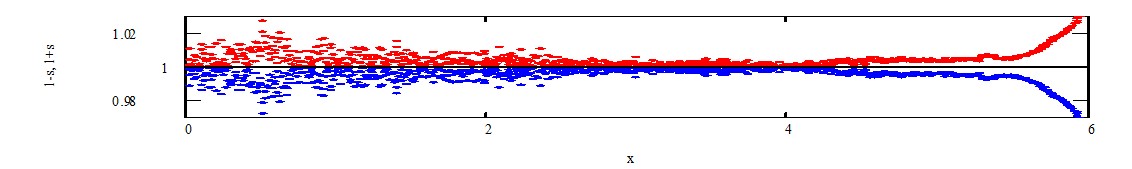
Рисунок 25 - График зависимости дисперсии от степени нейтрализации в текущий момент времени
Из рисунка 25 видно, что ошибка в расчётах по двум уравнениям не превышает 2% для любой точки на кривой титрования. Таким образом, проведённые исследования и их математическая обработка подтвердила существование лимонной кислоты (в частности, для сильноразбавленных растворов), как и ряда некоторых органических кислот [97; 102], в димерной форме, что имеет важнейшее значение при разработке методик по идентификации различных пищевых объектов.
Приведённые исследования положены в основу анализа кривых титрования, полученных в ходе определения суммы органических и минеральных кислот потенциометрическим методом с кулонометрической генерацией основания в целях идентификации подлинности вина (сока) [51; 52; 53].
3 Анализ экспериментальных данных и построение математической модели
3.1 Анализ экспериментальных данных
Для проведения анализа с достаточной точностью, необходимо, чтобы время титрования составляло 10-15 минут. При проведении эксперимента применено одновременное использование трёх ячеек, соединённых последовательно и подключённых одновременно к источнику стабилизированного тока. В каждую ячейку помещался серебряный анод и платиновый или графитовый катод. Для измерения рН во все ячейки погружали электроды (стеклянный и хлоридсеребряный). Стеклянный электрод подключали к соответствующему каналу анализатора жидкости «ЭКСПЕРТ-001», а хлорид-серебрянные, через специальный коммутатор, подсоединяли к гнезду для электрода сравнения. Анализатор "Эксперт - 001" подключали к компьютеру. В ячейки помещали 50 см3 1,0 моль/дм3 хлорида щелочного металла и аликвотную часть анализируемого раствора (1-2 см3). Чтобы показать возможность титрования растворов с небольшим содержанием кислот (например, опыты с уксусной и муравьиной кислотой) поступали следующим образом [51; 52; 53].
В ячейки для титрования помещали 50 см3 пробы и добавляли навеску сухой соли хлорида щелочного металла до его концентрации в ячейке 1 моль/дм3 и перемешивали магнитной мешалкой или воздухом, свободным от СО2, до полного растворения соли. Включали перемешивание, регистрацию рН и источник тока. Так как при использовании трёх каналов регистрации наблюдается задержка сигнала от каждого последующего сигнала, то регистрацию величин рН проводили с интервалом 3 секунды. Отсюда следует неопределенность в точности измерения количества электричества примерно равная ![]() t · 100/tK,%. Здесь
t · 100/tK,%. Здесь ![]() t - время задержки сигнала, tk - время, затраченное на титрование до точки эквивалентности, при
t - время задержки сигнала, tk - время, затраченное на титрование до точки эквивалентности, при ![]() t =3c и tk = 1000 с. Ошибка составляет меньше 0,3%. Результаты экспериментальных работ представлены на рисунках 4, 6 [50; 51; 52; 53].
t =3c и tk = 1000 с. Ошибка составляет меньше 0,3%. Результаты экспериментальных работ представлены на рисунках 4, 6 [50; 51; 52; 53].
На рисунке 4 приведены кривые титрования трёх одинаковых по объёму (50 см3 раствора кислоты + 2,9 - 3,0 г сухого NaCl) проб уксусной и трёх проб муравьиной кислот в тех же условиях в трехзвенной ячейке, основанием, генерированным током 10 мА [51; 52; 53].
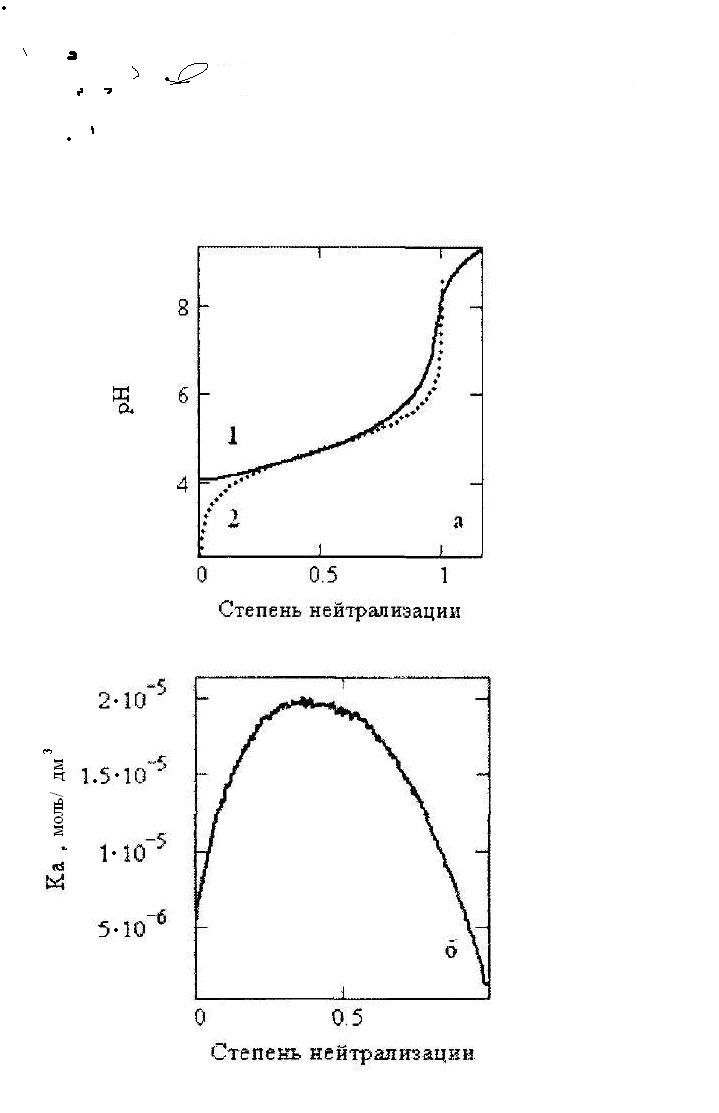
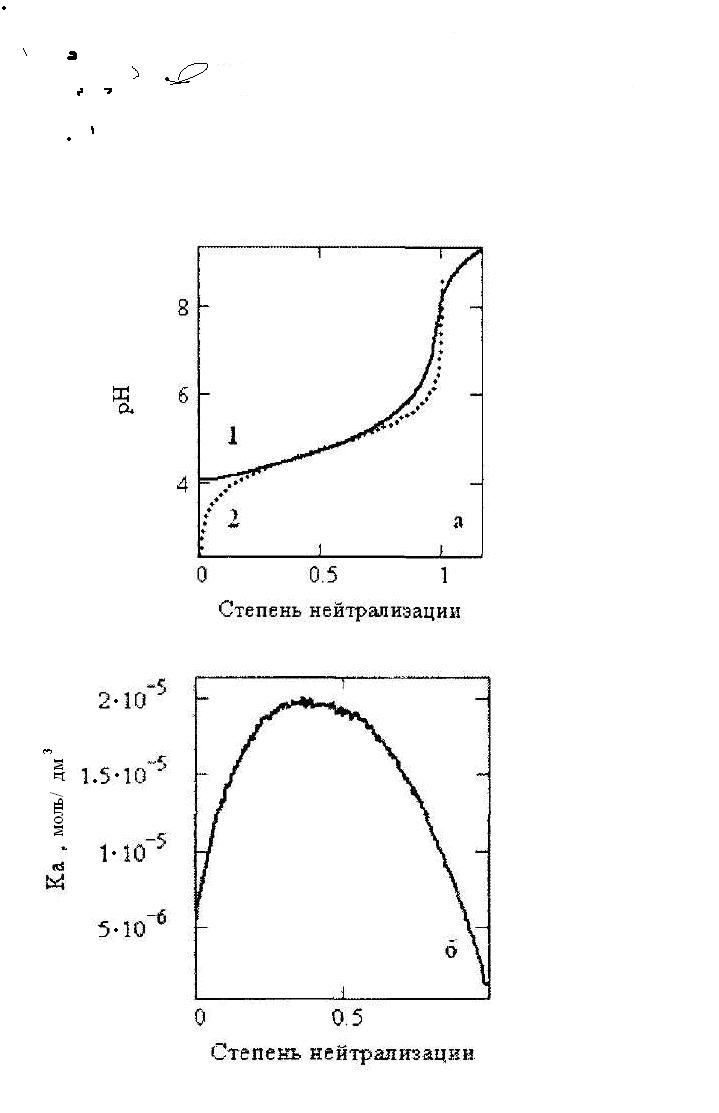
Кривые кулонометрического титрования получены для сильно разбавленных растворов. Казалось, что это даст практически сразу же возможность получить величины констант диссоциации мономерных форм изучаемых кислот. Однако это не так. Рассмотрим это на примере анализа средней кривой титрования уксусной кислоты. Справочное значение константы ионизации уксусной кислоты Ка = 1,75⋅10-5 [112]. Сравнение средних значений рН (из данных рисунка 4 а) с рассчитанными величинами рН по данному значению Ка для концентрации уксусной кислоты (Ка = 1,199 моль/дм3) с применением общепринятого уравнения (27) [115] приведено на рисунке 26а. На рисунке 26 показан расчёт константы ионизации уксусной кислоты с применением наших данных.
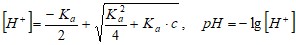 ( 27)
( 27)
|
|
Рисунок 26 − (а) сравнение экспериментальной (1) и теоретически рассчитанной кривых титрования (26), проверка уравнения (26); (б) расчёт константы ионизации (Ка) по экспериментальным данным рисунка 4(а)
Из рисунка 26 видно, что реальная и расчётная кривые титрования совпадают только в интервале степени нейтрализации (отношение добавленного основания к общей концентрации кислоты) 0,30,7. Теоретическая кривая (2) на рисунке 26а показывает, что при данной концентрации уксусная кислота должна диссоциировать в десятки раз сильнее, чем это наблюдается в реальных условиях (кривая 1 рисунка 26а). Реальная константа диссоциации (рисунок 26б) фактически не является постоянной, а проходит через максимум, приближаясь к общепринятому значению при степени нейтрализации, равной 0,5. Небольшое отличие можно объяснить тем, что титрование проходило в среде 1,0 моль/дм3 раствора NaCl. Подобные (кажущиеся) изменения величин констант ионизации для уксусной и муравьиной кислот по мере титрования были проанализированы в работах [81; 82; 83; 84; 85]. Исходя из того, что в твёрдом состоянии и в парах уксусная и муравьиная кислоты практически находятся в димерной форме авторы в работах [81; 82; 83; 84; 85] предположили, что и в водных растворах они существуют в димерной форме и, следовательно, могут диссоциировать и титроваться как двухосновные по схеме:
![]() ( 28)
( 28)
Анализируя результаты титрования и предложенную схему (28), авторы в работах [82; 83] пришли к выводу, что Ка1 = 4Ка2 и процесс титрования и диссоциации описывается следующим кинетическим уравнением
Y = [Н+]/Ка1 + 1/2; ( 29)
Здесь: Y = с/2([Н+]+ [Na+] - Kw/[H+]).
Зависимость (29) представляет уравнение прямой с наклоном, равным 1/Kat, и величиной отсекаемого на оси Y отрезка, равным 0,5.
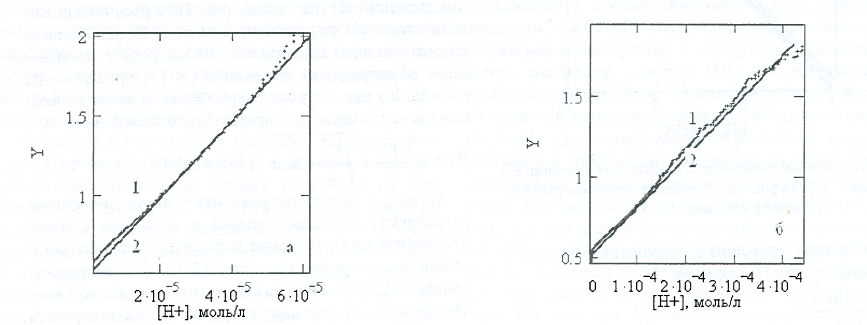
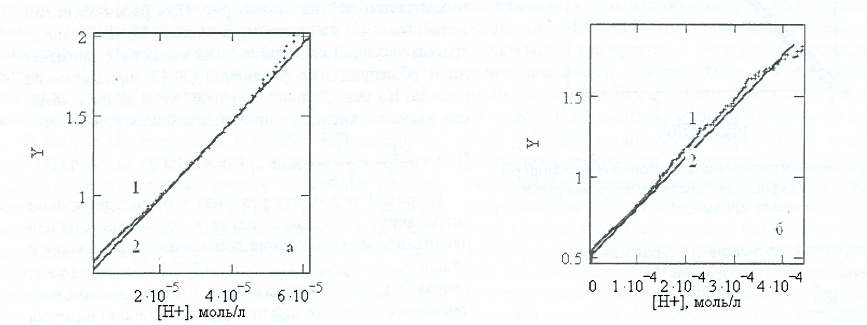
Уравнение (29) хорошо описывает и данные наших экспериментов, что видно из рисунка (27). По наклону прямых определены константы диссоциации уксусной и муравьиной кислоты. Эти значения и их сравнение с данными работ [81; 83; 84; 114] приведены в таблице 7.
|
|
Рисунок 27 - Проверка уравнения (29). Зависимости построены по усреднённым данным рисунка 4: а – уксусная кислота; б – муравьиная кислота; 1 – экспериментальные данные; 2 – данные, обработанные методом наименьших квадратов
Таблица 7 - Сравнительные данные по условиям эксперимента и найденными константами диссоциации уксусной и муравьиной кислот
Кислота | Условия опыта | Ка1, моль/дм3 | Данные | |
Концентрация, моль/дм3 | Ионная сила, NaCl, моль/дм3 | |||
Уксусная | 1,199⋅10-3 | 1,0 | (4.1-5.1) ⋅ 10-5 | из статьи |
Муравьиная | 1,713⋅10-3 | (2,4-3.2) ⋅ 10-4 | ||
Уксусная | 0,1 | 1,0 | 6,8⋅ 10-4 | из ранних работ |
Муравьиная | 0,1 | 3,2⋅ 10-4 |
Из таблицы 7 видно, что данные статьи близки к другим данным наших работ, с учётом различия в условиях опыта, хотя и несколько ниже. Последнее наблюдение возможно связано с тем, что по мере разведения степень ионизации уменьшается. Эти результаты свидетельствуют о том, карбоксильные группы связаны в кольцо связями более прочными, чем обычные водородные, и не разрушаются под влиянием растворителя с образованием цепочечных и других ассоциатов. Основным аргументом, подтверждающим то, что растворы имеют ближний порядок, является размытая дифракционная картина при отражении рентгеновского излучения, в отличие от дискретной дифракционной картины для кристаллического состояния. Проделаем мысленный опыт. Направив поток рентгеновских лучей в определённую точку раствора, получим конкретную дифракционную картину. Сдвинем источник излучения и направим его в другую точку раствора - дифракционная картина не изменится, и так далее. Следовательно, в любой точке жидкость структурирована, но в отличие от твёрдых тел эта структура способна изменяться под действием более слабых возмущений, чем возмущений, необходимых для твёрдых тел. Кроме того, жидкость восстанавливает свою исходную структуру после прекращения воздействий механических и электромагнитных сил. В твёрдых телах электронная плотность, которая рассеивает рентгеновское излучение, локализована в малых объёмах, а в жидкости она более размыта.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |