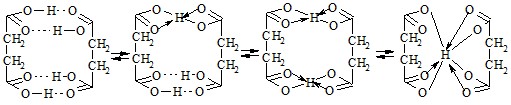
Рисунок 14 – Схема строения бициклических димеров янтарной кислоты и её анионов, образующихся при последовательном удалении протона
Для обоснования существования янтарной кислоты и её солей в водных растворах в виде бициклических димеров нами был проведён сравнительный анализ механизмов ионизации янтарной, иминодиянтарной и этилендиаминодиянтарной кислот в процессе титрования.
Приведём методику эксперимента. 20 см3 раствора, содержащего 1,000 моль/дм3 янтарной кислоты и 1 моль/дм3 азотнокислого натрия (для поддержания постоянной ионной силы раствора), титровали 1,081 моль/дм3 гидроокиси натрия. Кривая титрования приведена на рисунке 15.
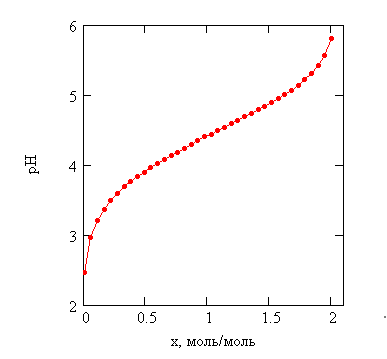
Рисунок 15 – Кривая титрования 1,000 моль/дм3 янтарной кислоты в 1 моль/дм3 азотнокислого натрия 1,081 моль/дм3 раствором гидроокиси натрия
Как видно из рисунка 15, кривая титрования непрерывна на всём интервале, носит S – образный характер, на ней отсутствуют скачки, отвечающие ступенчатой диссоциации. На рисунке 15: x – мольная доля основания, отнесённая к молю титруемой кислоты, с учётом разбавления раствора в процессе титрования.
Доказательство схемы 1 проведём, проделав следующие расчёты.
Первый расчёт. Исходная кислота находится в мономерной форме и диссоциирует по схеме (здесь и далее опущены квадратные скобки и заряды частиц, A – анион янтарной кислоты, H – ион гидроксония, в дальнейшем - протон): H2A→HA→A. Введём следующие определения: константа диссоциации по первой ступени Ka1 = H·HA/H2A; константа диссоциации по второй ступени Ka2 = A·H/HA; материальный баланс по частицам кислоты (с - общая концентрация янтарной кислоты с учётом разбавления в процессе титрования) с = H2A+HA+A = (H2/Ka1.Ka2+H/Ka2+1)A; правило электронейтральности H+Na – Kw/H = HA + 2A = A(H/Ka2+2). Совместным решением приведённых выше формул получим уравнение прямой (11):
y = Ka1.Ka2z + Ka1 ( 11)
В уравнении (11): y = H(H+Na – Kw/H)/(c–H–Na + Kw/H);
z =(2c– H–Na+Kw)/H(c–H–Na + Kw/H). Вид этой зависимости близок к прямой и приведён на рисунке 16.
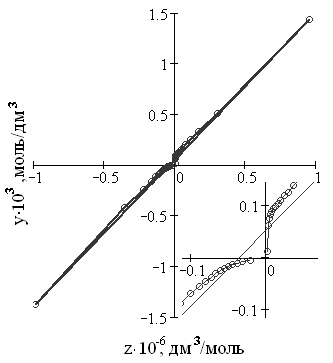
Рисунок 16 – Проверка уравнения (11)
Эта зависимость построена по данным кривой титрования, показанной на рисунке 15. По наклону зависимости (11) находим произведение Ka1.Ka2, путём экстраполяции методом наименьших квадратов к отрезку на оси y при x = 0 определяем Ka1. Таким образом, Ka1= 7,10·10–5 моль/дм3, Ka2 = 2,04·10–5 моль/дм3.
Несмотря на то, что кривая на рисунке 16 близка к прямой (коэффициент линейной регрессии R2 = 0,997), у неё есть свои особенности. Координаты первых точек (от момента начала титрования) возрастают вначале нелинейно (это хорошо видно на увеличенной области), затем увеличиваются по прямой, достигают максимума в точке полунейтрализации. После достижения максимума эти точки уходят в отрицательную область, из которой снова начинают нарастать, стремясь к координатам первой точки, но не достигают её. Следовательно, данная прямая фактически является кривой более высокого порядка, что позволило нам перейти к анализу второй схемы. Отметим, что подобная картина наблюдается и при описанной выше обработке данных по титрованию янтарной кислоты, приведённых в [100].
Второй расчёт. Исходная кислота находится в димерной форме и диссоциирует по схеме: H4A2→H3A2→H2A2→HA2→A2, которая описывается четырьмя константами равновесия: Ka1=H3А2∙H/H4A2, Ka2=H2A2∙H/H3A2, Ka3=HA23∙H+/H2A2, Ka4=L2∙H/HA2; уравнениями материального баланса по водороду: H+2∙с∙x–Kw/H=4A2+3∙HA2+2∙H2A2+H3A и кислоте:
c/2=A2+H A2+H2A2+H3A2+H4A2.
Объединением функций получим решение в виде (12):
(Y–4)∙Ka3∙Ka4/[H+]2+(Y–3)∙Ka3/[H+]+(Y–1)∙[H+]/Ka2+Y∙[H+]2/Ka1∙Ka2= 2 – Y. ( 12)
Здесь и ниже равновесные концентрации взяты в квадратные скобки, x - мольная доля основания к концентрации исходной кислоты.
В работе [100] анализом уравнения (12) было доказано и экспериментально проверено, что Ka1 = 3Ka2 и Ka3 = 3Ka4, поэтому уравнение (12) можно привести к виду (13):
(Y–4)∙Ka32/[H+]2+3(Y–3)Ka3/[H+]+3(Y–1)[H+]/Ka2+Y[H+]2/Ka22=6–3Y, ( 13)
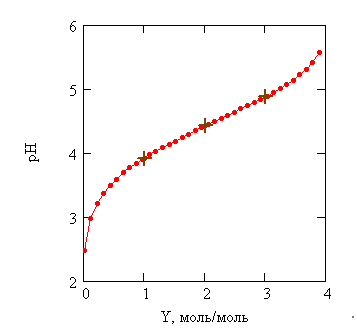
Уравнение (13) легко решить следующим образом. Строим зависимость рН от Y (рисунок 17). Находим pH и соответствующую ему концентрацию ионов водорода в трёх точках Y = 1, 2 и 3 и определяем величины Ka2=[H+]1/–[H+]22/[H+]1 и Ka4=(–1)[H+]3/3.
|
Рисунок 17 - Определение значений pH при Y = 1, 2 и 3 (+). По данным рисунка 15 |
Надёжность полученных констант определяем по расхождению текущих значений A2, которые рассчитываем по формулам (14), (15):
[A24–] = {[H+]+2∙с∙x–Kw/[H+]}/{4+9∙[H+]/Ka3+6∙[H+]2/Ka32+3[H+]3/Ka2∙Ka32}; ( 14)
[A24–] = c/{2+6[H+]/Ka3+ 6[H+]2/Ka32+ 6[H+]3/Ka2Ka32 +18[H+]4/Ka22Ka32}. ( 15)
Для янтарной кислоты получены следующие величины константы диссоциации: pKa1 == 3.381; pKa2 = 3.983; рKa3=4.611; рKa4=5.213.
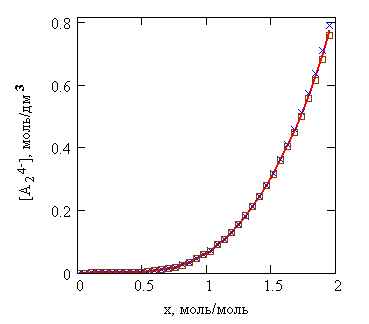
Сравнение значений [A24–], рассчитанных по уравнениям (14) и (15), приведены на рисунке 18, а на рисунке 19 дан анализ ошибок.
Изменение энергии Гиббса (ДG0) при переходе от равновесия по первой ступени к равновесию по второй RTln(Ka1/Ka2) = 2.722 кДж, от второй к третьей RTln(Ka2/Ka3) = = 3.583 кДж, от третьей к четвёртой RTln(Ka3/Ka4) = 2.722 кДж. Величины этих энергий сопоставимы с аналогичной величиной для уксусной кислоты.
|
Рисунок 18 - Сравнение значений [A24–], рассчитанных по уравнениям: (14) – х и (15)– □. Сплошная линия – среднее
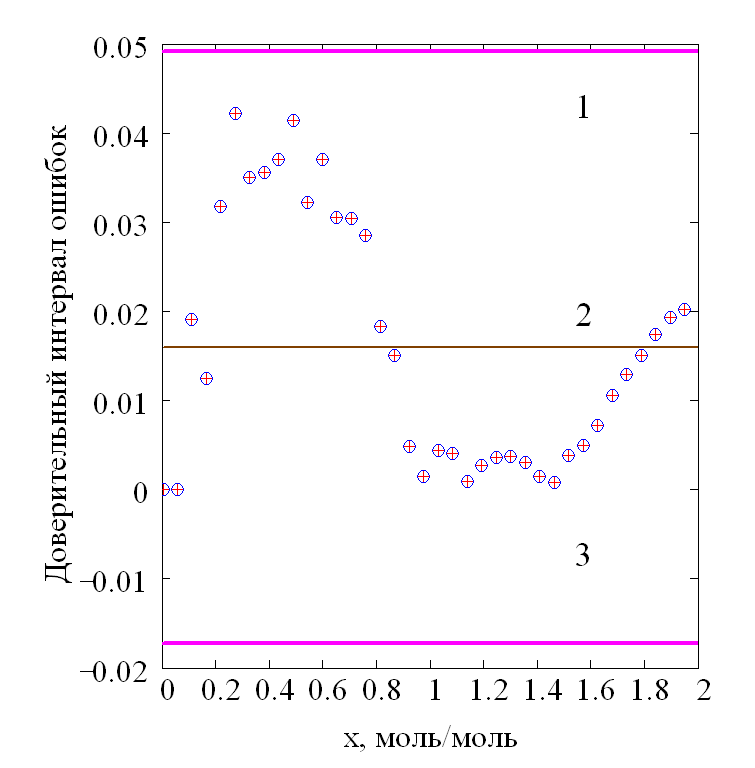
Рисунок 19 - Распределение относительных ошибок текущих значений [A24–] (х, □), и доверительный интервал: 2– среднее значение, 1– верхний предел, 3– нижний предел
Расчёт ошибок проводим по формулам (16) и (17):
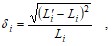 ( 16)
( 16)
![]() ( 17)
( 17)
где дi – точечная оценка погрешности;
Sx – среднее квадратическое отклонение;
n – число точек на экспериментальной кривой,
L – среднее значение из двух текущих величин [A24–], рассчитанных по уравнениям (14) и (15), L′– одно из текущих значений [A24–].
Доверительный интервал рассчитан по уравнению (18):
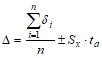 ( 18)
( 18)
где tб = 2 – критерий Стьюдента при n =36 и P = 0,95;
Д – доверительный интервал.
Анализ данных показал, что на всём изученном интервале величина ![]() не превышает 5% от текущих значений дi.
не превышает 5% от текущих значений дi.
Важным доказательством существования янтарной кислоты в циклической димерной форме является сравнение величин констант диссоциации янтарной с данными по этилендиаминодиянтарной и иминодиянтарной кислотам, взятыми из литературных источников. Рисунок 20 построен по нашим данным и по данным [110].
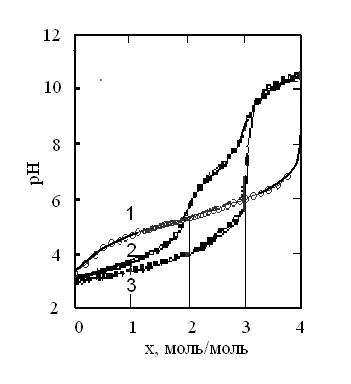
Рисунок 20 – Кривые титрования кислот: 1 – янтарной (расчёт на димерную форму); 2 – этилендиаминодиянтарной; 3 – иминодиянтарной. (ионная сила I = 1 (KNO3)) [110]
Ниже приведём анализ данных, представленных на рисунке 15 и в работе [110], косвенно подтверждающих димеризацию янтарной кислоты в водных растворах. При анализе кривых титрования димерных форм янтарной, этилендиаминодиянтарной, иминодиянтарной кислот видно, что они значительно отличаются друг от друга. Янтарная кислота титруется монотонно, вплоть до конца титрования. На интервале 0<x<2 значения pH лежат значительно выше, чем у остальных кислот, а на интервале 2<x<4 – значительно ниже. Этилендиаминодиянтарная кислота титруется в три ступени, причём на 1-й стадии расходуется два эквивалента основания, на 2-й и 3-й – по одному. Последний скачок не выражен, так как титрование происходит в сильнощелочной среде. Иминодиянтарная кислота титруется непрерывно на интервале 0<x<3, затем наблюдается скачок pH при x > 3, далее кривая переходит в щелочную область и плавно повышается. При x > 4 скачка не обнаружено, так как по нашим наблюдениям, если предшествующая ступень диссоциации лежит в сильнощелочной области, то скачок на следующей ступени отсутствует. Автор предполагает наличие циклических продуктов, блокирующих последующую ионизацию.
Такие процессы могут протекать при стоянии готовых растворов комплексонов. Пренебрежение возможностью циклизации могло явиться одной из причин несогласованности констант диссоциации, полученных разными авторами. Эти процессы также снижают координационную способность иминодиянтарной кислоты и приводят к уменьшению устойчивости образующихся комплексов. Для сравнения ступенчатые константы диссоциации димера янтарной кислоты, иминодиянтарной и этилендиаминодиянтарной кислот приведены в таблице 3.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |