В таблице 9 дано соотношение с/собщ, которое получено следующим образом. По данным рисунка 28 для кривой вина (1) построена зависимость h–х, которая представлена на рисунке 31, где h – соотношение числа молей ионов гидроксония к числу моль - эквивалентов суммы титруемых кислот в ячейке (c), а x = 2t/(t2+t1); где t – текущее время; (t2+t1)/2 – время, пошедшее на титрование до точки эквивалентности. На рисунке 31 эта часть кривой показана сплошной линией.
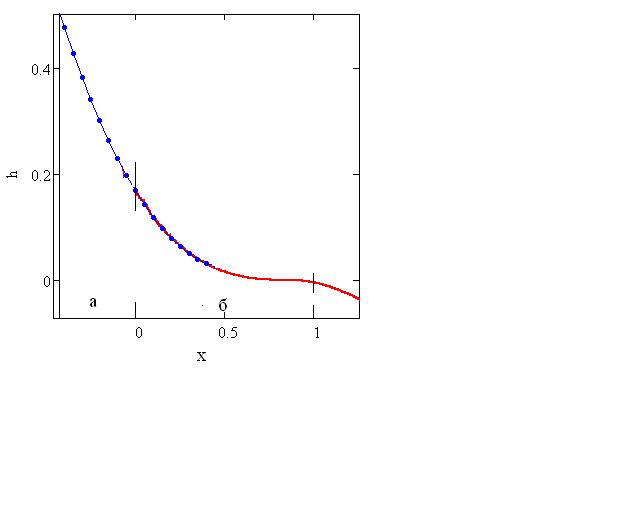
Рисунок 30 – Кривая титрования вина (1) в координатах h – x
По трём точкам (h0, h0,25, h0,5) находятся параметры a и b характеристического уравнения h(x) = h0 + a⋅x + b⋅x2, по которому экстраполируется экспериментальная кривая из рисунка 31 до значения h(x) = 0,5 (данная часть кривой показана тонкой линией с точками). Это значение принимает винная и яблочная кислоты при концентрациях, соизмеримых с содержанием титруемых кислот в вине. На оси x находим величину отрезка a, который пропорционален содержанию солевой части кислот в вине, а б пропорционален содержанию титруемой части. Тогда, с/собщ= б ⋅100 / (а+б), %.
Как видно из данных таблицы 9, соотношение с/собщ для розового и белых вин больше, чем для красного, это связано с тем, что красные вина получают брожением на мезге, из которой в процессе брожения в виноматериал переходят катионы.
Таким образом, для виноградных вин выбраны специфические критерии (таблица 9), которые можно использовать для оценки подлинности и качества вин. Пример обработки кривых титрования для получения данных о содержании суммы кислот приведён в приложении А.
3.2.3 Общее содержание катионов щелочных и щелочноземельных металлов
Содержание металлов (см) в моль-экв./дм3 определяется по формуле:
см = (собщ – с)·(V+v). (35)
В пересчёте на калий:
m(K) = см· MK, (36)
где MK– молярная масса калия, г/моль.
По данным титрования определяют следующие критерии: mобщ, m, h0, Дt = t2–t1, mо, ДpH. Если все эти критерии вместе не выходят за значения рекомендуемых диапазонов, приведённых в таблице 11, можно говорить о подлинности и высоком качестве вина.
Таблица 11 - Характерные критерии для высококачественных вин
вино | c, моль/дм3 | Титруемая кислотность, г/кг | Летучая кислотность, г/кг | Дt, c | pH0 | pH1 | pH2 | h0 | щ, % |
Красное | 1.1+ 0.1 | 4.6+0.5 | 0.8+0.2 | 212+50 | 3.8+0.2 | 5.2+0.3 0 | 9.0+0.1 | 0.17+0.05 | 70+10 |
Белое вино | 1.5+0.3 | 7.0+2 | 0.9+0.2 | 170+10 | 3.4+0.05 | 5.00+0.05 | 9.40+0.05 | 0.28+0.05 | 80+5 |
Таблица 11 получена анализом 20 образцов красных вин и 12 белых, получивших высокую дегустационную оценку.
3.2.4 Определение суммы аминокислот
Оценка суммарного содержания аминокислот в винах по виду кривых потенциометрического титрования проведена на основании того, что в отличие от кривой титрования винной кислоты (рисунок 31, кривая 10) кривые титрования вин, приведённые на рисунке 31 (кривые 1-9) после достижения точки эквивалентности выходят на плато при более низких значениях pH.

Рисунок 31 - Сравнение кривых титрования сухих вин (1-9):
1 − Анапский ранний; 2 − Алиготе; 3 − Каберне-Совиньон; 4 − Красностоп АЗОС; 5 − Достойный; 6 − Сацимлер; 7 − Литдар; 8 − Каберне АЗОС; 9 − Гранатовый и 10 − винной кислоты (представлено по данным работы [117])
Отдельными опытами было показано, что добавление соизмеримых количеств глицина, валина, аланина, пролина к раствору минеральной или винной кислот не мешает точному титрованию последних. Однако кривые титрования чистой винной кислоты и с добавками аминокислот несколько отличаются – начальное значение pH повышается с увеличением добавленного количества аминокислоты, а интервал скачка титрования уменьшается. После прохождения первого скачка титрования, pH медленно нарастает, но в выбранных нами условиях (малый ток генерации основания) не наблюдается второго скачка, который можно было бы связать с титрованием аминокислоты. После скачка титрования (рисунок 31, кривые 1–9) на кривых титрования вин наблюдается плавный подъём рН. Этот подъём начинается при более низких значениях pH, чем на кривой титрования чистой винной кислоты (рисунок 31, кривые 1).
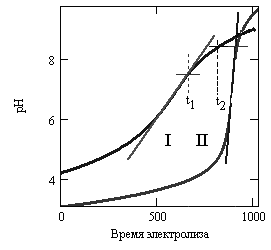
Для количественной оценки содержания суммы аминокислот поступали следующим образом. Проводили касательную к точке перегиба на кривой титрования вина. По верхней точке, в которой начиналось отклонение кривой титрования вправо от проведённой касательной, находили время t1 (время начала титрования аминокислот). Через найденную подобным образом точку на кривой титрования винной кислоты проводили горизонтальную линию, до пересечения с верхней частью кривой титрования виноматериала. Эту точку принимали за время t2, которое мы связали с окончанием титрования суммы аминокислот. Схема определения времени начала и конца титрования аминокислот показана на рисунке 32.
Расчёт содержания аминокислот в вине проводили по следующей формуле
![]() (37)
(37)
где ∑с – суммарная концентрация аминокислот;
i – ток электролиза, мА;
t1 – время начала титрования аминокислот, с;
t2 – время окончания титрования аминокислот, с;
F – число Фарадея, 96 500 Кл;
v – объём пробы вина, взятой для титрования, см3.
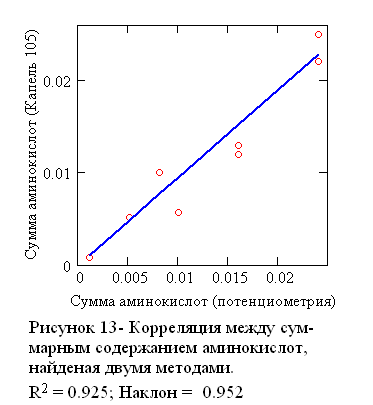
Качественный состав и суммарное содержание аминокислот в анализируемых виноматериалов, найденных методом электрофоретического разделения на анализаторе «Капель - 105», приведены в таблице 12. В последней строке таблицы 12 приведены суммарные концентрации аминокислот, найденные предложенным нами методом. Как видно из этой таблицы только один результат выпадает из корреляции (сорт Гранатовый). Если принять его за выброс, между остальными значениями наблюдается хорошая сходимость.
Рисунок 32 – Схема нахождения величин t1 и t2. I – Красностоп АЗОС; II – винная кислота |
Рисунок 33 – Корреляция между суммарным содержанием аминокислот, найденная двумя методами. R2 = 0,925 |
Таблица 12 – Аминокислотный состав изученных вин
Аминокислота, 104 моль/дм3 | Сорт винограда | ||||||||
Алиготе | Анапский ранний | Каберне-Совиньон | Красностоп АЗОС | Достойный | Сацимлер | Литдар | Каберне АЗОС | Гранатовый | |
Аргинин | 5,20 | 0,00 | 1,86 | 2,42 | 2,04 | 2,98 | 2,20 | 2,89 | 3,48 |
тирозин | 0,00 | 0,00 | 0,00 | 0,77 | 0,00 | 2,29 | 0,00 | 0,00 | 0,00 |
в–фенил–аланин | 0,22 | 0,52 | 0,27 | 0,61 | 0,17 | 0,58 | 0,24 | 0,18 | 0,30 |
гистидин | 1,00 | 0,00 | 0,57 | 1,43 | 0,35 | 1,06 | 0,62 | 1,62 | 2,38 |
лизин | 0,00 | 0,00 | 0,00 | 0,36 | 0,00 | 0,00 | 0,12 | 0,00 | 0,00 |
лейцин | 0,33 | 0,00 | 0,15 | 0,66 | 0,36 | 0,26 | 0,12 | 0,27 | 2,12 |
метионин | 1,98 | 0,00 | 1,64 | 2,53 | 4,58 | 3,74 | 1,62 | 5,98 | 5,59 |
валин | 2,34 | 0,00 | 0,56 | 0,23 | 0,31 | 3,30 | 0,19 | 0,31 | 0,13 |
пролин | 38,50 | 5,38 | 91,60 | 110,0 | 110,0 | 220,0 | 48,10 | 190,0 | 470,0 |
треонин | 4,02 | 0,19 | 6,80 | 6,58 | 8,57 | 14,1 | 4,75 | 12,3 | 16,9 |
триптофан | 0,54 | 0,16 | 0,60 | 0,86 | 0,71 | 0,81 | 0,260 | 0,63 | 0,74 |
серин | 0,89 | 0,00 | 0,95 | 1,66 | 1,13 | 1,25 | 0,32 | 1,38 | 1,14 |
б-аланин | 0,86 | 1,00 | 0,60 | 1,01 | 0,83 | 0,83 | 0,15 | 0,82 | 1,07 |
глицин | 0,00 | 0,44 | 0,39 | 0,71 | 0,51 | 0,00 | 0,41 | 0,53 | 0,00 |
сумма | 50,6 | 7,69 | 100 | 130 | 120 | 250 | 56,8 | 220 | 520 |
сумма(найдено) | 51,0 | 11,0 | 81,0 | 160 | 160 | 240 | 100 | 240 | 240 |
Пролин/сумма | 0.76 | 0.70 | 0.92 | 0.85 | 0.92 | 0.88 | 0.85 | 86 | 0.90 |
В заключение отметим, что расчётные методы оценки регистрируемых потенциометрических кривых титрования с кулонометрической генерацией основания позволяют оперативно и объективно определить массовую концентрацию титруемых кислот в виноматериалах и косвенно оценить суммарное содержание катионов щелочных и щелочноземельных металлов и аминокислот. Методы не требуют стандартизации растворов и по виду кривых кулонометрического титрования можно идентифицировать сорт виноматериала.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |