В целях совершенствования метода по определение суммы минеральных и органических кислот, предложенного в работе [66], нами был проведён анализ природы водородных и межмолекулярных связей димеров уксусной кислоты в водных растворах.
Установлено, что в процессе титрования при переходе кислоты в её среднюю соль происходит образование димера, что приводит к стабилизации протона и затрудняет его последующую диссоциацию [81].
Теории водородной связи и возможности её образования в растворах карбоновых кислот посвящено немало работ. Кристаллические структуры и состояние карбоновых кислот в газовой фазе довольно хорошо изучено [73; 76; 77; 116], построены кривые распределения молекулярных и ионных форм при титровании, рассмотрены причины устойчивости димеров уксусной кислоты в водных растворах, приведены доказательства существования димерной формы уксусной кислоты в жидкой фазе, а также было доказано, что одноосновные органические кислоты, а также и их соли, существуют в водных растворах в виде димеров и последовательно титруются по двум степеням как двухосновные, приведено математическое описание данной модели, проведён её анализ [80]. Следует отметить, что авторы работы [102] на основании данных ИК – спектроскопии по исследованию растворов уксусной, щавелевой и лимонной кислот проишли к выводу, что эти кислоты, даже в сильноразбавленных растворах, находятся в виде димеров., ИК - спектры кислот, полученные авторами в работе [102] приведены на рисунках 7-9.
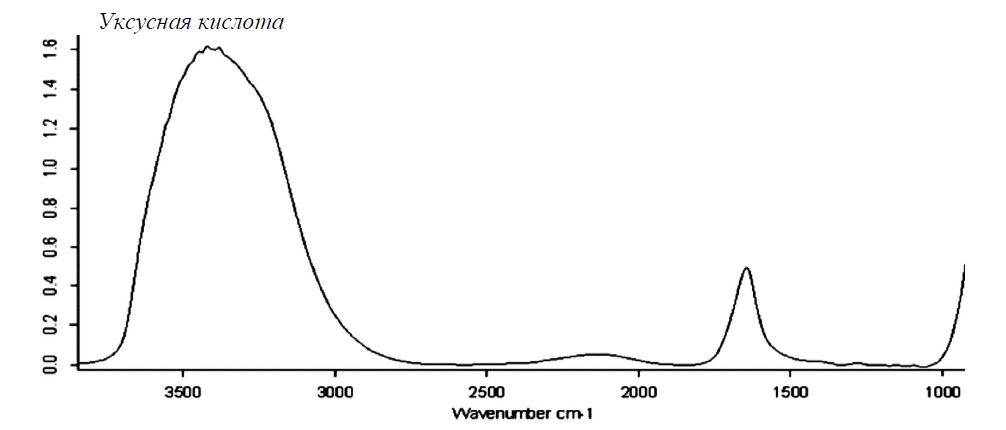
Рисунок 7 - ИК-спектр уксусной кислоты [102]
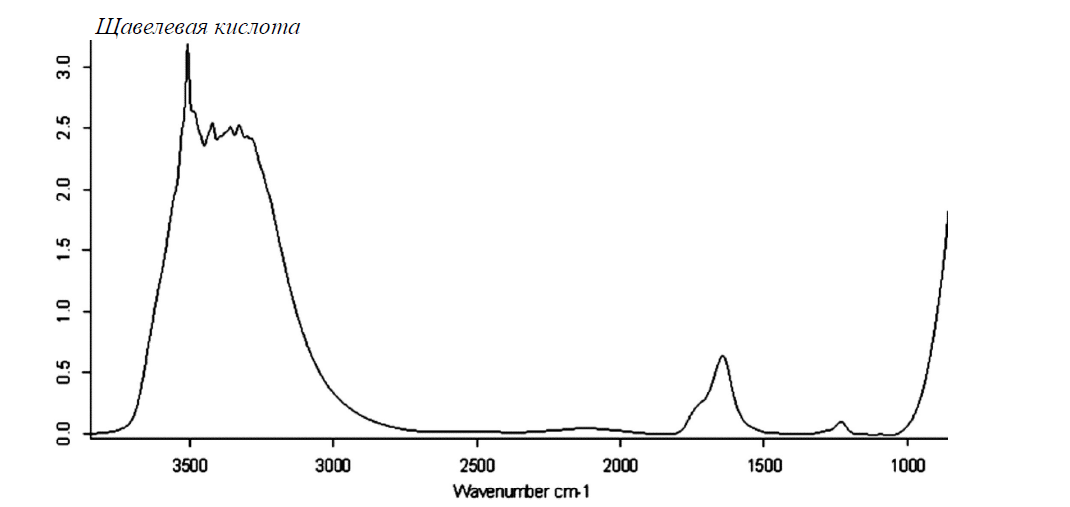
Рисунок 8 - ИК-спектр щавелевой кислоты [102]
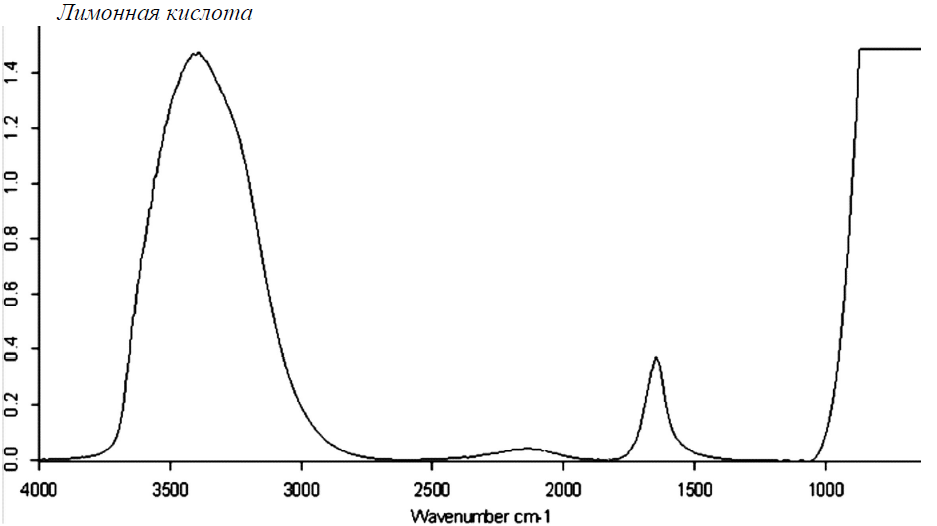
Рисунок 9 - ИК-спектр лимонной кислоты кислоты [102]
На основе полученных в работе [102] ИК-спектрах авторы предположили, что в водных растворах уксусная, щавелевая и лимонная кислота образует циклические димеры, так как в ИК-спектрах водных растворов этих кислот не было идентифицировано характеристических полос поглощения валентных колебаний свободных гидрокси - и карбонильных групп, которые участвуют в водородном связывании между собой [102]. Наличие небольшого пика в области 3500 см–1 на ИК-спектре водного раствора щавелевой кислоты, очевидно связано с наличием свободных гидрокси - и карбонильных групп, что свидетельствует о линейной структуре димера щавелевой кислоты.
Далее нами на основании литературных данных и анализа кривых титрования [81; 82; 83; 84; 85; 86; 87; 88; 89; 102] было принято, что ![]() и
и ![]() , а также и их соли существуют в водных растворах в виде димеров и последовательно титруются по двум степеням как двухосновные. Математически данная модель описывается следующим образом.
, а также и их соли существуют в водных растворах в виде димеров и последовательно титруются по двум степеням как двухосновные. Математически данная модель описывается следующим образом.
Схема последовательной ионизации димерных форм кислоты:
![]() .
.
![]() – материальный баланс по частицам кислоты;
– материальный баланс по частицам кислоты;
![]() – правило электронейтральности;
– правило электронейтральности;
![]() – выражение для первой константы диссоциации;
– выражение для первой константы диссоциации;
![]() – выражение для второй константы диссоциации.
– выражение для второй константы диссоциации.
Пусть ![]() тогда
тогда
![]() ,
,
![]() .
.
Посредством замены ![]() и решения приведённых выше уравнений получено в [81] окончательное уравнение второго порядка:
и решения приведённых выше уравнений получено в [81] окончательное уравнение второго порядка:
![]() ( 4)
( 4)
На основании того, что функция ![]() линейно зависела от концентрации ионов водорода, в работе [81] было доказано, что уравнение (4) распадается на пару прямых, если
линейно зависела от концентрации ионов водорода, в работе [81] было доказано, что уравнение (4) распадается на пару прямых, если ![]() Действительно, замена
Действительно, замена ![]() на
на ![]() , преобразует уравнение (4) к виду (5), а после его упрощения – к виду (6):
, преобразует уравнение (4) к виду (5), а после его упрощения – к виду (6):
![]() , ( 5)
, ( 5)
![]() . ( 6)
. ( 6)
Следует отметить, что при ![]() поэтому
поэтому ![]() . Здесь
. Здесь ![]() – константа ионизации, вычисляемая по классической теории, для монокарбоновой кислоты. Формально уравнение (6) описывает процесс нейтрализации слабой кислоты с помощью одной константы, но ионизация до точки полунейтрализации протекает значительно сильнее, чем после её прохождения (
– константа ионизации, вычисляемая по классической теории, для монокарбоновой кислоты. Формально уравнение (6) описывает процесс нейтрализации слабой кислоты с помощью одной константы, но ионизация до точки полунейтрализации протекает значительно сильнее, чем после её прохождения (![]() :
:![]() =1:4). В исходном димере слабой кислоты оба карбоксильных протона связаны в кольцо посредством водородных связей. В этом кольце каждый из протонов связан валентной связью с однозарядным атомом кислорода и водородной связью с другим атомом кислорода. При оттитровывании первого протона оставшийся протон связан более прочной связью, так как находится между двумя отрицательно заряженными атомами кислорода, а эта связь значительно прочнее, чем предыдущая (теория и эксперимент показывает, что в 4 раза). Этот процесс можно изобразить схемой, показанной на рисунке 10.
=1:4). В исходном димере слабой кислоты оба карбоксильных протона связаны в кольцо посредством водородных связей. В этом кольце каждый из протонов связан валентной связью с однозарядным атомом кислорода и водородной связью с другим атомом кислорода. При оттитровывании первого протона оставшийся протон связан более прочной связью, так как находится между двумя отрицательно заряженными атомами кислорода, а эта связь значительно прочнее, чем предыдущая (теория и эксперимент показывает, что в 4 раза). Этот процесс можно изобразить схемой, показанной на рисунке 10.
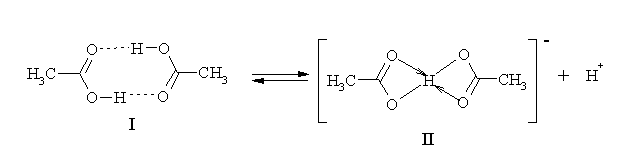
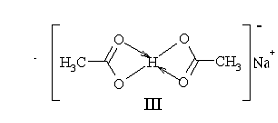
Рисунок 10 - Схема диссоциации димера уксусной кислоты
Аниону (II) соответствует кислая соль (III), образующаяся при смешивании в эквимолярном соотношении ледяной уксусной кислоты и безводного ацетата натрия.
Данная форма (III), так называемая, кислая соль ![]() (Villiers) [92] образуется с выделением тепла и представляет собой кристаллическое вещество. При нагревании она плавится и только выше 200 °С разлагается, выделяя уксусную кислоту и оставляя среднюю соль. Авторы [83] считают, что при растворении в воде она полностью разлагается на свои компоненты. Однако этому противоречит то обстоятельство, что при электролизе средней соли, как показал Кольбе [92], происходит образование этана, угольной кислоты и водорода:
(Villiers) [92] образуется с выделением тепла и представляет собой кристаллическое вещество. При нагревании она плавится и только выше 200 °С разлагается, выделяя уксусную кислоту и оставляя среднюю соль. Авторы [83] считают, что при растворении в воде она полностью разлагается на свои компоненты. Однако этому противоречит то обстоятельство, что при электролизе средней соли, как показал Кольбе [92], происходит образование этана, угольной кислоты и водорода:
H2O + C2H6⋅C2O3 = Н2 + [2CO2 + C2H6].
Реакция записана на основе рассуждений Кольбе. По современным представлениям электролиз протекает следующим образом:
(CH3COO)2Na2 – 2e– = C2H6 + 2CO2 + 2Na+– реакция на аноде;
2H2О + 2e– = H2 + 2OH– – реакция на катоде;
(CH3COO)2Na2 + 2H2О = C2H6 + 2CO2 + H2 +2NaOH – суммарный процесс.
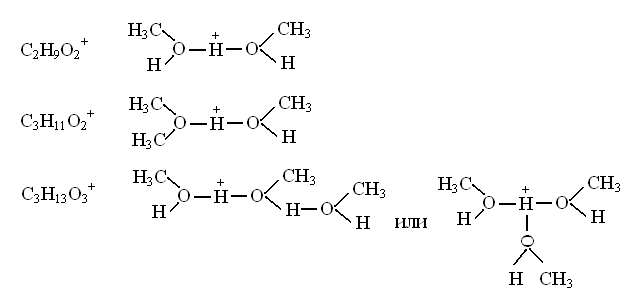
Стуктуры II и Ш обнаружены методом ионного циклотронного резонанса (ИСР) [э90] для ряда органических молекул. Как сказано в данной работе, образование иона Н+ приводит к появлению ионов с массой М+ и появлению ионов с массой (2М+1)+, в которых две молекулы сольватируют протон, находящийся между ними. Между МН+ и М образуется сильная (25–40 ккал/моль) водородная связь. Например, в ИЦР-спектре метанола при высоком давлении и большом времени нахождения в ячейке в метаноле обнаружены следующие структуры [91э]:
Важным доказательством существования димерной формы уксусной кислоты в жидкой фазе является то обстоятельство, что в твёрдом состоянии и в парах на линии кипения она димеризована и только при температуре выше 250 оС переходит полностью в мономерную форму [93]. Меняя температуру пара, авторы [94] определили геометрические параметры мономеров и димеров ряда карбоновых кислот (таблица 2).
Как следует из данных таблицы 2 образование водородных связей в димерах карбоновых кислот сопровождается изменением расстояний углерод – кислород. В мономерах r (С = О) близки к длинам соответствующих связей в альдегидах и кетонах и могут рассматриваться как обычные двойные связи: С =О. Длина связи С–О короче, чем в алифатических спиртах и эфирах примерно на 0,06, и подобна расстоянию r (О–СН2) в метилвиниловом эфире, где предполагается взаимодействие атома кислорода с двойной связью [93].
Таблица 2 – Геометрические параметры молекул мономеров и димеров карбоновых кислот [94]
Параметр (ra)·1010, м | Муравьиная кислота | Уксусная кислота | Пропионовая кислота | |||
HCOOH | (НСООН)2 | СНзСООН | (СН3СООН)2 | С2Н6СООН | (С2Н5СООН)2 | |
C=O | 1,217(3) | 1,220(3) | 1,214(3) | 1,231(3) | 1,211(3) | 1,232(6) |
C–O | 1,361(3) | 1,323(3) | 1,364(3) | 1,334(4) | 1,367(4) | 1,329(8) |
O–H | 0,984(24) | 1,036(17) | — | — | — | — |
Н2С–С | — | — | 1,520(5) | 1,506(5) | 1,518(10) | 1,518(10) |
Н3С–С | — | — | — | — | 1,543(10) | 1,547(15) |
О---Н – О | –– | 2,703(7) | — | 2,68(1) | — | 2,71(1) |
∠OC=O | 123,4(0,5) | 126,2(0,5) | 122,8(0,5) | 123,4(0,5) | 122,1(0,8) | 123,7(1,7) |
∠CCO | –– | –– | 110,6(0,6) | 113,0(0,8) | 111,2(0,8) | 113,4(1,6) |
В димерах значения длины связей углерод-кислород отличаются от таковых, найденных в мономерах: r (С=О) немного длинее (кроме НСООН, где изменения не выходят за пределы ошибок эксперимента), а r (С–О) значительно короче, чем в мономерах. Изменения длин связей С–О и С=О в димерах происходят за счет образования водородной связи. Влияние этого фактора на связь С=О существенно меньше, чем на С–О, что может быть связано с большей силовой постоянной двойной связи [93].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



