Из других различий в структурных параметрах мономеров и димеров можно отметить удлинение r (О–Н) и увеличение – ОС=О в (НСООН)2 по сравнению с НСОOН. Правда, большая ошибка в определении эффекта удлинения r (О–Н) снижает значимость этого эффекта. Из этих данных следует, что молекулы димерных форм занимают меньший объём, чем сумма двух мономерных молекул. Возможно, что в жидкой фазе и в растворах происходит дополнительное сжатие молекул и изменение их конфигурации. Следует отметить, что протоны карбоксильных групп карбоновых кислот интенсивно взаимодействуют с протонами воды, очевидно обмениваясь избыточной энергией. В работе [81] приведены зависимости относительного химического сдвига (![]() , м. д.) сигнала от протонов карбоксильных групп муравьиной и уксусной кислот и их смеси. Зависимость
, м. д.) сигнала от протонов карбоксильных групп муравьиной и уксусной кислот и их смеси. Зависимость ![]() от мольной доли кислоты или смеси кислот постоянного состава имеет вид плавных кривых. Химический сдвиг сигнала от протонов карбоксильной группы в сторону слабого поля уменьшается с увеличением концентрации воды и совпадает с сигналом от протонов воды, т. е. в растворе нет раздельных сигналов от протонов чистой воды и протонов карбоксильной группы кислоты. Последнее говорит о том, что протоны воды и карбоксильных групп образуют сложные пространственные структуры на основе водородных связей. Причём строение водородных связей очевидно близко по структуре, чего нельзя сказать о спиртах. В спиртовом растворе сигналы от протонов воды и гидроксильной группы этанола фиксированы и наблюдаются раздельно. Увеличение концентрации влияет только на величину сигнала. Кроме того, положение сигнала от спиртовой –OH группы зависит от природы спирта. Так, в метаноле сигнал от этой группы совпадает с сигналом (накладывается) от протонов воды и менее смещён в сторону слабого поля.
от мольной доли кислоты или смеси кислот постоянного состава имеет вид плавных кривых. Химический сдвиг сигнала от протонов карбоксильной группы в сторону слабого поля уменьшается с увеличением концентрации воды и совпадает с сигналом от протонов воды, т. е. в растворе нет раздельных сигналов от протонов чистой воды и протонов карбоксильной группы кислоты. Последнее говорит о том, что протоны воды и карбоксильных групп образуют сложные пространственные структуры на основе водородных связей. Причём строение водородных связей очевидно близко по структуре, чего нельзя сказать о спиртах. В спиртовом растворе сигналы от протонов воды и гидроксильной группы этанола фиксированы и наблюдаются раздельно. Увеличение концентрации влияет только на величину сигнала. Кроме того, положение сигнала от спиртовой –OH группы зависит от природы спирта. Так, в метаноле сигнал от этой группы совпадает с сигналом (накладывается) от протонов воды и менее смещён в сторону слабого поля.
Решив уравнение (6) относительно [H+], получим (7):
![]() . ( 7)
. ( 7)
С физической точки зрения уравнение (7) имеет смысл при условии, что Y > 0,5. Но выражение (7) получено из решения квадратической функции (4), следовательно, вторым корнем уравнения (4) будет следующее значение (8):
![]() ( 8)
( 8)
Его значение тоже положительно, поэтому для вычисления текущих значений [H+] можно использовать приведенное ниже уравнение (9):
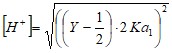 . ( 9)
. ( 9)
При такой записи концентрация [H+] положительна на всем интервале изменения значений ![]() . Из уравнения (9) видно, что концентрация ионов водорода в любой точке кривой титрования описывается одной константой
. Из уравнения (9) видно, что концентрация ионов водорода в любой точке кривой титрования описывается одной константой ![]() . Заменим её на величину классической константы
. Заменим её на величину классической константы ![]() , численно равной концентрации ионов водорода в точке полунейтрализации кислоты. Учитывая, что
, численно равной концентрации ионов водорода в точке полунейтрализации кислоты. Учитывая, что ![]() , получим следующее выражение:
, получим следующее выражение:
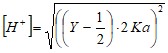 ( 10)
( 10)
Покажем, как с помощью уравнения (10) можно построить кривые распределения различных частиц анализируемой кислоты от степени нейтрализации – x. Здесь х - отношение суммы эквивалентов добавленного основания и определяемого количества ионов водорода к концентрации, взятой для титрования димера кислоты; с=сHA - концентрация мономера.
x =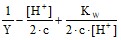 ; – определение степени нейтрализации димерной формы кислоты;
; – определение степени нейтрализации димерной формы кислоты;
[H2A2] =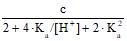 ; – концентрация нейтрально-заряженного димера;
; – концентрация нейтрально-заряженного димера;
[HA2–] = 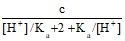 ; – концентрация одно-зарядного димера;
; – концентрация одно-зарядного димера;
[A22–] = 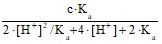 ; – концентрация двух-зарядного димера.
; – концентрация двух-зарядного димера.
Зависимость распределения молекулярных и ионных форм димеров уксусной кислоты от степени ионизации представлена на рисунке 11, на котором условию x < 0 отвечает наличие сильной минеральной кислоты, следует отметить, что она полностью подавляет диссоциацию уксусной кислоты при условии, что на каждый моль карбонильного кислорода приходится моль протонов сильной кислоты. Это объясняет проявление слабых щелочных свойств уксусной кислоты по отношению к минеральным кислотам в безводных растворах. Анализ зависимости распределения различных частиц, показанной на рисунке 12, от исходной концентрации уксусной кислоты выглядит следующим образом: при с ~ 1·10–5 моль/дм3 доминирует частица [HA2–], а концентрации частиц [H2A2] и [A22–] примерно равны. Увеличение концентрации уксусной кислоты приводит к росту концентрации нейтральной формы и снижению моно - и билигандных форм. При уменьшении концентрации уксусной кислоты ниже 1·10–5 моль/дм3 происходит увеличение степени диссоциации. Однако даже при концентрации 1·10–7 моль/дм3 полной диссоциации не происходит, что видно из рисунка 12. Дальнейшее уменьшение концентрации не имеет смысла, так как концентрация уксусной кислоты становится меньше концентрации ионов гидроксония, образующихся за счёт диссоциации молекул воды. Данное наблюдение позволяет сделать вывод о том, что димеры уксусной кислоты не распадаются на молекулы, что существование мономеров привело бы к значительно большей степени диссоциации. Данные расчеты согласуются как с нашими результатами, так и с данными по электропроводности, приведенными на рисунке 13.
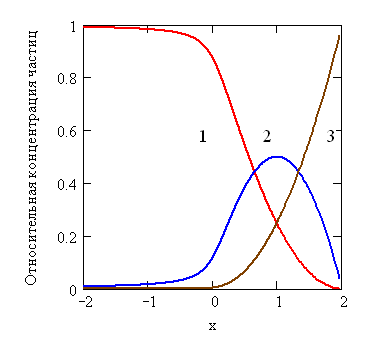
Рисунок 11 - Зависимость распределения молекулярных и ионных форм димеров уксусной кислоты от степени ионизации (расчёт сделан для уксусной кислоты с концентрацией на мономер 0,001моль/дм3; Ка = 1,75·10-5 моль/дм3). 1– [H2A2]; 2– [HA2–]; 3 – [A22–]
Здесь х - отношение суммы эквивалентов добавленного основания и определяемого количества ионов водорода к концентрации взятого для титрования димера кислоты; с = c(HA) – концентрация мономера.
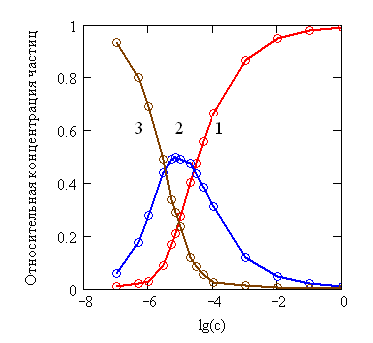
Рисунок 12 – Распределение частиц: 1– [H2A2], 2– [HA2–], 3 – [A22–] с ростом концентрации уксусной кислоты (расчёт сделан для чистой уксусной кислоты с разной концентрацией на мономер; Ka = 1,75·10–5 моль/дм3)
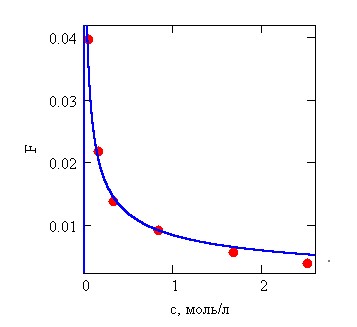
Рисунок 13 – Зависимость концентрации ионов водорода от концентрации уксусной кислоты. Сплошная кривая – расчёт по уравнению (10), точки – справочные данные по электропроводности
Полученные данные могут быть использованы для изучения механизмов возможностей кулонометрического титрования для определения общего количества органических и минеральных кислот в продуктах (в т. ч. винах и виноматериалах), а также они имеют важнейшее значение для изучения природы процессов проходящих при титровании органических кислот, что в свою очередь может быть использовано для разработки и совершенствования методов для оценки качества и идентификации сырья и продукции винодельческой и другой промышленности.
2.3 Протолитические равновесия в водных растворах при образовании объёмных бициклов некоторых многоосновных органических кислот
Известно, что янтарная кислота является одной из важнейших кислот, участвующих в биохимических процессах при созревании пищевого сырья, в частности, винограда. Массовая концентрация янтарной кислоты в готовых винах может колебаться от следов до 1 г/дм3 и выше. Так как янтарная кислота оказывает благотворное влияние на организм человека, являясь важным микронутриентом в физиологии питания, то актуальным вопросом является создание современной технологии производства вина, позволяющей накапливать в готовом продукте максимальную концентрацию данной кислоты. Поэтому необходимо изучить поведение и свойства янтарной кислоты и её солей в водных растворах.
На основании потенциометрического метода определения суммы органических и минеральных кислот с кулонометрической генерацией основания, предложенного в работах [95; 96], нами были изучены ионизация и строение димеров янтарной кислоты в водных растворах [97; 98].
Ранее в работах [99; 100; 101; 102; 103; 104; 105; 106; 107] было показано, что щавелевая, малоновая и янтарная кислоты и другие кислоты титруются как димеры с четырьмя кислотными протонами. Щавелевая кислота представляет собой линейный димер, в центре которого находится циклическая форма из двух карбоксильных групп, связанных двойной водородной связью. Оказалось, что концевые карбоксильные группы, не связанные в циклы, очень легко диссоциируют. Малоновая кислота представляет собой димер, который титруется по двум ступеням. Очевидно, что центр димера представляет собой также кольцо из карбоксильных групп, а концевые карбоксильные группы, в отличие от щавелевой кислоты, частично замкнуты во второе кольцо. Это кольцо непрочно, но усиливается по мере оттитровывания одного из четырех протонов. В работе [108] сделан вывод о том, что при удалении одного из протонов второй протон начинает взаимодействовать с четырьмя кислородными атомами, что и приводит к упрочнению кольца. Янтарная кислота титруется по четырём ступеням с примерно равными по силе константами диссоциации [109]. На основании этого авторами [108] сделан вывод, что её димер представляет собой объёмную кольцевую структуру, ионизация которой протекает в соответствии со схемой, представленной на рисунке 14.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



