2. Поверхностно-активные вещества. Адсорбция на границе раздела жидкость-газ и жидкость-жидкость. Уравнение Гиббса. Ориентация молекул в поверхностном слое и структура биологических мембран.
3. Адсорбция на границах раздела твердое тело-газ и твердое тело-жидкость. Уравнения Фрейндлиха и Лэнгмюра.
4. Адсорбция сильных электролитов. Ионообменная адсорбция. Иониты и их применение в медицине.
5. Хроматография, ее сущность и применение в медицине.
Раздел 7. Физикохимия дисперсных систем.
1. Особенности коллоидного состояния вещества. Получение и свойства коллоидных растворов, методы их очистки. Диализ, электродиализ, ультрафильтрация. Гельфильтрация. Искусственная почка.
2. Молекулярно-кинетические свойства коллоидных систем.
3. Особенности оптических свойств коллоидных систем.
4. Механизм возникновения электрического заряда коллоидных частиц. Мицелла, ядро, гранула. Электрокинетические явления. Электрофорез. Иммуноэлектрофорез. Электроосмос. Их использование в медицинской практике.
5. Устойчивость коллоидных систем. Коагуляция. Закономерности электролитной коагуляции. Порог коагуляции. Правило Шульце-Гарди. Коагуляция золей смесями электролитов. Коллоидная защита. Пептизация. Значение этих явлений в медицине
6. Виды дисперсных систем и их свойства. Аэрозоли как лекарственные формы и как причины возникновения некоторых заболеваний легких. Суспензии. Эмульсии. Полуколлоиды. Липосомы как модели клеток.
Раздел 8. Строение атомов и химическая связь. Химия биогенных элементов.
1. Атомная орбиталь. Характеристика энергетического состояния электрона набором квантовых чисел: главное, орбитальное, магнитное и спиновое квантовые числа. Принцип минимума энергии. Правило Хунда. Основное и возбужденное состояние атома.
2. Периодический закон и периодическая система в свете квантовой теории строения атома. s-, p-, d-, f - блоки элементов. Периодичность изменения радиусов атомов и ионов, энергии ионизации и сродства к электрону, электроотрицательности элементов.
3. Химическая связь и строение молекул. Метод валентных связей. Механизм образования ковалентной химической связи. Энергия связи. Сигма и пи связи. Насыщаемость, направленность и длина связи.
4. Понятие о методе молекулярных орбиталей.
5. Водородная связь. Межмолекулярная и внутримолекулярная водородная связь. Роль водородной связи в биохимических процессах.
6. Биогенные элементы. Понятие о биогенных элементах. Макро - и микроэлементы элементы в окружающей среде и организме человека. Человек и биосфера. Охрана окружающей среды. Закономерности распределения биогенных элементов в организме человека.
7. Общая характеристика s-элементов. Щелочные и щелочноземельные элементы. Водород, изотопы водорода и их применение в медицине и медицинских исследованиях. Пероксид водорода. Кислотно-основные и окислительно-восстановительные свойства. Роль пероксида водорода как побочного продукта метаболизма в жизнедеятельности организмов. Бактерицидные свойства пероксида водорода.
8. Элементы Iа и IIa групп. Важнейшие соединения: оксиды, пероксиды, гидроксиды, соли. Физико-химические свойства важнейших представителей. Соединения кальция в костной ткани. Радиостронций -90. Бериллий. Типичные аналитические реакции на элементы Iа и IIa групп. Применение в медицине карбонатов и хлоридов элементов Ia группы, оксидов, сульфатов, карбонатов и хлоридов элементов II a группы.
9. D-Элементы и их соединения. Общая характеристика d-элементов. Переходные металлы. Изменение комплексообразующих свойств в соответствии с периодическим законом . Переходные металлы в ферментах.
10. Элементы Ib и IIb групп. Общая характеристика групп. Типичные свойства важнейших соединений меди, серебра, золота, цинка, ртути. Аналитические реакции на элементы Ib и IIb групп. Хром, молибден, марганец их биологическое значение в организме. Применение соединений элементов YIb и YIIb в медицине.
11. Элементы YIIIb группы. Общая характеристика группы. Типичные свойства важнейших соединений железа, кобальта, никеля. Аналитические реакции на данные элементы. Железо, кобальт, никель в организме и их биологическая роль.
12. P-Элементы и их соединения. Общая характеристика p - элементов. Типичные свойства важнейших соединений. Кислорода, серы, фосфора, азота.
13. Элементы YIIa группы. Типичные свойства важнейших соединений галогенов, их биологическая роль.
Контролируемые компетенции: ОПК-7.
Дифференцированный зачет проводится в виде тестовых заданий. Комплекты индивидуальных тестовых заданий для дифференцированного зачета составлены в соответствии с программой курса и включают 30 вопросов.
Пример теста.
Вариант ХХХ.
1. Почему термодинамика рассматривает не абсолютные значения внутренней энергии, а только её изменение?
Потому, что оценка абсолютного значения внутренней энергии не входит в задачу термодинамики, а входит в задачу другого раздела физической химии. Потому, что термодинамика связывает взаимный переход теплоты и работы с изменением внутренней энергии системы, зависящей от пути перехода из одного состояния в другое. Потому, что невозможно оценить количественно совокупность всех видов энергии, составляющих систему молекул, атомов и элементарных частиц. Потому, что именно изменение внутренней энергии характеризует процесс перехода системы из одного состояния в другое.2. Напишите уравнение I закона термодинамики для конечного изменения состояния системы и укажите какие величины, входящие в это уравнение, зависят от пути процесса.
Q = ΔU + A; Q и A. 3) Q = ΔU + A; Q и ΔU. A = Q + ΔU; ΔU. 4) ΔQ = A + ΔU; ΔU и A.3. Коллигативным свойством растворов не является
1) осмотическое давление;
2) повышение температуры кипения;
3) понижение температуры замерзания;
4) степень диссоциации.
4. Закон Рауля справедлив для …
1) предельно разбавленных растворов;
2) концентрированных растворов;
3) растворов любых концентраций;
4) растворов неэлектролитов.
5. Изменение концентрации реагирующего вещества в единицу времени в единице объема называется:
Механизмом реакции; 3) скоростью химической реакции; порядком реакции; 4) молекулярностью реакции.6. Покажите характер зависимости периода полураспада от начальной концентрации в реакции второго порядка.
1) τ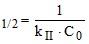 ; 2) τ
; 2) τ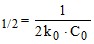 ;
;
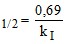 ; 4) τ
; 4) τ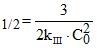 .
. 7. Какую величину можно использовать в качестве критерия оценки силы электролита:
а) pH раствора; б) константу диссоциации;
в) удельную электропроводность; г) ионную силу раствора.
8. Укажите какой из приведенных гальванических элементов является химическим гальваническим элементом:
а) Ni | NiCl2 (С1) || (С2) AgNO3 | Ag; б) Ni | NiCl2(C1) || NiCl2(C2) | Ni;
в) (Pt) | Sn2+, Sn4+ || Fe3+, Fe2+ | (Pt); г) правильный ответ не указывается.
9. Структурной и кинетической единицей в коллоидно-дисперсных системах являются:
а) атомы б) молекулы
в) мицеллы, либо молекулы-полимеры.
10. Выберите правильно изображенную мицеллу коллоидной частицы
а) {[mAgCl]nNa+(n-x)Cl-}xCl-
б) {[mAgCl]nSO42-(n-x)Ag+}-2xxAg+
в) {[mAgCl]·nCl - ·(n-x)Na+}-x ·хNa+
11. Какое из приведенных уравнений является уравнением Фрейндлиха?
а) Г=к ⋅ с 1/n; б) Г =к / с 1/n;
в) Г=к ⋅ п 1/с; г) Г =х / m.
12. Молекулы поверхностного слоя обладают …
1) меньшей энергией по сравнению с молекулами в объеме фазы;
2) одинаковой энергией с молекулами в объеме фазы;
3) большей энергией по сравнению с молекулами в объеме фазы;
4) в зависимости от природы вещества могут обладать большей,
меньшей или одинаковой энергией
13. Для измерения pH желчи был составлен гальванический элемент из водородного и насыщенного хлорсеребряного электродов. ЭДС этого элемента при 298 К оказалась равной 0,577 В, потенциал насыщенного хлорсеребряного электрода составляет 0,222 В. Рассчитайте pH желчи.
14. Вычислите, во сколько раз увеличится скорость реакции при повышении температуры на 50 °C, принимая температурный коэффициент скорости реакции равным 2.Чему равна энергия активации реакции, если начальная температура равна 25°C?
15. Золь AgCl получен путем смешивания равных объёмов 0,0095 М раствора хлорида калия и 0,012 М раствора нитрата серебра.
Напишите молекулярное уравнение реакции, полное ионное уравнение, определите вещество - стабилизатор, составьте формулу строения мицеллы золя AgCl (укажите агрегат, ядро, потенциалопределяющие (ПО) и противоионы (ПИ), диффузный слой).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



