Вариант 2
1. В каких единицах измеряется молярная электропроводность?
Варианты ответа
а) Ом-1 м-1; б) Ом-1;
в) Ом-1 м2 моль-1; г) не указан.
2. Напишите формулу, позволяющую рассчитать эквивалентную электропроводность раствора?
Варианты ответа
а) ![]()
![]() б)
б) 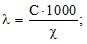
в) ![]() г) ответ не указан.
г) ответ не указан.
3. Электроды, потенциал которых зависит от концентрации ионов водорода в исследуемом растворе, относятся:
Варианты ответа:
а) к электродам сравнения;
б) к электродам определения (индикаторные электроды);
в) правильный ответ не указывается;
г) к окислительно-восстановительным электродам.
4. Укажите какой из приведенных гальванических элементов относится к концентрационному гальваническому элементу.
Варианты ответа:
а) Ni | NiCl2 || AgNO3 | Ag; б) Ni | NiCl2(C1) || NiCl2(C2) | Ni;
в) (Pt) | Sn2+, Sn4+ || Fe3+, Fe2+ | (Pt); г) правильный ответ не указывается.
5. Какой электрод можно использовать в качестве отрицательного электрода в паре с хлоридсеребряным электродом?
Варианты ответа:
а) Ni | NiSO4 (ц° = −0,25В) ; б) Cu | CuSO4 (ц° = +0,34В)
в) Mg | MgSO4 (ц° = −2,36В) ; г) Ag | AgNO3 (ц° = +0,799В)
5. На поверхности стандартного водородного электрода
(Pt) H2 | НCI (1 M) протекает электрохимическая реакция:
Варианты ответа:
1) Pt4+ +4з ↔ Pt0; 2) H2 + Pt4+ ↔ Pt0 + 4H+;
3) 2H+ + 2з ↔ H2; 4) 2H+ + Pt0 ↔ 2H2 + Pt0.
в) Ag | AgNO3( ц°= +0,799В) ; г) правильный ответ не указывается.
Вариант 3
1. Напишите формулу, связывающую удельную электропроводность (χ), постоянную сосуда (Z) и сопротивление раствора электролита (Rx).
Варианты ответа
а) χ = z ⋅ Rx; б) 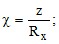
в) ![]() г) не указан.
г) не указан.
2. Какой электрод записывается слева в условной форме записи гальванического элемента?
Варианты ответа:
а) электрод, стандартный электродный потенциал которого более положительный;
б) электрод, стандартный электродный потенциал которого более отрицательный;
в) любой электрод;
г) правильный ответ не указывается.
3. Электрод, потенциал которого зависит от концентрации ионов водорода в исследуемом растворе:
Варианты ответа:
а) каломельный;
б) хингидронный
в) правильный ответ не указывается;
г) хлоридсеребряный.
4. При каком соотношении концентраций растворов ЭДС медно-цинкового гальванического элемента будет наибольшей?
Варианты ответа:
а) Zn | ZnSO4 (0,1 M) || CuSO4 (0,1 M) | Cu;
б) Zn | ZnSO4 (0,1 M) || CuSO4 (1 M) | Cu;
в) Zn | ZnSO4 (0,01 M) || CuSO4 (1 M) | Cu;
г) Zn | ZnSO4 (1,0 M) || CuSO4 (1,0 M) | Cu.
5. На поверхности стандартного водородного электрода
(Pt) H2 | НCI (1 M) протекает электрохимическая реакция:
Варианты ответа:
1) Pt4+ +4з ↔ Pt0; 2) H2 + Pt4+ ↔ Pt0 + 4H+;
3) 2H+ + 2з ↔ H2; 4) 2H+ + Pt0 ↔ 2H2 + Pt0.
Вариант 4
1. Каким образом связаны между собой удельная (χ) и эквивалентная (λ) электропроводности? Напишите формулу.
Варианты ответа
а) ![]() в)
в) ![]()
б) ![]() г) ответ не указан.
г) ответ не указан.
2. Каким образом удельная электропроводность сильного электролита зависит от концентрации раствора?
Варианты ответа
а) Увеличивается; б) проходит через максимум;
в) проходит через минимум; г) уменьшается.
3. К какому типу электродов относится электрод Cu | CuSO4?
Варианты ответа:
а) электрод I рода; б) электрод II рода;
в) электрод сравнения; г) окислительно-восстановительный электрод.
4. Укажите какой из приведенных гальванических элементов относится к окислительно-восстановительным.
Варианты ответа:
а) Ag | AgCl, KCl || CuSO4 | Cu; б) (Pt) | Sn2+, Sn4+ || Fe3+, Fe2+ | (Pt);
в) Zn | ZnSO4 || CuSO4 | Cu. г) правильный ответ не указывается;
5. Какой электрод можно использовать в качестве отрицательного электрода в паре с медным электродом Cu | CuSO4?
Варианты ответа:
а) Zn | ZnSO4 (ц° = −0,76В) ; б) Ag | AgNO3 (ц° = +0,799В) ;
в) (Pt) | Fe2+, Fe3+ (ц° = +0,77В) ; г) правильный ответ не указывается.
Вариант 5
1. Каким образом удельная электропроводность сильного электролита зависит от концентрации раствора?
Варианты ответа
а) Проходит через минимум; в) уменьшается;
б) проходит через максимум; г) увеличивается.
2. Напишите закон Кольрауша, для электропроводности растворов электролитов при бесконечном разбавлении.
Варианты ответа
а) α = ![]() ; б) λ∞ = λа + λк;
; б) λ∞ = λа + λк;
в) 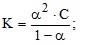 г) λк = F ⋅ Uк; λа = F ⋅ Uа;
г) λк = F ⋅ Uк; λа = F ⋅ Uа;
3. К какому типу электродов относится электрод Hg | Hg2Cl2, KCl?
Варианты ответа:
а) электрод сравнения;
б) электрод определения;
в) окислительно-восстановительный электрод;
г) электрод I рода.
4. Укажите схему гальванического элемента, с помощью которого можно измерить pH раствора.
Варианты ответа:
а) Ag | AgCl, KCl | H+, хинон, гидрохинон | (Pt);
б) Ag | AgCl, KCl | CuSO4 | Cu; в) Ag | AgCl, KCl || KCl, Hg2Cl2 | Hg;
г) правильный ответ не указывается.
5. Какой электрод можно использовать в качестве положительного электрода в паре с никелевым электродом Ni | NiSO4?
Варианты ответа:
а) Zn | ZnSO4 (ц° = −0,76В) ; б) Cu | CuSO4 (ц° = +0,34В) ;
в) Mg | MgSO4 (ц° = −2,36В) ; г) правильный ответ не указывается.
Вариант 6
1. К какому типу электродов относится электрод (Pt) | Sn2+, Sn4+?
Варианты ответа:
а) электрод сравнения; б) электрод определения;
в) окислительно-восстановительный электрод; г) электрод I рода.
2. Укажите схему гальванического элемента, с помощью которого можно измерить pH раствора.
Варианты ответа:
а) Ag | AgCl, KCl || AgNO3 | Ag; б) (Pt) | H2, H+ || KCl, AgCl | Cl;
в) Ag | AgCl, KCl || Сu2+ | Сu0 ; г) правильный ответ не указывается.
3. Какой электрод можно использовать в качестве отрицательного электрода в паре с алюминиевым электродом Al | AlCl3(ц° = −1,66В) ?
Варианты ответа:
а) Mg | MgSO4 (ц° = −2,36В); б) Zn | ZnSO4(ц° = −0,76В) ;
в) Fe | FeCl2 (ц° = −0,44В); г) Fe | FeCl3(ц° = −0,037В) .
4. Удельная электрическая проводимость с ростом концентрации…
Варианты ответа:
а) не изменяется; б) увеличивается;
в) уменьшается; г) вначале увеличивается, затем уменьшается.
5. При одинаковой концентрации самую высокую электрическую
проводимость будет иметь водный раствор:
Варианты ответа:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



