Варианты ответа
Правильный ответ не указывается; безразмерная величина; концентрация-2⋅время-1; время-1.5. Реакция между газообразными NO и Сl2протекает по уравнению:
2NO + Сl2 = 2NOCl.
Как изменится скорость реакции при увеличении концентраций обоих исходных веществ в 2 раза?
Вариант 9
1. Какие экспериментальные данные необходимо иметь для определения константы скорости?
Варианты ответа
Температуру и давление; энергию активации при двух различных температурах; изменение концентрации реагирующих веществ с течением времени при постоянной температуре; период полураспада веществ.2. Влияет ли изменение концентрации исходных веществ на величину константы скорости?
Варианты ответа
С уменьшением концентрации исходных веществ константа скорости уменьшается; с уменьшением концентрации исходных веществ константа скорости увеличивается; с уменьшением концентрации исходных веществ константа скорости остается постоянной величиной; правильный ответ не указывается.3. В каком количественном соотношении находятся константы скорости двух реакций первого порядка, если известно, что период полупревращения первой реакции в пять раз больше, чем второй?
Варианты ответа
Правильный ответ не указывается; k1< k2; 5k1 = k2; k1 = 5k2.4. За время равное 10 сек, концентрация вещества А изменилась от 3,10 до 3,05 моль/л. Укажите среднее значение скорости реакции по веществу А:
Варианты ответа
а) 0,005л/моль·мин;
б) 0,005 моль/л·сек;
в) 0,3 моль/л·мин;
г) 0,3л/моль·мин.
5. Во сколько раз повысится скорость химической реакции при увеличении температуры процесса от 21 до 54 °С, если температурный коэффициент скорости реакции равен 2?
Вариант 10
1. Константа скорости некоторой реакции имеет размерность - c-1. Каков порядок этой реакции?
Варианты ответа
1; 2; 0; 3.2. Изобразите схематически график линейной зависимости, которым следует воспользоваться для определения энергии активации реакции. Напишите соответствующую расчетную формулу.
Варианты ответа
1)
2)
3) правильный ответ не указывается;
4)
3. Какие из следующих факторов влияют на скорость химической реакции?
Варианты ответа
природа реагирующих веществ; концентрация реагирующих веществ; катализатор; растворитель;5) температура.
4. Для некоторой реакции 1-го порядка при C0 = 1 моль/лτ1/2 = 500 с.
Каково значение τ1/2 при C0 = 2 моль/л.?
Варианты ответа
1) 500 с;
2) 1000 с;
3) правильный ответ не указывается;
4) 250 с.
5. Написать выражение кинетического уравнения процесса:
2СО + О2 = 2СО2,
определить во сколько раз увеличится скорость реакции, если повысить концентрацию СО в 3 раза и понизить О2 в 2 раза.
Вариант 11
1. Необходимый избыток энергии (по сравнению со средним уровнем), которым должны обладать молекулы, чтобы реакция была возможной, называется:
Варианты ответа
Внутренней энергией системы; энергией активации; поверхностной энергией; свободной энергией.2. Можно ли по написанному уравнению химической реакции установить кинетический порядок реакции?
Варианты ответа
Нельзя; можно, если реакция является простой (идущей в одну стадию); можно, если реакция является сложной (идущей в несколько стадий);4) правильный ответ не указывается.
3. Укажите формулу для расчета константы скорости реакции второго порядка при равных исходных концентрациях реагирующих веществ.
Варианты ответа
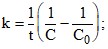 правильный ответ не указывается;
правильный ответ не указывается; 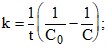
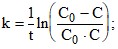
4. Напишите уравнение зависимости константы скорости реакции от температуры.
Варианты ответа
Правильный ответ не указывается; ln v =5. Как изменится скорость реакции, протекающей в газовой фазе, при повышении температуры на с 32°С до 54°С, если температурный коэффициент скорости реакции равен 2,2?
Вариант 12
1. Влияет ли присутствие катализатора в системе на величину энергии активации?
Варианты ответа
Не оказывает влияния; увеличивает величину энергии активации; уменьшает величину энергии активации; свой вариант ответа.2. Напишите выражение для константы скорости реакции первого порядка, если C0-концентрация исходного вещества в начальный момент времени, C-концентрация исходного вещества в момент времени t
Варианты ответа
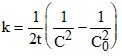 ; правильный ответ не указывается;
; правильный ответ не указывается; 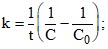
3. Как меняется lg k с ростом величины 1/T? Покажите это графически.
Варианты ответа
правильный ответ не указывается;
4. Какие из следующих факторов влияют на скорость химической реакции: природа реагирующих веществ, концентрация реагирующих веществ, катализатор, растворитель, температура?
Варианты ответа
Влияют все переменные факторы; температура и катализатор; растворитель, концентрация, температура; правильный ответ не указывается.5. Как изменится скорость гомогенного процесса:
2Н2 + О2 = 2Н2О,
если повысить давление в системе в 4 раза?
Решение:
Вариант 13
1. Процессы, в которых превращение исходных веществ в продукты реакции осуществляется путем регулярного чередования нескольких реакций с участием свободных радикалов, называются:
Варианты ответа
Сопряженными; параллельными; последовательными: цепными.2. Изобразите схематически график линейной зависимости, которым следует воспользоваться для определения энергии активации реакции. Напишите соответствующую расчетную формулу.
Варианты ответа
правильный ответ не указывается;
3. Укажите размерность константы скорости реакции первого порядка.
Варианты ответа
Правильный ответ не указывается; безразмерная величина; концентрация-2⋅время-1; время-1.4. Если константа скорости одной реакции (k') больше константы скорости второй реакции (k"), то какое соотношение между энергиями активации этих реакций при одинаковой температуре:
Варианты ответа
1) Еа'>Ea";
3) нельзя определить;
2) Ea'<Ea";
4) Еа'>>Ea".
5. Во сколько раз увеличится скорость процесса при повышении температуры с 35°С до 67°С, если температурный коэффициент скорости реакции равен 2,5?
Решение:
Вариант 14
1. В какой из реакций энергия активации будет наименьшей?
Варианты ответа
Каталитической; некаталитической; ферментативной;4) правильный ответ не указывается.
2. Укажите размерность константы скорости реакции 2-порядка.
Варианты ответа
Правильный ответ не указывается; время-2 концентрация-2; время-1 концентрация-1; время-1 концентрация-2.3. Напишите математическое выражение правила Вант-Гоффа.
Варианты ответа
Правильный ответ не указывается;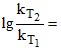 γ;
γ; 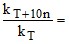 γn.
γn. 4. Зависит ли и как от исходной концентрации реагирующего вещества период полупревращения для реакции 1-го порядка?
Варианты ответа
Правильный ответ не указывается; возрастает с ростом концентрации; падает с ростом концентрации; не зависит.5. Период полураспада ф исходного вещества в реакции первого порядка выражается формулой (с0– начальная концентрация, k – констант а скорости реакции):
Варианты ответа
1) С = С0 – kф
2) lnC = lnC0 – kф
3) С = С0+kф
4) ![]()
5) ![]()
Контролируемые компетенции: ОПК-7
Критерии оценок (максимальный балл 2,5)
2,5 балла выставляется, если студент правильно ответил на все 5 вопросы теста.
Каждый вопрос теста оценивается в 0,5 балла.
Тестовое задание №2 Тема: “Электрохимия ”
Вариант 1
1. В каких единицах измеряется удельная электропроводность?
Варианты ответа
а) Ом-1 м2; б) Ом-1 м-1;
в) Ом-1 ; г) Ом1 м2 моль-1.
2. Электроды, имеющие постоянное значение электродного потенциала, относятся:
Варианты ответа:
а) к электродам определения;
б) к электродам сравнения;
в) к окислительно-восстановительным электродам;
г) правильный ответ не указывается.
3. Укажите какой из приведенных гальванических элементов относится к химическому гальваническому элементу.
Варианты ответа:
а) Ni | NiCl2 || AgNO3 | Ag; б) Ni | NiCl2(C1) || NiCl2(C2) | Ni;
в) (Pt) | Sn2+, Sn4+ || Fe3+, Fe2+ | (Pt); г) правильный ответ не указывается.
4. Какой электрод записывается слева в условной форме записи гальванического элемента?
Варианты ответа:
а) электрод, стандартный электродный потенциал которого более положительный;
б) электрод, стандартный электродный потенциал которого более отрицательный;
в) любой электрод;
г) правильный ответ не указывается.
5. При каком соотношении концентраций растворов ЭДС медно-цинкового гальванического элемента будет наибольшей?
Варианты ответа:
а) Zn | ZnSO4 (1 M) || CuSO4 (1 M) | Cu;
б) Zn | ZnSO4 (0,1 M) || CuSO4 (1 M) | Cu;
в) Zn | ZnSO4 (0,01 M) || CuSO4 (1 M) | Cu;
г) Zn | ZnSO4 (1 M) || CuSO4 (0,1 M) | Cu.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



