Варианты ответа
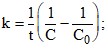 правильный ответ не указывается;
правильный ответ не указывается; 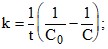
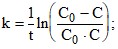
4. При введении в систему катализатора скорость химических процессов увеличивается за счет:
Варианты ответа
а) увеличения кинетической энергии молекул;
б) возрастания числа столкновений;
в) уменьшения числа активных молекул;
г) уменьшения энергии активации процесса.
5. Взаимодействие оксида углерода (II) с хлором выражено уравнением:
CO + Cl2![]() COCl2.
COCl2.
Концентрация CO равна 0,3 моль/л, а хлора - 0,2 моль/л. Во сколько раз увеличится скорость прямой реакции, если увеличить концентрацию CO до 1,2 моль/л, а концентрацию Cl2- до 0,6 моль/л? Считать, что это реакция второго порядка.
Решение:
Вариант 2
1. Может ли скорость химической реакции быть отрицательной величиной? Варианты ответа
Да; нет; может, в зависимости от конкретного случая.4) ответить однозначно трудно
2. Отразится ли на величине константы скорости реакции замена одного катализатора другим? Варианты ответа
Не отразится; константа скорости увеличится; константа скорости уменьшится; в зависимости от вида катализатора, константа скорости может как увеличиться, так и уменьшиться.3. Напишите уравнение зависимости константы скорости реакции от температуры.
Варианты ответа
Правильный ответ не указывается; ln v =4. Энергия активации химического процесса – это:
Варианты ответа:
1) избыточная кинетическая энергия молекул исходных веществ, которая при столкновении молекул, позволяет разрушить связи между атомами в молекулах и привести к образованию новых химических связей в продуктах реакции;
2) общий запас внутренней энергии системы;
3) разница между потенциальной энергией молекул продуктов реакции и исходных веществ;
4) внутренняя энергия химической системы, способной совершить механическую работу.
5. Во сколько раз изменится скорость гомогенной реакции:
2А + В = А2В,
если концентрацию А увеличить в 2 раза, а концентрацию В одновременно уменьшить в 2 раза?
Вариант 3
1. Какие факторы оказывают влияние на скорость химической реакции?
Варианты ответа
Природа реагирующих веществ и растворителя; концентрация и температура; присутствие и концентрация катализатора; все перечисленные выше факторы.2. Какими уравнениями описывается влияние температуры на скорость реакции?
Варианты ответа
τ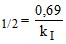 ;
; 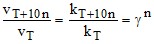 ;
; 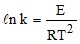 + const;
+ const; 3. Каков физический смысл константы скорости реакции?
Варианты ответа
скорость реакции при концентрации реагирующих веществ равных 1 моль/л; правильный ответ не указывается; скорость реакции в данный момент времени; скорость реакции при данной температуре.4. Кинетическим уравнением для данного гомогенного процесса:
2NO(Г)+ O2(Г) = 2NO2(Г), является:
Варианты ответа
1) v = k[NO]2[O2]
2) v = k[O2]
3) v = k[NO2]2
4) v = k[NO]2
5. Вычислить, во сколько раз увеличится скорость реакции при повышении температуры с 25°C до 53°С, принимая температурный коэффициент скорости реакции равным 2.
Вариант 4
1. Можно ли по значениям констант скоростей, измеренным при одинаковых температурах, сравнить с какой скоростью протекают две различные реакции?
Варианты ответа
4) правильный вариант не указан.
2. Энергия активации для реакции распада пероксида водорода под действием иона железа (II) и молекулы наталазы соответственно равны 42 и 7,1 кДж/моль. В каком случае разложение H2O2 произойдет быстрее и почему?
Варианты ответа
Величина энергии активации не оказывает влияния на химические процессы; чем выше энергия активации, тем быстрее пойдет процесс разложения H2O2; чем ниже энергия активации, тем быстрее пойдет процесс разложения H2O2; чем ниже энергия активации, тем медленнее протекает химическая реакция.3. Единица измерения скорости химической реакции
Варианты ответа
A) с·л/моль;B) моль·с/л;C) моль/л·с; D) г/моль E) кДж/моль.
4. Как изменится скорость реакции
2NO(г) + O2(г) = 2NO2(г),
если уменьшить объем реакционного сосуда в 3 раза?
5. Напишите математическое выражение правила Вант-Гоффа.
Варианты ответа
Правильный ответ не указывается;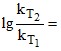 γ;
γ; 4) 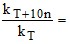 γn.
γn.
Вариант 5
1. Число частиц вступающих в химическое взаимодействие в элементарном акте превращения определяет:
Варианты ответа
Порядок реакции; скорость реакции; молекулярность реакции; механизм реакции.2. Что понимают под механизмом реакции?
Варианты ответа
Число частиц, участвующих в элементарном акте превращения; изменение концентрации реагирующих веществ в единицу времени в единице объема; совокупность стадий, из которых складывается химическая реакция; правильный ответ не указывается.3. От каких факторов зависит величина константы скорости химической реакции?
Варианты ответа
правильный ответ не указывается; от температуры, природы реакции, катализатора; от концентрации, температуры; от времени реакции, температуры.4. Напишите уравнение зависимости константы скорости реакции от температуры в дифференциальной форме.
Варианты ответа
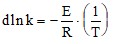 ;
; 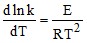 .
. 4) ответ не указан
5. Температурный коэффициент скорости реакции равен 3. Во сколько раз возрастет скорость реакции при повышении температуры от 22 до 78°C?
Вариант 6
1. Сформулируйте основной закон кинетики - закон действующих масс.
Варианты ответа
Вещества взаимодействуют друг с другом в количествах, пропорциональных их эквивалентам; в равных объемах любых газов, взятых при одной и той же температуре и при одинаковом давлении, содержится одно и то же количество молекул; скорость химической реакции при постоянной температуре прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях соответствующих стехиометрическим коэффициентам; масса веществ, вступающих в реакцию, равна массе веществ, образующихся в результате реакции.2. Молекулы, которые обладают определенным запасом энергии, необходимой для осуществления той или иной реакции, называются:
Варианты ответа
Активными; дифильными; полярными; неполярными.3. Покажите графически, как зависит константа скорости реакции от исходной концентрации веществ?
Варианты ответа
1) правильный ответ не указывается;
2)
3)
4)
4. Какие из следующих факторов влияют на константу химической реакции: природа реакирующих веществ, концентрация, катализатор, растворитель, температура?
Варианты ответа
Концентрация реагирующих веществ, температура; влияют все факторы; природа реагирующих веществ, катализатор, растворитель, температура; правильный ответ не указывается.5. Записать кинетическое уравнение гомогенного процесса, протекающего по уравнению:
АВ + 2С = А + ВС2.
Определить, во сколько раз увеличится скорость реакции, если концентрацию АВ увеличить в 2 раза, а концентрацию C увеличить 3 раза?
Вариант 7
1. Молекулярность реакции может выражаться:
Варианты ответа
Только дробным числом; только целым числом; может быть как целым, так и дробным числом; может быть отрицательной величиной.2. Зависит ли и как от исходных концентраций реагирующих веществ период полупревращения для реакции 2-го порядка?
Варианты ответа
Правильный ответ не указывается; не зависит; прямо пропорционален исходной концентрации; обратно пропорционален исходной концентрации.3. Реакции, в которых активация частиц одного из реагирующих веществ осуществляется в результате поглощения кванта света, называются:
Варианты ответа
Фотохимическими; ферментативными; каталитическими; сопряженными.4. Какие факторы влияют на скорость химической реакции:
Варианты ответа
а) природа реагирующих веществ;
б) концентрация реагирующих веществ;
в) температура;
г) присутствие катализатора.
5. Как изменится скорость реакции, протекающей в газовой фазе, при увеличении температуры с 13°С до 59°С, если температурный коэффициент скорости реакции равен 2,3?
Вариант 8
1. В лабораторных условиях кислород часто получают разложением бертолетовой соли в присутствии оксида марганца (IV) в качестве катализатора. Какой это тип катализа?
Варианты ответа
Гетерогенный; микрогетерогенный (связан с ферментативными процессами); гомогенный;4) правильный ответ не указывается.
2. Могут ли порядок реакции и молекулярность быть дробными величинами?
Варианты ответа
Порядок может, молекулярность - нет; молекулярность может, порядок - нет. не могут; правильный ответ не указывается.3. Напишите уравнение зависимости константы скорости реакции от температуры.
Варианты ответа
Правильный ответ не указывается; ln v =4. Укажите размерность константы скорости реакции первого порядка.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



