3. У эритроцитов человека гемолиз начинается в 0,4%-ном растворе хлорида натрия, а в 0,34%-ном растворе NaCl наступит «осмотический шок». Каково осмотическое давление этих растворов при 37°С, если принять плотность раствора с = 1 г/мл и степень диссоциации соли равной 86%?
4. Понижение давления насыщенного пара над водным раствором глюкозы по сравнению с чистой водой при 293 К равно 963 Па. Давление насыщенного пара воды при этой температуре равно 2338 Па. Определите молярную долю глюкозы в растворе.
5. Чему будет равняться изотонический коэффициент Вант-Гоффа для хлорида кальция, если это вещество полностью продиссоциировало в водном растворе:
1) i = 1 2) i = 2 3) i = 3 4) i =4
Вариант №8
1. Вычислите процентную концентрацию водного раствора сахара С12Н22О11, зная, что температура кристаллизации раствора равна –0,93°С. Криоскопическая константа воды 1,86 (К кг)/моль.
2. Раствор, содержащий 1,22 г бензойной кислоты С6Н5СООН в 100 г сероуглерода, кипит при 46,529°С. Температура кипения сероуглерода 46,3°С. Вычислить эбуллиоскопическую константу сероуглерода.
3. Вычислите степень диссоциации нитрата калия в 0,2М растворе, имеющего при Т= 37°С осмотическое давление равное 917 кПа.
4. Рассчитайте молярную массу неэлектролита, если 28,5 г этого вещества, растворенного в 785 г воды, вызывают понижение давления пара воды над раствором на 52,37 Па при 25°С. Давление пара над чистым растворителем равно 7375,9 Па
5. Для 0,01 моляльных растворов NaCl, K2SO4 и FeCl3 при степени диссоциации б=1 выполняется соотношение..…
1)Тк(NaCl) >Тк (K2SO4) >Тк (FeCl3);
2)Тк (K2SO4) >Тк (FeCl3) >Тк (NaCl);
3)Тк (FeCl3) >Тк (K2SO4) >Тк (NaCl);
4)Тк (NaCl) >Тк (FeCl3) >Тк (K2SO4).
Вариант №9
1. Раствор, содержащий 0,85 г хлорида цинка в 125 г воды, кристаллизуется при – 0,23°С. Рассчитайте кажущуюся степень диссоциации хлорида цинка в данном растворе.
2. При растворении 20 г твердого вещества в 300 г бензола было экспериментально установлено, что температура кипения бензола повысилась от 80,1°С до 80,9°С. Какова молярная масса растворенного вещества, если эбуллиоскопическая константа для бензола равна 2,36 (К∙кг)/моль?
3. Рассчитайте осмотическое давление при 310 К 20%-ного раствора глюкозы (если плотность раствора с = 1,08 г/см3), используемого для внутривенных вливаний и сравните с осмотическим давлением крови.
4. При температуре 70°С давление водяного пара составило 31,2·103 Па. Давление пара над раствором, содержащим 65,6 г вещества в 180 г воды, при этой же температуре было на 500 Па ниже. Рассчитайте молярную массу растворенного вещества.
5. Водный раствор замерзает при температуре –1,86°С (КН2О = 1,86(кг∙град/моль)). Моляльность данного раствора составляет (моль/кг):
1) 0,5; 2) 1; 3) 3,72; 4) 0,6.
Вариант №10
1. Какова массовая доля глицерина в водном растворе, если он замерзает при –0,52°С? Криоскопическая константа воды 1,86 (К кг)/моль.
2. При растворении 19,46 г сульфата натрия в 100 г воды температура кипения воды повысилась на 1,34 град. Определите степень диссоциации соли в растворе. Эбуллиоскопическая константа воды 0,512 град•кг/моль.
3. Осмотическое давление водного раствора 4 г неэлектролита в 200 мл воды равно 5,133·105 Па при 273 К. Определите молярную массу этого вещества.
4. При 315К давление насыщенного пара над водой равно 8,2 кПа. На сколько понизилось давление пара при указанной температуре, если в 540 г воды растворить 36 г глюкозы?
5 Для какого из электролитов изотонический коэффициент будет наибольшим:
1) С(NaCl) = 0,01 моль/л 2) С(K2SO4) = 0,01 моль/л
3) С(KCl) = 0,01 моль/л 4) С(MgSO4) = 0,01 моль
Вариант №11
1 Раствор, содержащий 0,512 г неэлектролита в 100 г бензола, кристаллизуется при 5,296 °С. Температура кристаллизации бензола 5,5°С. Криоскопическая константа бензола 5,1 (К кг)/моль. Вычислите молекулярную массу растворенного вещества.
2. Вычислите изотонический коэффициент и степень диссоциации KCl в растворе, если его моляльная концентрация в растворе равна 1 моль/кг, а температура кипения составила 100,94°С. Эбуллиоскопическая константа воды 0,512 град·кг/моль.
3. В 300 мл водного раствора глюкозы содержится 10 г растворенного вещества. При какой температуре осмотическое давление этого раствора составит 500 кПа?
4. Осмотическое давление водного раствора глицерина С3Н8О3 составляет при 0°С 567,3 кПа. Приняв плотность раствора равной единице, вычислить давление пара раствора при 0°С, если давление пара воды при той же температуре составляет 610,5 кПа.
5. При одинаковой температуре даны 5 водных растворов с молярной концентрацией 0,05 моль/л. Какие из этих растворов являются изотоническими по отношению друг к другу:
а) СаС12 б) NаС1 в) С6Н12О6 г) МgSO4 д) AlCl3 ?
Вариант №12
1. Раствор, содержащий 1,05 г неэлектролита в 30 г воды, замерзает при –0,7°С (К(Н2О) =1,86 град·кг/моль). Определите молярную массунеэлектролита.
2. Вычислите температуру кипения водного раствора фруктозы, с массовой долей 5%. Эбуллиоскопическая константа воды 0,512 град·кг/моль.
3. Что произойдет с эритроцитами при 37°С в 2%-ном растворе глюкозы (с = 1,006 г/мл)?
4. Определите давление паров воды над раствором, если давление пара чистой воды при данной температуре равно 7,37 кПа. Мольная доля растворенного в воде вещества равняется 0,027.
5. При одинаковой температуре даны 5 водных растворов с молярной концентрацией 0,05 моль/л. Какие из этих растворов являются изотоническими по отношению друг к другу:
а) СаС12 б) NаС1 в) С6Н12О6 г) МgSO4 д) AlCl3 ?
Вариант №13
1. Вычислите температуру кристаллизации раствора мочевины (NH2)2CO, содержащего 5 г мочевины в 150 г воды. Криоскопическая константа воды 1,86 (К кг)/моль
2. Вычислите процентную концентрацию водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,39°С. Эбуллиоскопическая константа воды 0,512 (К кг)/моль.
3. При внутренних кровоизлияниях (легочных, желудочно-кишечных), а также для усиления диуреза внутривенно вводят от 5 до 20 мл 10%-ного раствора NaCl (с = 1,071 г/мл, б = 87%). Рассчитайте осмотическое давление этого раствора и определите, каким он будет по отношению к плазме крови. (Т = 37°С).
4. Давление насыщенного пара над раствором, содержащим 5,2 г некоторого вещества в 117 г воды, равно при 70°С 307 кПа. Давление насыщенного пара над водой при той же температуре равно 312 кПа. Определите молярную массу вещества.
5. Для какого из водных растворов температура кипения будет наибольшей:
1) Сm(FeCl3) = 0,01 моль/кг 2) Сm(KCl) = 0,01 моль/кг
3) Сm(K2SO4) = 0,01 моль/кг 4) Сm(NaCl) = 0,01 моль/кг
Вариант №14
1. Рассчитайте молярную массу неэлектролита, если его массовая доля в водном растворе 1,96%, а раствор замерзает при – 0,248°С.
2. Вычислите температуру кипения 0,9%-ного раствора NaCl, применяемого в медицинской практике, если степень его диссоциации равна 95%. Эбуллиоскопическая константа воды 0,512 град·кг/моль.
3. Какова степень электролитической диссоциации дихлоруксусной кислоты (Cl2CHCOOH) в ее 0,01 М растворе, если при 300К этот раствор создает осмотическое давление в 43596,4 Па?
4. В каком количестве воды надо растворить 6,84 г глюкозы С6Н12О6, чтобы давление пара воды, равное при 65°С 250 кПа, снизилось до 248 кПа
5. Установите, каким будет раствор по отношению к плазме крови (изо-,гипо - или гипертоническим) при 37°С хлорида калия с концентрацией 0,01 моль/л и степенью диссоциации 96%.
Контролируемые компетенции: ОПК-7
Критерии оценок (максимальный балл 5)
5 баллов выставляется, если студент привел полное и верное решение всех пяти расчетных задач;
4 -4,9 балла выставляется, если студент представил верное и полное решение четырех задач из пяти или допустил незначительные расчетные ошибки в одной из задач;
3 - 3,9 балла выставляется, если студент привел верное решение трех задач и частично решил другие задачи своего варианта.
2 - 2,9 балла выставляется, если студент привел верное решение двух задач и частично решил другие задачи своего варианта.
1 - 1,9 балла выставляется, если студент привел верное решение одной задачи задач и частично решил другие задачи своего варианта.
Комплект индивидуальных тестовых заданий
Тестовое задание №1. Тема: “Химическая кинетика”
Вариант 1
1. Изменение концентрации реагирующего вещества в единицу времени в единице объема называется:
Варианты ответа
Механизмом реакции; 2) скоростью химической реакции; порядком реакции; 4) молекулярностью реакции.2. Покажите характер зависимости периода полураспада от начальной концентрации в реакции второго порядка.
Варианты ответа
τ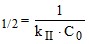 ; 2) τ
; 2) τ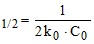 ; τ
; τ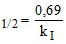 ; 4) τ
; 4) τ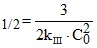 .
. 3. Укажите формулу для расчета константы скорости реакции второго порядка при равных исходных концентрациях реагирующих веществ.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



