Если свежая смесь движется навстречу фронту пламени со скоростью, равной скорости распространения пламени, то пламя будет неподвижным (стационарным).
Теоретическое обоснование условий распространения пламени можно привести при рассмотрении стационарного пламени, когда скорость его рас-пространения Uпл равна скорости подачи газовой смеси ?г: Uпл=?г (рис. 27). В данном случае соотношение между нормальной скоростью горения Uн и ско-ростью распространения пламени Uпл выразится уравнением:
Uн = Uпл*sin?. (7.1)
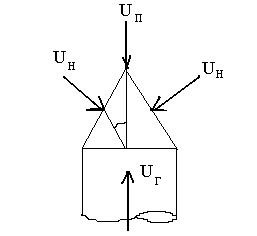
Рис. 27.
К свежей смеси от единицы поверхности пламени в единицу времени путем теплопроводности подводится количество тепла:
![]()
![]() (7.2)
(7.2)
где: ![]() - коэффициент теплопроводности;
- коэффициент теплопроводности;
![]() - ширина фронта пламени.
- ширина фронта пламени.
Это тепло расходуется на нагрев свежей смеси от начальной темпера-туры То до температуры горения Тг:
![]() (7.3)
(7.3)
где: с – удельная теплоемкость;
![]() - плотность смеси.
- плотность смеси.
С учетом уравнений (7.2) и (7.3) при Uпл=?г скорость распространения пламени определяется соотношением:
![]() (7.4)
(7.4)
где: ![]() - коэффициент температуропроводности.
- коэффициент температуропроводности.
Поскольку скорость горения очень сильно зависит от температуры, сгорание основной массы газа происходит в зоне, температура которой близ-ка к Тг.
Скорость химической реакции, как рассмотрено в § 6.1., определяется уравнением:
![]() . (7.5)
. (7.5)
Тогда скорость распространения пламени:
![]() (7.6)
(7.6)
где: b – показатель, зависящий от свойств смеси, ![]() .
.
Таким образом, пламя не сможет распространяться по горючей смеси, если его температура будет ниже теоретической температуры горения на ве-личину ![]() превышающую
превышающую ![]() (см. § 9.3).
(см. § 9.3).
![]() - характеристический интервал температур в химической кинетике. Изменение температуры на эту величину приводит к изменению скорости реакции в “e” раз.
- характеристический интервал температур в химической кинетике. Изменение температуры на эту величину приводит к изменению скорости реакции в “e” раз.
Предельное значение скорости распространения пламени UПРЕД опреде-ляется соотношением:
![]() (7.7)
(7.7)
В отличие от рассмотренного случая нормального горения, в реальных условиях взрывов в замкнутом пространстве процесс дефлаграционного горе-ния самоускоряется. Это связано с расширением поверхности горения, воз-никновением движения газов и повышением давления при горении.
2.ЛАБОРАТОРНЫЕ И ПРАКТИЧЕСКИЕ РАБОТЫ.
Лабораторная работа 1.
Правила ТБ в лаборатории. Ознакомление с посудой и приборами.
Цель: познакомиться с правилами техники безопасности при работе в кабинете химии, лабораторным оборудованием и приёмами обращения с ним
Ход работы
Правила техники безопасности при работе в кабинете химии
1) Познакомьтесь с правилами техники безопасности, которые необходимо соблюдать при выполнении лабораторных и практических работ в кабинете химии.
2) Изучите краткую инструкцию по оказанию мер первой медицинской помощи при различного рода отравлениях и поражениях организма.
Изучите информацию о группах лабораторного оборудования.
Можно выделить несколько групп лабораторного оборудования:
I группа - стеклянная посуда
II группа - фарфоровая посуда
III группа - нагревательные приборы
IV группа - приборы для фиксации и закрепления посуды
Стеклянная посуда может быть сделана из толстого (нетермостойкого) стекла и, соответственно, из термостойкого стекла (тонкостенного).
Посуда из термостойкого стекла используется для проведения операций, сопровождающихся изменением температуры (нагревание, охлаждение).
Посуда из толстого стекла предназначена для хранения реактивов или проведения простейших операций, не сопровождающихся изменением температуры.
2) Ознакомьтесь с назначением лабораторного оборудования
Пробирки | Используются для проведения опытов и монтажа приборов
| |
Химические стаканы | Служит для проведения простейших операций | |
Колба плоскодонная (нетермостойкое стекло) | Используется для проведения химических реакций при комнатной температуре или для хранения реактивов | |
Колба круглодонная (из термостойкого стекла) | Используется для проведения разнообразных химических реакций при нагревании | |
Воронка | Для разнообразных целей, например, переливания жидкости из одного сосуда в другой, фильтрования | |
Стеклянная палочка | Для разнообразных химических целей, например перемешивание веществ в стакане | |
Шпатель | Используется для насыпания твердых веществ | |
Пробиркодержатель | Используется для удержания пробирок | |
Тигельные щипцы | Используется для переноса тигля и фарфоровой чашки с веществами | |
Фарфоровая чашка | Применяется для выпаривания жидкостей | |
Тигель | Предназначен для нагревания и прокаливания твердых веществ | |
Ложечка для сжигания | Предназначена для сжигания твердых веществ | |
Фарфоровая ступка с пестиком | Служит для размельчения и растирания твердых веществ | |
Мерный цилиндр | Используется для измерения объема жидкости | |
Ареометр | Предназначен для измерения плотности растворов | |
Термометр | Предназначен для измерения температуры реакционной смеси или температуры кипения и плавления | |
Делительная воронка | Используется для разделения двух несмешивающихся жидкостей или для прикапывания раствора какого-либо вещества | |
Химическая пипетка | Служит для отбора пробы жидких веществ (Прибор для взятия определенного объема жидкости) | |
Штатив для пробирок | Служит для закрепления пробирок при проведение опытов | |
Мерная колба | Служит для приготовления растворов определенной концентрации | |
Чашка Петри | Используется для высушивания различных веществ |
4) Оформите отчёт
Сделайте общий вывод по проделанной работе, исходя из цели урока.
Лабораторная работа 2.
Разложение пероксида водорода в присутствии диоксида марганца MnO2.
Цель работы: Определить среднее значение константы скорости реакции.
Описание работы:
Перед началом опыта необходимо подготовить катализатор: небольшой кусочек стеклянной палочки смазать клеем БФ или крахмальным клейстером. Необходимо смазать клеем только торец, немного порошка MnO2 насыпать на часовое стекло, прикоснуться торцом палочки к порошку, чтобы небольшое количество MnO2 осталось на стекле. Клей Высушивают в течение нескольких минут (1-2 мин). Давление внутри системы для сбора Н2О2 необходимо привести к атмосферному: открыть пробку реакционной пробирки, с помощью уравнительной склянки установит уровень воды в бюретке на нулевую отметку.
Схема прибора для измерения скорости разложения Н2О2 представлена рис.1.
уравнительн. склянка
вода
пробирка с Н2О2
катализатор
Рис.1 – Прибор для изучения кинетики разложения Н2О2.
Пипеткой или мерным цилиндром отмеряют 2 мл 3 %-ного раствора Н2О2, выливают в пробирку 1. Если опыт проводится при комнатной температуре, готовят секундомер, таблицу для записи опытных данных, Опускают в пробирку катализатор, нанесенный на кусочек стеклянной палочки. Закрывают реакционный сосуд пробкой. Записывают объем выделяющегося кислорода сначала через 30 сек, затем интервал можно увеличить до 1 мин.
По мере понижения уровня жидкости в бюретке уравнительную склянку опускают так, чтобы уровень жидкости в бюретке и склянке не изменялся, разность уровней была минимальной.
Реакция считается законченной, если уровень жидкости в бюретке перестает опускаться.
Объем кислорода, соответствующий полному разложению Н2О2 –V?, можно получить, если реакционный сосуд поместить в стакан с горячей водой. После охлаждения пробирки до комнатной температуры. После определяют объем О2, соответствующий полному разложению Н2О2.
Таблица – Экспериментальные данные
№ п/п | Время от начала опыта ?, мин | Объем кислорода V?, мл | V? –V?, мл | ln(V–V?) | ln | k, мин -1 |
По результатам эксперимента вычисляют среднее значение константы скорости реакции.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |




