Различают два типа цепных реакций: с неразветвленными и разветвленными цепями. Примером первого типа реакций может служить реакция образования хлороводорода из водорода и хлора
Н2 + Сl2 > 2НСl,
схема механизма которой была предложена Нернстом.
В схеме можно выделить три группы реакций. Начинается процесс с реакции зарождения цепи:
Cl2 > Cl + Cl
Эта реакция диссоциации молекулы хлора на атомы может происходить при поглощении света
Cl2 + h? > Cl + Cl,
термическим путем – при столкновении, например, двух молекул хлора с повышенной энергией:
Cl2 + Cl2 > Cl + Cl + Cl2,
химическим путем – например, при взаимодействии молекулы хлора с атомом натрия, пары которого введены в систему. Образующиеся атомы хлора обладают высокой реакционной способностью и вступают в дальнейшее взаимодействие с исходными веществами, протекает вторая группа реакций – развитие цепи:
Cl + H2 > HCl + H
H + Cl2 > HCl + Cl
В результате первой реакции появляется атом водорода, который легко вступает во взаимодействие молекулой хлора, в результате чего образуется хлороводород и регенерируется атом хлора, который дает начало следующему звену:
Cl + H2 > HCl + H
H + Cl2 > HCl + Cl
и так далее. В результате возникают последовательно идущие один за другим циклы – развивается цепь реакций
Cl > H > Cl > H > Cl > ...
При благоприятных условиях такая цепь может состоять из многих тысяч звеньев. В результате на одну первоначально активированную молекулу хлора образуется не две молекулы HCl, как при обычной бимолекулярной реакции, а тысячи и десятки тысяч молекул.
Для приведенной реакции характерным является то, что на одну вступающую в реакцию активную частицу Сl или Н вновь образуется одна активная частица. Такие цепи и называют неразветвленными.
Кроме приведенных реакций зарождения и развития цепи в системе протекает третья группа реакций – реакции обрыва цепи, приводящие к гибели активных частиц при соударении с какой-либо третьей частицей М или стенкой сосуда S:
Н + Н + М > Н2 + М
Н + Н + S > Н2 + S
Cl + Cl + M(S) > Cl2 + M(S)
Н + Cl + M(S) > HCl + M(S)
В присутствии, например, кислорода обрыв цепи может происходить в результате реакции
Н + О2 + М > ![]() + М
+ М
Образующийся малоактивный радикал ![]() гибнет на стенках сосуда или по реакции
гибнет на стенках сосуда или по реакции
![]() + Н > Н2 + О2
+ Н > Н2 + О2
При низких давлениях активные центры гибнут в основном на стенках сосуда, а при высоких давлениях происходит тримолекулярный обрыв в объеме. Поэтому для цепных реакций и характерны особенности, о которых говорилось выше – зависимость скорости реакции от величины удельной поверхности сосуда, от присутствия какого-либо инертного вещества, от давления или концентрации реагирующих веществ.
Кинетическое уравнение неразветвленной цепной реакции можно получить, исходя из механизма реакции. Например, детальное изучение реакции между водородом и бромом
Н2 + Br2 > 2HBr
показало, что реакция проходит в несколько элементарных стадий с разными константами скорости k:
Br2 > Br + Br k1
Br + H2 > HBr + H k2
H + Br2 > HBr + Br k3
H + HBr > H2 + Br k4
Br + Br > Br2 k5
Исходя из этой схемы, скорость образования бромистого водорода можно представить уравнением:
![]()
![]() +
+ ![]() –
– ![]() . (22.1)
. (22.1)
Рассматривая атомы брома и водорода как промежуточные продукты, можно применить к ним принцип стационарных концентраций Боденштейна (см. разд. 20.6):
![]() . (22.2)
. (22.2)
![]() . (22.3)
. (22.3)
Из суммы этих равновесий находим концентрацию атомов брома:
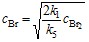 . (22.4)
. (22.4)
После подстановки этой концентрации в уравнение (22.3) получим концентрацию атомов водорода:
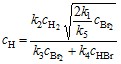 . (22.5)
. (22.5)
Подстановка концентраций атомов брома и водорода в уравнение (22.1) дает окончательное уравнение для скорости реакции:
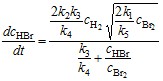 . (22.6)
. (22.6)
Это уравнение совпадает с уравнением (20.6), полученным по экспериментальным данным.
В ряде реакций в результате одного элементарного акта может возникать не одна, а две или больше химически активных частиц, т. е. происходит разветвление цепи. Такие реакции получили название разветвленных цепных реакций. В таких реакциях в начальный период времени число активных частиц, а следовательно, и скорость реакции лавинообразно нарастают вплоть до того момента, когда из-за израсходования исходного вещества скорость реакции начинает уменьшаться. Примером таких процессов может служить реакция окисления водорода, механизм которой по современным представлениям можно представить совокупностью последовательно протекающих элементарных химических актов:
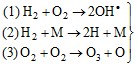 Зарождение цепи
Зарождение цепи
(4) ![]() + Н2 > Н2О + Н Продолжение цепи
+ Н2 > Н2О + Н Продолжение цепи
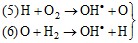 Разветвление цепи
Разветвление цепи
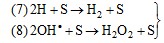 Обрыв цепи на стенке
Обрыв цепи на стенке
(9) Н + О2 + М > ![]() + М Обрыв цепи в объеме
+ М Обрыв цепи в объеме
Образующиеся малоактивные радикалы ![]() могут распадаться на стенке:
могут распадаться на стенке:
2![]() + S > Н2О2 + О2 + S
+ S > Н2О2 + О2 + S
При больших давлениях возможны реакции в объеме:
(10) ![]() + Н2 > Н2О2 + Н Продолжение цепи через
+ Н2 > Н2О2 + Н Продолжение цепи через
(11) ![]() + Н2О > Н2О2 +
+ Н2О > Н2О2 + ![]() малоактивний радикал
малоактивний радикал
Если разветвление цепи осуществляется часто, то даже одна первоначально возникшая цепь может привести к развитию многих цепей. В предельном случае можно представить, что разветвление происходит в каждом звене, и тогда говорят о сплошь разветвленной цепной реакции. В других случаях разветвление может происходить более редко.
Существование нижнего и верхнего пределов воспламенения качественно можно объяснить следующим образом. При давлениях, меньших нижнего предела, активные частицы легко диффундируют к стенкам сосуда, где происходит их гибель. Обрыв цепей на стенках преобладает над разветвлением, и быстрая реакция не развивается. При повышении давления диффузия к стенкам затрудняется, а возрастает число двойных соударений типа (5) и (6), которые ведут к разветвлению цепей; зарождение и разветвление цепей начинают преобладать над обрывом. В результате реакция самоускоряется и может закончиться самовоспламенением или взрывом, что и происходит внутри полуострова воспламенения.
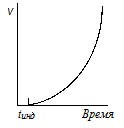
Рис. 22.2. Зависимость
скорости разветвленной цепной реакции от времени внутри полуострова
воспламенения
При дальнейшем повышении давления все более вероятными становятся тройные соударения в объеме, приводящие к обрыву цепей. Если давление превышает значение верхнего предела II (рисунок 22.1), обрыв начинает преобладать над развитием цепей и возможность быстрого протекания реакции исчезает.
Воспламенению горючей смеси внутри полуострова воспламенения предшествует индукционный период tинд (рис. 22.2). Он объясняется тем, что сначала число цепей может быть очень малым и практически реакция незаметна из-за недостаточной чувствительности методов анализа. Но по истечении некоторого времени tинд число цепей очень быстро нарастает вследствие их размножения и наступает самовоспламенение или взрыв. Зависимость скорости реакции v от времени t можно представить уравнением:
![]() , (22.7)
, (22.7)
где A и ? – постоянные для данной реакции и зависящие от ряда условий. При выводе этой зависимости не учитывалось уменьшение концентрации реагирующих веществ вследствие выгорания, поэтому стремление скорости к бесконечности с течением времени не имеет физического смысла – скорость становится большой, но не бесконечной.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |




