Еще в начале XIX века было установлено, что химически активны лишь те лучи, которые поглощаются реагирующими веществами (закон Гротгуса – Дрепера, который иногда называют I законом фотохимии). Поглощение монохроматического света с длиной волны ? описывается законом Ламберта – Бера: ослабление интенсивности dI света, прошедшего через слой толщиной dx, прямо пропорционально толщине слоя, интенсивности падающего света I и числу поглощающих частиц n (или их концентрации в слое):
– dI = kIdx (23.1)
где коэффициент пропорциональности k – молекулярный коэффициент поглощения, который является мерой поглощательной способности молекулы для данной длины волны и в первом приближении не зависит от концентрации. После интегрирования в пределах x от 0 до l (l - общая толщина поглощающего слоя) и I от Io (интенсивность падающего света) до I (интенсивность выходящего света) получим выражение закона Ламберта – Бера:
![]() . (23.2)
. (23.2)
Если концентрацию выражать числом молей вещества в литре раствора (c), то
![]() , (23.3)
, (23.3)
где ? – молярный коэффициент поглощения, связанный с k соотношением kn = ? c.
Бунзен и Роско (1855) установили, что химическое действие света прямо пропорционально произведению интенсивности света на время его действия. Эта зависимость является приближенной, так как отмечалось выше, не вся поглощенная световая энергия всегда полностью расходуется на химический процесс.
Обобщение всех закономерностей было сделано Вант-Гоффом (1904), который сформулировал количественную закономерность, лежащую в основе кинетики фотохимических реакций: количество фотохимически измененного вещества пропорционально поглощенной энергии света. Математическое выражение этой формулировки можно получить следующим образом. Количество световой энергии A, поглощенной в единицу времени фотохимической системой, равно по закону Ламберта – Бера
![]() , (23.4)
, (23.4)
а количество фотохимически измененного вещества dc в единицу времени, т. е. скорость реакции, пропорциональна A:
![]()
![]() . (23.5)
. (23.5)
Если концентрация очень мала или поглощающий слой очень тонкий (l = dx, величина cl мала), то после разложения экспоненты в ряд получим
![]() , (23.6)
, (23.6)
т. е. фотохимическая реакция протекает по первому порядку, ее скорость пропорциональна концентрации реагирующего вещества.
При больших концентрациях или толстом поглощающем слое (cl велико, ![]() << 1) весь световой поток поглощается и
<< 1) весь световой поток поглощается и
![]() , (23.7)
, (23.7)
т. е. скорость реакции постоянна и не зависит от концентрации реагирующего вещества (нулевой порядок).
Число квантов света, поглощенных в единицу времени nh? =A/h?, следовательно, за это время изменению должны подвергнуться np = A/h? молекул. Но, как показывает опыт, очень часто число фотохимически прореагировавших молекул не равно числу поглощенных квантов. В связи с этим для характеристики фотохимических процессов введено понятие квантового выхода ?. Квантовым выходом называется отношение числа химически прореагировавших молекул к числу поглощенных квантов:
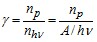 . (23.8)
. (23.8)
Тогда скорость химической реакции
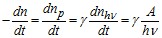 , (23.9)
, (23.9)
или с учетом уравнения (23.4)
![]() . (23.10)
. (23.10)
Это уравнение объединяет все законы фотохимии и представляет собой общее выражение для скорости фотохимической реакции.
Основные типы фотохимических процессов
В зависимости от величины квантового выхода все фотохимические реакции можно подразделить на четыре группы: 1) с квантовым выходом ? = 1; 2) с квантовым выходом ? < 1; 3) с квантовым выходом ? > 1; 4) с квантовым выходом ? >> 1. Примеры некоторых реакций различных групп приведены в таблице 23.1. В уравнениях реакций первым указано вещество, поглощающее свет.
Отклонения квантового выхода от единицы связано с механизмом протекания фотохимической реакции, в которой можно выделить три основные стадии:
1) начальный акт поглощения света;
2) первичный фотохимический процесс;
3) вторичные реакции.
Начальное действие света состоит в образовании электронно-возбужденной молекулы А*:
А + h? > А*
Квантовый выход этого процесса в большинстве случаев равен единице. За начальным актом поглощения немедленно следуют первичные процессы превращения элекронно-возбужденной молекулы различного вида:
1. Флуоресценция А* > А + h?
2. Дезактивация при соударении А* + М > А + М
3. Спонтанная диссоциация А* > В1 + В2
4. Диссоциация при столкновении А* + М > В1 + В2 + М
5. Внутренняя перестройка А* > В
6. Реакции с другими молекулами А* + В > С
В результате процессов 1 – 2 возбужденная молекула дезактивируется и дальнейших превращений не происходит. В реакциях 5 – 6 образуются продукты и квантовый выход будет равен единице или меньше, если частично протекают также реакции 1 – 2.
В результате диссоциации в реакциях 3 – 4 могут образоваться как устойчивые, так и реакционно-способные молекулы, а также свободные радикалы и атомы. Именно свободные радикалы и атомы чаще всего образуются в результате диссоциации и, обладая высокой реакционной способностью, вступают во вторичные реакции различного типа.
Таблица 23.1
Характеристики некоторых фотохимических реакций
Реакция | Длина волны, нм | Квантовый выход |
O2 + H2 > H2O2 (газ) | 172 | 1 |
Br2 + C6H12 > C6H11Br + HBr (газ) | 470 | 1 |
Cl2 + 2CCl3Br > 2CCl4 + Br2 | 470 | 1 |
2NH3 > N2 + 3H2 (газ) | 200 – 220 | 0,15 – 0,2 |
CH3Br > (CH4, Br2) (газ) | 254 | 4.10-3 |
С6Н6 + 3Br2 > С6H6Br6 (р-р в С6H6) | 300 – 550 | 0,4 – 0,9 |
2HBr > H2 + Br2 (газ) | 207 – 254 | 2 |
Cl2 + SO2 > SO2Cl2 (газ) | 420 | 2 – 3 |
2HClO > 2HCl + O2 (р-р в воде) | 366 – 436 | 2 |
Cl2 + CO > COCl2 (газ) | 400 – 436 | 103 |
Cl2 + H2 > 2HCl (газ) | 303 – 500 | 104 – 106 |
2H2O2 > 2H2O + O2 (р-р в воде) | 275 – 366 | 20 – 500 |
Таблица 23.2
Вторичные реакции с участием активных частиц
Тип процесса | Уравнение реакции | Квантовый выход |
1. Рекомбинация | В1 + В2 > А + М | <1 |
2. Реакция с продуктом или другими молекулами с регенерацией А | В1 + В > А + С | <1 |
3. Нецепные реакции без участия А и без образования А | В1 + В2 > В + С | 1 |
4. Нецепные реакции с участием новых молекул А | В1 + А > В + С | 2 – 3 |
5. Цепные реакции без участия молекул А | В1 + В > D + В2 | >1 или >>1 |
6. Цепные реакции с участием молекул А | В1 + А > В + В2 | >1 или >>1 |
В таблице 23.2 представлены возможные вторичные процессы и зависимость квантового выхода от характера реакции (В1 и В2 – активные частицы, В, С, D – устойчивые молекулы, отличные от А).
Как следует из таблицы, большой квантовый выход характерен для тех фотохимических реакций, в которых могут протекать цепные процессы (разветвленные или неразветвленные). Малый квантовый выход свидетельствует о прохождении процессов рекомбинации или реакций с регенерацией молекул А. Если ? равно небольшому числу и слабо зависит от условий опыта, то вероятно, что происходит быстрая и полная диссоциация на устойчивые молекулы или радикалы, реагирующие только по процессам 3 и 4. Вообще же представление о механизме конкретной реакции составляется на основании зависимости квантового выхода от условий опыта: от концентрации или давления реагирующих веществ и присутствия инертных добавок; интенсивности светового потока; длины волны; температуры; размеров и материалов стенки сосуда.
Хемолюминесценция.Некоторые химические реакции сопровождаются излучением света. Это явление носит название хемилюминесценции. Возбуждение при этом не термическое; в пламени (в котором мож-но наблюдать характерное излучение, например, частиц Сг, СН и ОН) интенсивность излучения может быть гораздо выше значений, ожидаемых исходя из температуры пламени, а само излучение носит люминесцентный характер. Хорошо известно несколько естественных хемилюминесцентных явлений, среди которых свечение жуков-светляков, гниющей рыбы, многих бактерий, блуждающие огоньки.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |




