Лекция №2.
Гомолитические реакции.
План:
Гомолитические реакции. Мономолекулярный распад молекул на радикалы. Реакции замещения. Гомолитические реакции. Мономолекулярный распад молекул на радикалы.Гомолитические реакции (от греч. homos - равный, одинаковый, общий и lysis-разложение, распад), протекают с гемолизом хим. связи, т. е. с таким ее разрывом, при котором электронная пара, осуществляющая связь, разделяется между образующимися фрагментами (своб. радикалами):
![]()
Иногда к гомологическим относят все р-ции, протекающие с участием и образованием своб. радикалов или ион-радикалов.
Для осуществления гомолитических реакций обычно используют термохимические, каталитические, фотохимические, радиационно-химические и электрохимические методы. Возможность реализации реакции определяется энергией диссоциации связи. В газовой фазе гомолиз протекает значительно легче, чем гетеролиз.
По гомолитическому механизму протекают многие цепные реакции, например фотогалогенирование предельных углеводородов (металепсия), радикальная полимеризация, нитрование алифатических соединений.
Радикальные реакции, осуществляются с участием радикального центра свобных радикалов. Характеризуются, как правило, большими значениями предэкспоненц. множителя в уравнениинии Аррениуса и малыми энергиями активации Е. Включают по крайней мере две стадии - образование своб. радикалов и их гибель. Образование своб. радикалов происходит вследствие разрыва хим. связи, при котором на обоих фрагментах молекулы или на одном из них остается по одному неспаренному электрону, напр.:
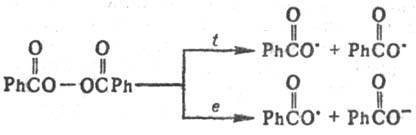
Эта реакция может быть индуцирована нагреванием, облучением, действием восстановителей или др. путями.
Радикалы обладают различной реакционной способностью, зависящей от их природы, типа реакций, полярного и стерического факторов, эффекта растворителя.
Реакции между свободными радикалами. Осуществляются при взаимодействии двух одинаковых или различных радикалов с образованием новой хим. связи (рекомбинация). Реакция обычно диффузионно контролируемая; Е от 0 до 5 кДж/моль. Происходит, напр., при дегидродимеризации орг. соедине-ний под действием пероксидов или др. окислителей, напр.:
![]()
![]()
Другой пример рекомбинации свободных радикалов - электрохим. анодный синтез углеводородов (реакции Кольбе ):
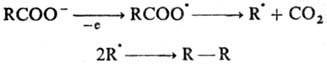
Рекомбинация в - катодном процессе может происходить при электрохим. восстановлении, напр., карбонильных соед.:
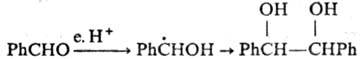
При близком расположении двух своб. радикалов в "клетке" р-рителя (напр., генерируемых при термораспаде пероксидов или диазосоединений) р-ция осуществляется с высокой селективностью (см. Клетки эффект). Влияние этого эффекта уменьшается с увеличением т-ры и понижением вязкости р-рителя.
При взаимод. двух радикалов возможно также диспропор-ционирование - перенос атома Н (реже-атома галогена) от одного радикала к другому, напр.:
![]()
Диспропорционирование, как правило, более медленный процесс, чем рекомбинация. Обе р-ции экзотермичны и нередко идут одновременно.
Реакции свободных радикалов с молекулами. Характерны для таких практически важных процессов, как хлорирование, бромирование, сульфохлорированис, автоокисление, полимеризация и др., протекающих по цепному механизму (см. Цепные реакции). Их константы скорости на неск. порядков ниже, чем для рекомбинации; Е = 20-60 кДж/моль. Так, р-ция автоокисления осуществляется в результате многократно повторяющихся р-ций по схеме:
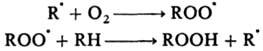
Обрыв цепи происходит путем рекомбинации![]() с
с![]() или с ROO•. Для торможения автоокислит. процессов используют ингибиторы, обычно пространственно-затрудненные фенолы или ароматич. амины. Радикалы, взаимодействуя с ингибиторами, образуют неактивные феноксильные или аминильные радикалы, к-рые не способны участвовать в стадиях роста цепи. Стереохимия р-ции зависит от характера субстрата. Обычно образующийся радикал с неспаренным электроном у хирального атома С имеет плоскую или близкую к плоской конфигурацию, что приводит к рацемизации. В циклич. системах инверсия радикального центра затруднена, особенно в случае малых циклов.
или с ROO•. Для торможения автоокислит. процессов используют ингибиторы, обычно пространственно-затрудненные фенолы или ароматич. амины. Радикалы, взаимодействуя с ингибиторами, образуют неактивные феноксильные или аминильные радикалы, к-рые не способны участвовать в стадиях роста цепи. Стереохимия р-ции зависит от характера субстрата. Обычно образующийся радикал с неспаренным электроном у хирального атома С имеет плоскую или близкую к плоской конфигурацию, что приводит к рацемизации. В циклич. системах инверсия радикального центра затруднена, особенно в случае малых циклов.
2. Реакции замещения
Реакции замещения (англ. substitution reaction) — химические реакции, в которых одни функциональные группы, входящие в состав химического соединения, меняются на другие группы. Реакции замещения обозначают английской буквой «S».
Общий вид реакций замещения:
![]()
Обычно, один из реагентов, в котором происходит замещение («R-X»), называют субстратом, а другой («Y-Z») — атакующим реагентом. Группа «X» называется уходящей, а группа «Y» — вступающей[1].
Примером реакции замещения может служить фотолитическое хлорирование метана:
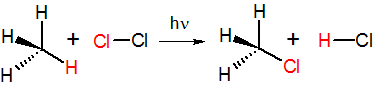
В зависимости от способа расщепления связи, реакции замещения делятся на гомолитические (радикальные) и гетеролитические. Последние, в свою очередь, из-за типа атакующего реагента относят к нуклеофильным или электрофильным реакциям.
В органической химии реакции замещения имеют важнейшее значение. Детальное изучение типового механизма реакции позволяет не просто предсказать её результат для конкретных реагентов, но и получить представление о выборе оптимальных температурных условий её протекания, подборе растворителя или возможного катализатора.
Реакции нуклеофильного замещения
В реакциях нуклеофильного замещения атакующей частицей является нуклеофил, то есть отрицательно заряженная частица или частица со свободной электронной парой. Уходящая группа носит название нуклеофуг.
Реакции нуклеофильного замещения более характерны для алифатических систем.
Общий вид реакций нуклеофильного замещения:
![]()
Реакции нуклеофильного замещения обозначаются «SN». Обычно, разделяют реакции алифатического (SN) и ароматического (SNAr) нуклеофильного замещения.
Наиболее распространено два типа механизмов реакций нуклеофильного замещения:
SN1 — мономолекулярное нуклеофильное замещение: двухстадийный процесс — на первой (медленной) стадии образуется промежуточный карбкатион, который на второй (быстрой) стадии реагирует с нуклеофилом.
SN2 — бимолекулярное нуклеофильное замещение: одностадийный процесс без образования интермедиата.
Примером реакции нуклеофильного замещения может служить гидролиз алкилгалогенидов:
![]()
Наиболее распространенные нуклеофильные группы[4]:
![]()
![]()
Реакции электрофильного замещения
В реакциях электрофильного замещения атакующей частицей является электрофил, то есть положительно заряженная частица или частица с дефицитом электронов. Уходящая частица носит название электрофуг.
Реакции электрофильного замещения более характерны для ароматических систем.
Общий вид реакций электрофильного замещения:
![]()
Реакции электрофильного замещения обозначаются «SE».
Для ароматических систем существует только один (основной) механизм электрофильного замещения SEAr, который включает в себя образование промежуточного положительно заряженного интермедиата, у которого на второй стадии отщепляется уходящая группа[3].
У алифатических соединений встречаются как механизмы SE1, так и SE2, аналогичные механизмам SN1 и SN2.
Пример реакции электрофильного замещения:

Наиболее распространенные электрофильные группы:
![]()
Реакции радикального замещения
В реакция радикального замещения атакующей частицей являются свободные радикалы.
Общий вид реакций радикального замещения:
![]()
Реакции радикального замещения обозначаются «SR».
Примером реакции радикального замещения может служить приведенная выше реакция хлорирования метана.
Основные понятия, которые необходимо знать:
Мономолекулярные реакции
Гомолитический реакции
Гетеролитические реакции
Константа мономолекулярной реакции
Реакция диспропорционирования
Нуклеофильное замещение
Электрофильное замещение.
Вопросы для самоконтроля:
Что называют гомолитическими реакциями? Характеристика взаимодействий радикалов с атомами и молекулами Механизм электрофильного замещения.Литература:
1. Курс физической химии. М.:Химия,1975.725с..
2. Физическая химия М.: Высшая школа, 1999. -496с..
Лекция №3.
Модуль 2.Химия высоких энергий. Цепные реакции.
Фотохимия.
План:
1.Кинетика фотохимических реакций.
2. Хемилюминесценция.
Кинетика фотохимических реакций.Под фотохимическими обычно понимают реакции, прохождение которых обусловлено действием света – излучением с частотами видимого спектра или близкими к ним.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |




