Кроме квазинейтральности, плазменное состояние характеризуется еще двумя свойствами: 1) электростатическим коллективным взаимодействием заряженных частиц (в достаточно разреженном газе при нормальных условиях происходит взаимодействие только двух частиц); 2) сильной зависимостью параметров плазмы от электрических и магнитных полей.
В плазменном состоянии могут находиться газы (газовая плазма, которая здесь и будет в основном рассматриваться) и твердые тела полупроводникового типа (плазма твердых тел), где в качестве свободных заряженных частиц выступают электроны и дырки. Различают полностью ионизованную плазму и частично ионизованную (слабоионизованную) плазму, называемую обычно «низкотемпературной».
В лабораторных и производственных условиях низкотемпературную плазму получают с помощью специальных аппаратов— плазмотронов.
В научно-технической литературе часто можно встретить термины «равновесная и неравновесная», «высокотемпературная и низкотемпературная», «горячая и холодная» плазма. В последние два термина в явном или неявном виде входит понятие температуры. В статистической физике температура определяется для системы, вероятность нахождения которой в состоянии с энергией Е пропорциональна ехр(—?Е), где ? = = 1/kT, a k — постоянная Больцмана. Только для таких систем можно говорить об одной и только одной температуре.
В плазме молекулярных газов может быть также затруднен обмен энергией между различными степенями свободы молекул. Поэтому при некоторых условиях плазма может описываться не одной, а несколькими температурами: электронной, колебательной, вращательной и поступательной.
В плазме, образованной ударной волной в сильном электрическом и магнитном полях, а также в плазме молекулярных газов, в которой существенную роль играет возбуждение внутренних степеней свободы молекул, может не быть даже и частичного равновесия. Тогда не имеет смысла ни одна из названных температур. Такую плазму следует характеризовать функциями распределения соответствующих частиц по энергиям либо их средними энергиями.
Неравновесной плазмой называют плазму, характеризующуюся неравновесными концентрациями и/или различными энергиями (температурами) компонентов, либо плазму, в которой имеет место частичное равновесие.
Кинетика плазмохимических процессов, как неравновесных, так и квазиравновесных, является одним из частных случаев неравновесной химической кинетики. При рассмотрении плазмохимической кинетики необходимо пользоваться методами математического моделирования.
В плазме электроны и нейтральные частицы, электроны и ионы обмениваются энергией. Обмен энергией электронов и ионов происходит в результате кулоновских соударений. Эти процессы могут привести к химическим реакциям: одной из задач плазмохимической кинетики и является исследование механизма и вероятности этих реакций.
Механизмы плазмохимических реакций
Присутствие заряженных и возбужденных частиц в слабоиони-зованной плазме, реакции с их участием являются одной из главных особенностей механизмов и кинетики химических реакций в ней. Образование и гибель этих частиц происходит в процессах возбуждения, диссоциации, ионизации, дезактивации и рекомбинации
Диссоциативное прилипание электронов к молекулам
Диссоциация молекул может происходить и в результате образования нестабильного отрицательного молекулярного иона при прилипании медленных электронов к молекулам по схеме
![]()
где в скобках условно обозначена совокупность квантовых чисел, характеризующих внутреннее состояние молекул и атомов.
В низкотемпературной плазме при этом процессе образуется, как правило, ион в основном состоянии.
Максимальные значения сечений этого процесса составляют ~10-14 см2 для Н2 при Е=10 эВ и -~10-23 см2 для D2 при ?Е = 3,75 эВ. Сечения и коэффициенты скорости могут по-разному зависеть от температур в зависимости от формы потенциальных кривых молекул и отрицательных ионов. Однако если молекула является малой добавкой к газу, у которого потенциал ионизации больше потенциала ионизации молекулы, основным каналом в процессе диссоциации могут быть ионно-молекулярные реакции.
Рекомбинация тяжелых незаряженных частиц с образованием молекул.
Процессом, обратным диссоциации, является рекомбинация. Она может протекать в газовой среде (гомогенная рекомбинация) и на поверхности твердых или жидких тел (гетерогенная рекомбинация). Экспериментально установлено, что при гомогенной рекомбинации образуются электронно-возбужденные молекулы. Она играет важную роль при средних и больших давлениях. Гетерогенная рекомбинация важна в низкотемпературной плазме пониженного давления. Она происходит при столкновениях атомов из газовой фазы с адсорбированными на поверхности; ее скорость зависит от количества свободных центров адсорбции.
Диссоциативная рекомбинация молекулярных ионов с электронами
Основным процессом нейтрализации заряженных частиц в плазме, состоящей из молекулярных газов, является диссоциативная рекомбинация молекулярных ионов с электронами
![]()
Выделяющаяся в результате рекомбинации энергия идет частично на возбуждение частиц и частично увеличивает их кинетическую энергию. Этот процесс существен и в плазме атомных газов, поскольку в них при относительно низких температурах газа также образуются молекулярные ионы и даже сложные комплексные ионы — кластеры. Последние эффективно образуются и в молекулярной плазме по реакции
![]()
Коэффициенты скорости диссоциативной рекомбинации велики (10-5—Ю-8 см3/с) и зависят от температуры электронов и газа. Эти процессы также вызывают отклонения от ионизационного равновесия - в низкотемпературной плазме.
Основные понятия, которые необходимо знать:
Искровой разряд
Тлеющий разряд
Плазма
Горячая плазма
Холодная плазма
Вопросы для самоконтроля:
1.Какое явление называют несамостоятельным разрядом?
2.Объясните возникновение темного разряда?
3.Механизмы плазмохимических реакций
Литература:
1. , , . Химия высоких энергий. М.:Химия, 1988. 368с.(глава6 с. 257-296)
2. Р. Уэйн. Основы и применения фотохимии. Изд.:Мир, 1991-304с.(глава 5 с.119-146)
Лекция №6.
Цепные реакции
План:
Основные понятия о цепных реакциях Механизм цепных реакций Элементарная теория цепных реакций1. Основные понятия о цепных реакциях
В ряде случаев в химических реакциях в качестве промежуточных продуктов выступают такие активные частицы как свободные атомы и радикалы, которые имеют свободные валентности и потому обладают высокой реакционной способностью. Эти частицы вступают в реакции, в результате которых вновь возникают свободные атомы и радикалы. Такая последовательность периодически повторяющихся реакций с участием активных частиц (свободных атомов и радикалов) называется цепной реакцией.
Хотя процесс образования свободных атомов или радикалов требует большой энергии активации, но их высокая реакционная способность и возникновение новых активных частиц при реакциях с насыщенными молекулами приводят к тому, что скорость цепных реакций оказывается обычно значительно выше скорости нецепных реакций. Зарождение в начале реакции небольшого количества реакционноспособных частиц приводит к превращению большого количества исходных веществ. Так как цепные реакции протекают циклически, то активная частица, возникающая в конце цикла, дает начало новому циклу, в конце которого происходит вновь регенерация активной частицы.
К цепным относятся реакции различных классов. По цепному механизму протекают, например, реакции горения или медленного окисления в газовой фазе:
2Н2 + О2 > 2Н2О
СН4 + 2О2 > СО2 + 2Н2О
К цепным относятся многие реакции с участием углеводородов (реакции полимеризации, разложения), фотохимические реакции (образование НСl, НВr, СОСl2 и др.), цепные ядерные реакции – распад урана-235 или плутония в ядерном реакторе или бомбе.
Характерной особенностью цепных реакций является большая чувствительность скорости этих реакций к наличию некоторых примесей. Например, тщательно высушенные водород и кислород реагируют между собой очень медленно, но реакция протекает с нормальной скоростью в присутствии незначительного количества паров воды. Смесь водорода с хлором не реагирует в темноте при комнатной температуре, но быстро реагирует при введении в систему малых количеств паров натрия. В других случаях присутствие примесей приводит к резкому снижению скорости реакции. Например, при фотохимическом инициировании реакции водорода с хлором скорость образования хлороводорода уменьшается примерно в тысячу раз в присутствии одного процента кислорода.
На скорость многих газовых реакций влияет форма и материал сосуда, в котором протекает реакция. Обычно реакции замедляются при увеличении отношения S/V (S – площадь поверхности сосуда, V – его объем). Это отношение практически можно изменять, вводя в сосуд осколки материала сосуда – стекла, кварца и т. п.
Для многих реакций окисления в газовой фазе характерно то, что быстрая реакция (самопроизвольное воспламенение) протекает лишь в определенных пределах давления и температуры. На рисунке 22.1 показана зависимость пределов воспламенения от давления и температуры, которая наблюдается при окислении водорода, паров фосфора, сероуглерода и др.
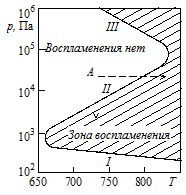
Рис. 22.1. Пределы воспламенения для реакции окисления водорода
Воспламенение смеси происходит только в условиях, соответствующих на рисунке заштрихованной площади, которая получила название полуострова воспламенения. Вне пределов полуострова воспламенения не происходит и реакция идет с малой скоростью или практически вовсе не происходит. Исходя из точки А, воспламенение можно вызвать нагреванием смеси или снижением давления смеси до значений, лежащих в области между кривыми II и I.
Объяснение указанных особенностей дает теория цепных реакций, начало развития которой относится к 1913 г., когда Боденштейном было введено понятие цепной реакции.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |




