В некоторых случаях наблюдается и третий предел воспламенения (рис. 22.1), лежащий при более высоких давлениях. Его существование связывают с протеканием цепных реакций за счет малоактивных радикалов или с развитием теплового взрыва.
2. Элементарная теория цепных реакций
Имеется два варианта теории цепных реакций – более строгий, основанный на решении системы дифференциальных уравнений, и менее строгий, но более наглядный вероятностный вариант, который и рассматривается далее.
Важной характеристикой цепной реакции является средняя длина цепи ? - среднее число элементарных реакций, вызываемых одной активной частицей (атомом или радикалом), возникшей первоначально каким-либо независимым путем. Если no – число таких независимо возникающих частиц в единицу времени в единице объема, то no можно назвать скоростью зарождения цепей.
Величина, обратная средней длине цепи, представляет собой вероятность обрыва цепи ?. Эту связь можно понять с помощью схематического изображения цепи на рисунке 22.3. На схеме точка означает появление и регенерацию активной частицы, а крестик – ее гибель, т. е. обрыв цепи.
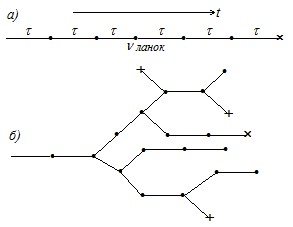
Рис. 22.3. Схематическое изображение цепной реакции:
а – неразветвленная цепь; б – разветвленная цепь
На один благоприятствующий случай – обрыв – приходится всего ? случаев, следовательно,
? =1/?. (22.8)
Допустим также возможность разветвления цепи – появление в каком-либо звене двух или более активных частиц и охарактеризуем такую возможность вероятностью разветвления цепи ?.
Обозначим через ? время, в течение которого в среднем протекает одно звено цепной реакции. Тогда произведение ?? равно среднему времени прохождения всей цепи от момента зарождения до обрыва. Концентрация активных частиц, т. е. их число в единице объема, пусть будет n. Скорость изменения концентрации этих частиц будет равна разности скоростей их образования no и исчезновения.
Если длина цепи ? = 1 (т. е. фактически цепь отсутствует), то активная частица гибнет в каждом звене. Тогда за среднее время развития одного звена ? прореагируют все n частиц, а скорость исчезновения будет равна n/? частиц/см3 с. Если же цепи развиваются и их средняя длина равна ? > 1, частица в среднем будет реагировать ? раз, а среднее время ее жизни будет равно ??. Следовательно, скорость уменьшения концентрации частиц выразится соотношением
![]() . (22.9)
. (22.9)
Если возможно разветвление цепи, т. е. ? > 0, то его влияние можно учесть, считая, что разветвление действует как бы в направлении, обратном обрыву, удлиняя цепь и уменьшая вероятность обрыва до величины (? – ?). Тогда для скорости изменения концентрации активных частиц можно записать выражение:
![]() . (22.10)
. (22.10)
Решение этого дифференциального уравнения можно провести следующим образом. Для простоты записи введем обозначение a = (? – ?)/?. Тогда
![]() . (22.11)
. (22.11)
Полагаем вначале, что no = 0, и после разделения переменных получаем:
![]() , (22.12)
, (22.12)
интегрирование которого дает:
lnn = –at + lnZ(t), (22.13)
где Z(t) – некоторая условная “постоянная” интегрирования. Тогда
n = Z(t)e–at. (22.14)
Продифференцируем это уравнение с учетом того, что Z не является постоянной величиной:
![]() . (22.15)
. (22.15)
Из сопоставления этого уравнения с уравнением (22.11) следует, что
![]() (22.16)
(22.16)
и
![]() . (22.17)
. (22.17)
После интегрирования этого уравнения получим
![]() , (22.18)
, (22.18)
где I – постоянная интегрирования. Подстановка этой величины в уравнение (22.15) дает
![]() . (22.19)
. (22.19)
Из условия, что в начальный момент реакции (t = 0) величина n = 0, следует, что
![]() (22.20)
(22.20)
и
![]() . (22.21)
. (22.21)
После подстановки значения a получим
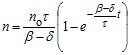 . (22.22)
. (22.22)
Скорость реакции v можно определить как скорость увеличения концентрации молекул продукта реакции. Так как в одном звене за время ? появляется одна молекула, то общее число молекул, образующихся в единице объема за единицу времени, равно n/?. Таким образом, мы получаем основное уравнение теории цепных реакций:
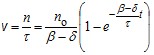 . (22.23)
. (22.23)
Рассмотрим использование этого уравнения для некоторых частных случаев.
При протекании неразветвленной цепной реакции ? = 0. Так как средняя длина цепи ? = 1/?, то скорость такой реакции
![]() . (22.24)
. (22.24)
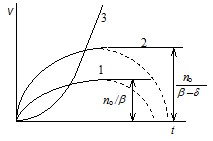 Рис. 22.4. Зависимость скорости
Рис. 22.4. Зависимость скорости
цепной реакции от времени:
1 – ? = 0; 2 – 0 < ? < ?; 3 – ? > ?
Как следует из этого уравнения, скорость реакции должна нарастать с течением времени и достигать предела, равного ?no = no/? (рис. 22.4), т. е. система должна достигать стационарного состояния, в котором скорость реакции постоянна. Эта скорость в ? раз больше скорости зарождения первичных реакционноактивных частиц no, т. е. скорости реакции в отсутствие цепей (? =1).
При возможности протекания разветвленной цепной реакции вероятность разветвления может оказаться меньше вероятности обрыва, т. е. 0 < ? < ?. В этом случае, согласно уравнению (22.23), система также должна достигать стационарной скорости, но эта скорость больше, чем в первом случае:
Если же вероятность разветвления больше вероятности обрыва, т. е. ? > ?, уравнение (22.23) принимает вид:
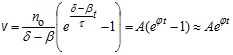 , (22.25)
, (22.25)
где A и ? являются положительными постоянными. Полученное уравнение совпадает с приведенным ранее уравнением (22.7). Уравнение показывает, что скорость реакции может стать бесконечно большой (рис. 22.4), т. е. свидетельствует о возможности развития цепного воспламенения или взрыва.
Следует, однако, отметить, что полученные зависимости относятся к некоторым идеализированным условиям протекания реакции – предполагается, что концентрации исходных веществ поддерживаются постоянными, а продукты реакции выводятся из реакционной зоны. В реальных условиях, например, при проведении реакции в замкнутом сосуде, происходит “выгорание” исходных веществ, а продукты остаются в реакционной смеси. Поэтому для неразветвленных цепных реакций или для разветленных реакций с ? < ? скорость проходит через максимум (пунктир на рис.22.4). Возможно, что стационарное состояние вообще не будет достигнуто, так как максимальная скорость может оказаться меньше стационарной. В случае разветвленной цепной реакции с
? > ? учет выгорания реагентов должен дать, как уже указывалось ранее, очень большую, но все же конечную скорость.
Условие ? > ? соответствует протеканию реакции в области полуострова воспламенения, а условие ? > ? – вне него. Таким образом, теория разветвленных цепных реакций количественно объясняет существование нижнего и верхнего пределов воспламенения.
К воспламенению или взрыву может также привести, независимо от механизма реакции, саморазогрев реагирующей смеси. По уравнению Аррениуса, скорость реакции увеличивается при повышении температуры по экспоненциальному закону, в то время как скорость теплоотвода – более медленно (пропорционально разности температур). В случае экзотермической реакции, если теплота не будет отводиться из реакционной зоны с достаточной скоростью, реакционная смесь начнет саморазогреваться, а скорость реакции все более возрастать. Развитие этих процессов может привести к воспламенению реакционной смеси или взрыву. В этом случае говорят о тепловом самовоспламенении (тепловом взрыве). Кинетика теплового самовоспламенения внешне может не отличаться от кинетики цепного воспламенения, что нужно иметь в виду при изучении реакций, переходящих в воспламенение или взрыв.
Основные понятия, которые необходимо знать:
Цепные реакции
Разветвленные цепи
Неразветвленные цепи
Вопросы для самоконтроля:
1.Объясните механизм цепных разветвленных реакций?
2.Перечислите основныестадии цепных реакций?
3. Основное уравнение теории цепных реакций?
Литература:
1. Курс физической химии. М.:Химия,1975.725с..
2. Физическая химия М.: Высшая школа, 1999. -496с.
Лекция №7.
Модуль 3. Физика и химия горения и взрыва. Предельные явления в химических процессах.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |




