Полагая, что порядок реакции первый, константу скорости реакции вычисляют по кинетическому уравнению первого порядка:
k = 1/?·ln![]()
По результатам эксперимента вычисляют среднее значение константы скорости реакции.
Период полураспада пероксида водорода вычисляют по уравнению:
?0,5 = 0,693/k, используя среднее значение константы скорости.
Определяют константу скорости и период полураспада графически, используя зависимость V?= f (?) и ln(V? – V?) = f (?), которые представлены на рис.2 и рис. 3. Сравнивают результаты, полученные двумя методами – аналитическим и графическим.
V, мл lg (V? – V? )
V?
?

?, мин? ?, мин
Рис. 2 –Зависимость V? = f(?) Рис.3 – Зависимость ln(V? – V?) = f(?)
Контрольные вопросы:
Общая характеристика катализаторов. Виды катализа. Зависимость скорости реакции от катализатора, температуры, концентрации Особенности кинетики каталитических процессов Теории гетерогенного катализа.Лабораторная работа 3
Фотометрическое изучение кинетики разложения
комплексного иона триоксалата марганца.
Цель работы: определение константы скорости и периода полураспада
реакции диссоциации комплексного иона триоксалата марганца (III) методом
абсорбционной фотометрии.
Сущность работы:
Реакция диссоциации комплексного иона триоксалата марганца (III)
протекает по уравнению:
[Mn(C2O4)3] 3 - = Mn2+ + 2,5 C2O43 - + CO2.
Данная реакция является реакцией первого порядка.
Поскольку исходное вещество окрашено в коричневый цвет, а продукты
распада бесцветны, для изучения кинетики реакции применяют
фотометрический метод.
Учитывая, что оптическая плотность прямо пропорциональна
концентрации раствора, уравнение можно записать следующим образом:
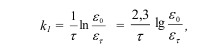
где ?0 – начальная оптическая плотность,
?? – оптическая плотность к моменту времени ?.
Ход работы.
Приготовить следующие исходные растворы:0,01М KMnO4; 0,1M
MnSO4 и 0,1M H2C2O4. Смешать растворы MnSO4 и H2C2O4 в соотношении
1:7. Прибавить к четыр?м частям бесцветной смеси одну часть раствора
KMnO4. Быстро образуется коричневая комплексная соль. Поместить е? в кювету и начать измерения оптической плотности с помощью
фотоколориметра с синим светофильтром, записывая показания через
каждые 2 мин. Закончить измерения, когда оптическая плотность снизится до
0,1. Данные занести в таблицу.
Таблица
Время в мин. | ?? | lg?? | k1 | kсредн. |
0 | ||||
2 | ||||
4 | ||||
и т. д. |
ОБРАБОТКА РЕЗУЛЬТАТОВ
1. Результаты оформить в виде таблицы 2. Вычислить k1 по уравнению (27)
для всех значений ?, а затем – среднее арифметическое полученных
констант (kсредн.).
2. Построить график в координатах ?? – ? и lg?? – ?, откладывая значения ? по
оси абсцисс. Преобразование формулы приводит к уравнению
прямой
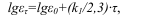
следовательно, второй график должен представлять собой прямую линию(рис1)
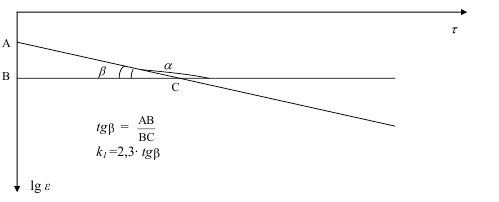
Рис. 1. Полулогарифмическая зависимость оптической плотности от
концентрации раствора.
Определить константу скорости реакции графическим методом, вычисливтангенс угла наклона ?, который есть константа скорости k1, деленная на
множитель 2,3. Сравните е? с kсредн. из таблицы 2.
4. Рассчитайте время полупревращения для данной реакции по уравнению 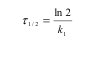
Контрольные вопросы:
1. Назовите основные узлы фотоэлектроколориметра.
2. Какие вещества можно анализировать методом фотоколориметрии? Что такое фотометрические реакции? 3. Спектры поглощения и их происхождение. Особенности молекулярных спектров поглощения.
5. Основные законы светопоглощения: закон Бугера – Ламберта – Бера и закон аддитивности. Условия выполнения закона Бугера – Ламберта – Бера и причины отклонения от него.
6. Спектральные приборы: устройство и принцип работы.
7. Условия и этапы фотометрических измерений.
8. Приемы установления неизвестной концентрации в фотоколориметрии.
Литература:
Курс физической химии, т.2 М:Химия.1973 Даниэльс, Р. Альберти Физическая химия. М:Высшая школа, 1967. Курс физической химии. Госхимиздат, М-Л.,1955. Гл. 14, с. 625-670.Лабораторная работа 4.
Измерение температуры термопарным методом, изготовление и калибровка термопар.
Цель работы: ознакомиться со способом измерения температуры при помощи термопары, произвести ее градуировку.
Методика эксперимента
В данной работе проводится градуировка медь-константановой термопары (константан - это сплав никеля и меди с добавкой марганца, отличающийся слабой зависимостью сопротивления от температуры). Термопара, проволоки которой изолированы в двухканальной фарфоровой трубке, прикреплена к дюралевой планке, в свою очередь укрепленной на штативе. Эдс термопары измеряется потенциометром (принцип работы потенциометра и его устройство изложены ниже).
В работе используются три реперные точки: 0°C, 100°C, 231,97°C. Реперная точка 0°C - это температура тающего льда (смеси льда с водой). Реперная точка 100°C - температура кипящей воды, точнее, паров над кипящей водой. Реперная точка 231,97°C - температура, при которой твердое олово плавится или жидкое олово отвердевает. Иначе, это температура олова, когда оно плавится, но еще не полностью расплавилось, или когда жидкое олово твердеет, но еще не полностью отвердело. Словом, температура плавления олова (как и всякого другого металла) - это температура, при которой олово находится, как говорят, в двухфазном состоянии - жидкое олово соседствует с твердым. Пока есть еще такое соседство, температура олова остается постоянной. Причина та же, из-за которой постоянна и равна 0°C температура тающего льда, когда лед тоже соседствует с жидкой водой - выделение теплоты при отвердевании и поглощении теплоты при плавлении кристалла.
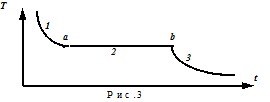
Чтобы измерить термоэдс термопары именно при температуре плавления (отвердевания) олова, снимают кривую охлаждения или кривую нагревания. Это график зависимости термоэдс от времени при охлаждении жидкого или при нагревании твердого олова. Это, в то же время, и график зависимости температуры от времени. Для олова, как и для любого другого кристаллического вещества, график имеет вид, показанный на рис.3, где представлена кривая охлаждения. Участок 1 представляет собой монотонное понижение температуры жидкого олова. Начиная с момента времени, соответствующего точке a, температура перестает понижаться, несмотря на то, что отвод тепла продолжается. Это и означает, что начался процесс отвердевания, который продолжается до момента времени, соответствующего точке b. Температура, соответствующая этой второй ветви кривой, то есть ее горизонтальному участку, и есть температура отвердевания олова. После этого температура, теперь уже твердого олова, снова монотонно уменьшается (ветвь 3). В случае олова, температура, соответствующая горизонтальному участку, равна 231,97°C. Это одна из реперных точек МПТШ-68.
Эдс термопары измеряется потенциометром - прибором, который реализует компенсационный метод измерения эдс. Как известно, электродвижущая сила любого источника тока равна разности потенциалов на концах (полюсах) разомкнутого источника тока. Но можно измерить эдс и в том случае, когда источник включен в замкнутую цепь. При этом ток через источник должен быть равен нулю, что возможно лишь, если в электрическую цепь помимо источника, эдс которого должна быть измерена, включен другой, вспомогательный источник, и включен так, чтобы ток от него был направлен против тока от измеряемого источника эдс и компенсировал его. Именно таким, компенсационным методом, всегда и измеряют электродвижущую силу.
Компенсация токов осуществляется с помощью, так называемой, потенциометрической схемы. Она представляет собой сопротивление R (обычно большое), на которое замкнут источник тока Е (см. рис.4). (В простейшем варианте сопротивление R может быть просто длинной проволокой).
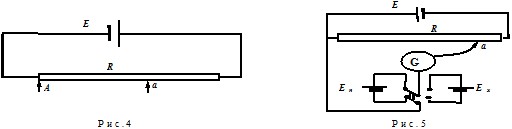
Если снабдить эту схему подвижным контактом, скользящим вдоль R, то между ним и одним из концов, например A, можно получить любую часть разности потенциалов на концах R. Поэтому описанное устройство называется также делителем напряжения: оно позволяет делить Е на части. Можно выделить и такую часть, чтобы ею скомпенсировать эдс измеряемого источника. Нужно только, чтобы эдс вспомогательного источника, включаемого в схему потенциометра, была больше измеряемой, т. к. для компенсации используется часть эдс вспомогательного источника.
На применении потенциометра основан компенсационный метод измерения эдс. Сущность метода поясняет рис.5. На этой схеме Е - вспомогательный источник, включаемый в цепь потенциометра, а Ех - источник тока, эдс которого нужно измерить. В цепь этого источника включен гальванометр G, присоединяемый к потенциометру подвижным контактом a. Источник тока En - это источник тока с хорошо и точно известным значением эдс. Называется он нормальным элементом Вестона. Эдс его известна с точностью до 5-го знака после запятой и отличается большим постоянством. Это как бы эталон эдс. Значение эдс нормального элемента при 20°C лежит в пределах 1,01850 - 1,01870В. Последние два знака определяются по паспортным данным элемента с учетом температуры окружающей среды. Первые три знака гарантированы у каждого исправного элемента.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |




