Во втором варианте центральное внимание уделяется только первому компоненту каталитической системы, а второй компонент выполняет лишь вспомагательную роль. Монометаллический механизм основан на октаэдрической конфигурации атома Ti, которая получается из исходной тетраэдрической конфигурации при взаимодействии Tiс алкилалюминием. В результате атом Tiв кристаллической решетке располагается в центре правильного октаэдра и имеет одну вакантную d-орбиталь, расположенную в одной из вершин октаэдра.
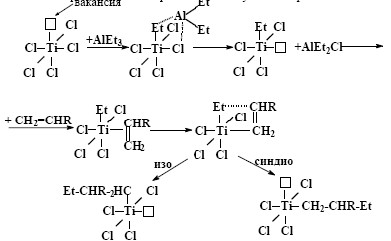
Схема монометаллического механизма роста цепи на катализаторе Циглера-Натта.
В соответствии с этим механизмом координация мономера приводит к переходному комплексу из четырех атомов, включая алкильную группировку. Затем переходный комплекс быстро перестраивается за счет внедрения молекулы мономера по связи Ti–Et. Одновременно с внедрением мономера и ростом цепи происходит регенерация вакантной d-орбитали Ti. Способ ее регенерации определяет возможность получения той или иной стереоструктуры получаемого полимера.
Лекция 3 – Поликонденсация
Содержание:
Классификация поликонденсационных процессов.
Поликонденсационное равновесие и молекулярная масса полимеров.
Кинетика линейной поликонденсации.
Проведение поликонденсации в расплаве, растворе, на границе раздела фаз.
1.Поликонденсацией называется процесс образования полимеров из би - или полифункциональных мономеров, сопровождающийся выделением побочных низкомолекулярных соединений (воды, спирта). При поликонденсации элементный состав звеньев полимера не совпадает с элементным составом исходных веществ. Поликонденсация происходит в результате взаимодействия функциональных групп.
Различают гомополиконденсацию, в которой участвуют однородные молекулы с различными реакционноспособными функциональными группами:
nH2N(CH2)6COOH ↔ [- NH(CH2)6CO - ]n + (n-1)H2O
или однородные молекулы с одинаковыми реакционноспособными функциональными группами:
nHO(CH2)2OH ↔ [- (CH2)2 – O-]n + (n-1)H2O
и гетерополиконденсацию, в которой участвуют разнородные реакционноспособные молекулы с функциональными группами:
![]()
По характеру химических процессов, лежащих в основе реакции поликонденсации, различают равновесную и неравновесную поликонденсацию. Если в результате поликонденсации наряду с полимерами получается низкомолекулярное вещество, способное реагировать в условиях реакции с образовавшимся полимером, то процесс является равновесным. Если образовавшееся при поликонденсации низкомолекулярное соединение не реагирует в условиях реакции с полимером, то поликонденсация является неравновесной.
2. Средняя степень поликонденсации образующегося полимера ![]()
![]() равна:
равна:
![]()
Величина ![]()
![]() линейно возрастает во времени. Высокомолекулярные продукты могут быть получены при степенях превращения p > 0,95. При меньших конверсиях образуются лишь олигомерные соединения. Предельное значение
линейно возрастает во времени. Высокомолекулярные продукты могут быть получены при степенях превращения p > 0,95. При меньших конверсиях образуются лишь олигомерные соединения. Предельное значение ![]()
![]() при р=1 определяют по уравнению
при р=1 определяют по уравнению ![]()
![]() , где
, где ![]()
![]() - отношение начальных концентраций функциональных групп. Практически величина р никогда не достигает 1, и поэтому
- отношение начальных концентраций функциональных групп. Практически величина р никогда не достигает 1, и поэтому
![]()
Для получения ВС полимеров состав мономерной смеси должен быть близок к стехиометрическому.
Молекулярная масса полимера в равновесных условиях не зависит от концентрации мономера. Скорость же поликонденсации пропорциональна концентрации реагирующих веществ. Поэтому с повышением концентрации мономера сокращается время, необходимое для достижения равновесия и получения полимера с максимальной молекулярной массой.
Для получения ВМ полимера необходимо тщательное удаление НМС.
3. Скорость линейной поликонденсации определяется скоростью изменения концентрации одной из функциональных групп (сА) или (сВ):
-dcA/dt = - dcB/dt = k1ckcAcB=kcAcB,
где ck – концентрация катализатора, принимаемая за постоянную величину в течение всего процесса; k=k1ck – эффективная константа скорости. Принимая, что сА≈сВ=с, получим:
-dc/dt=kc2.
Интегрируя это уравнение и подставляя с=ср(1-р), где р – степень завершенности реакции по исчерпыванию функциональных групп, получаем
c0kt = 1/1-p,
где с0 – начальная концентрация функциональных групп. Катализаторами поликонденсации служат те же соединения, которые катализируют реакции монофункциональных веществ (минеральные кислоты, сульфокислоты и т. д.).
4.Поликонденсацию проводят в расплаве, растворе, на границе раздела фаз, а также в твердой фазе.
Поликонденсацию в расплаве проводят в отсутствие растворителя или разбавителя при 200-2800С. Процесс осуществляется в атмосфере инертного газа и заканчивают обычно в вакууме. Достоинства: возможность получения полимеров из мономеров с пониженной реакционной способностью, высокий выход полимера и его высокая степень чистоты, сравнительная простота технологической схемы и возможность использования полимера в виде расплава для формования волокон и пленок. Недостатки: необходимость использования термически стойких мономеров, большая продолжительность процесса и необходимость его проведения при высоких температурах, что вызывает деструкцию полимера.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



