При поликонденсации в растворе мономеры находятся в растворенном состоянии. Преимуществом этого способа является возможность осуществления процесса в относительно мягких условиях, хорошая теплопередача и облегченное удаление низкомолекулярного побочного продукта.
Межфазная поликонденсация протекает на границе раздела двух несмешивающихся жидкостей или жидкости и газа. Для проведения поликонденсации на границе раздела двух несмешивающихся жидкостей исходные реагенты растворяют раздельно в двух несмешивающихся жидкостях. При контакте растворов на границе раздела фаз мгновенно образуется полимер, который непрерывно удаляют из зоны реакции, и процесс ведут до полного исчерпания мономеров. Для увеличения контакта компонентов фазы перемешивают. Преимущества – высокие скорости и низкие температуры реакции, не требуется высокая степень очистки реагентов, стехиометрический состав поддерживается автоматически. Недостаток – использование дорогостоящих мономеров с высокой реакционной способностью, затраты на регенерацию растворителя.
Поликонденсация в твердой фазе. Проводят при нагревании в вакууме и присутствии водоотнимающих средства порошкообразного линейного полимера или специально приготовленной из него пленки. Процесс протекает с высокой скоростью. Процесс используют при синтезе полимеров из мономеров, разлагающихся при температуре плавления.
Лекция 4 - Мембранная осмометрия
Содержание:
Определение осмометрическим методом среднечеслового молекулярного веса. Определение осмотическим методом второго вириального коэффициента. Осмотическое давление высококонцентрированных полимерных растворов. Мембранные осмометры.
|
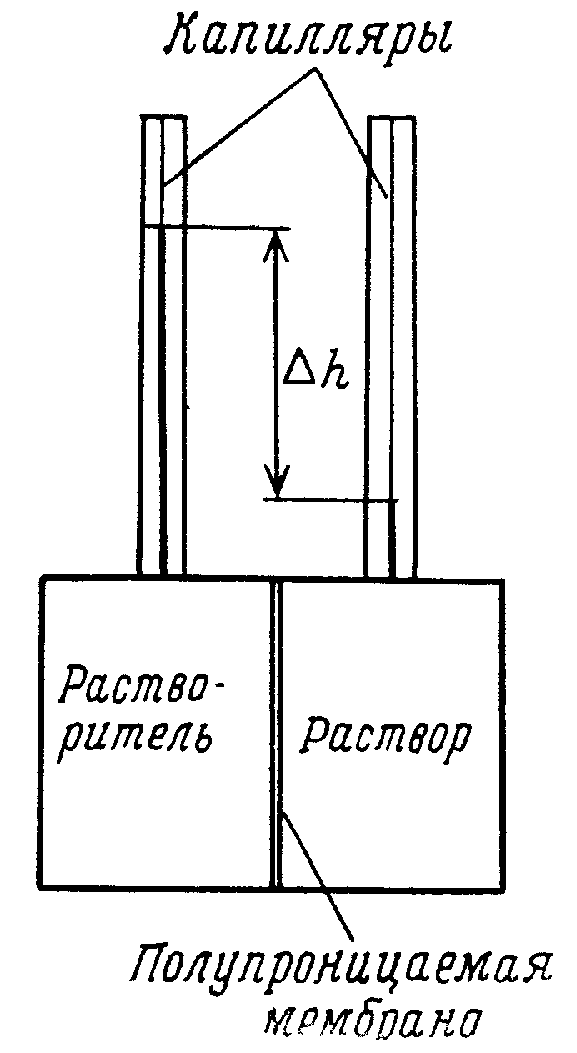
Рис. 1 Принцип измерения осмотического давления |
Если чистый растворитель отделен полупроницаемой мембраной от того же растворителя, находящегося в растворе, их химические потенциалы не равны друг другу. Это обусловливает перенос растворителя через мембрану к раствору. Разность давлений по обе стороны от мембраны в состоянии равновесия называется осмотическим давлением и оценивается разностью высот в капиллярах раствора и растворителя (∆һ) (рис.1). Интервал молекулярных весов, которые можно определить с помощью мембранной осмометрии, составляет 5*103 – 5*105 и даже 106.
Нижний предел задается проницаемостью мембраны (диффузией частиц низкого молекулярного веса), тогда как верхний предел определяется тем наименьшим осмотическим давлением, которое поддается измерению.
1. Для полудисперсного линейного полимера среднечисловой молекулярный вес (Мn)можно расчитать по данным осмометрии, используя следующие выражения:
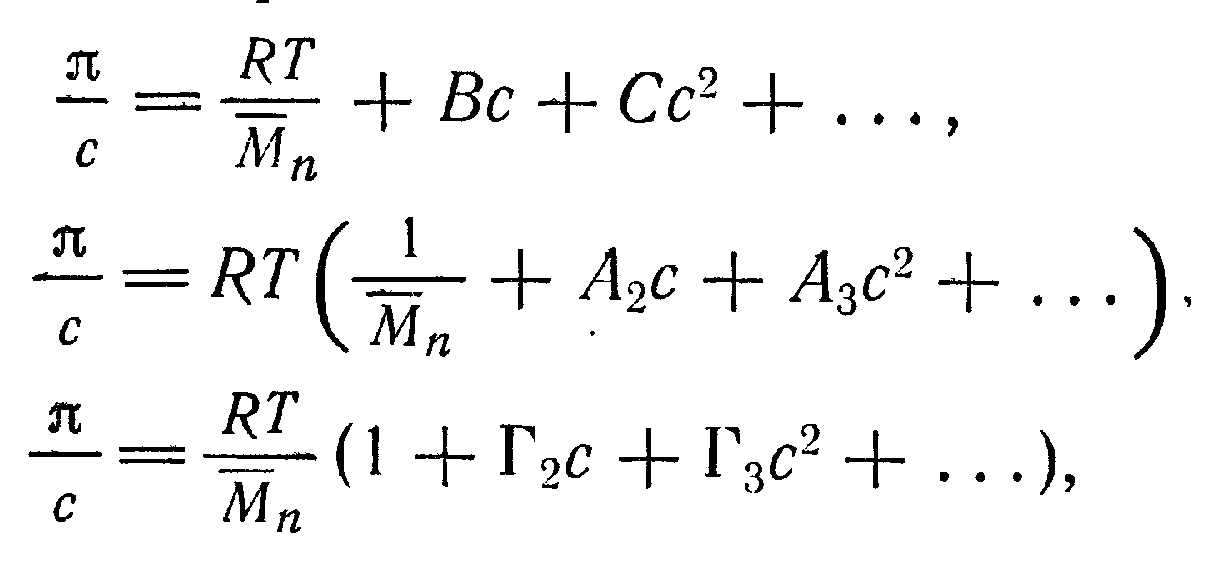 (1-3)
(1-3)
Размерность которых дин-л на грамм-сантиметр (СРГ) или джоуль на килограмм (СИ). В этих выражениях р – осмотическое давление, определяемое как
р═сg∆h (4)
с –плотность растворителя; g – ускорение силы тяжести (0,981 м*с-2); ∆h – давление, выражаемое через высоту столба растворителя (см); с – концентрация раствора; (р/с) – приведенное осмотическое давление; R – универсальная газовая постоянная; Т – термодинамическая температура (К); В, А, Г2 и С, А3, Г3 – вириальные коэффициенты; ![]() – среднечисловой молекулярный вес.
– среднечисловой молекулярный вес.
|
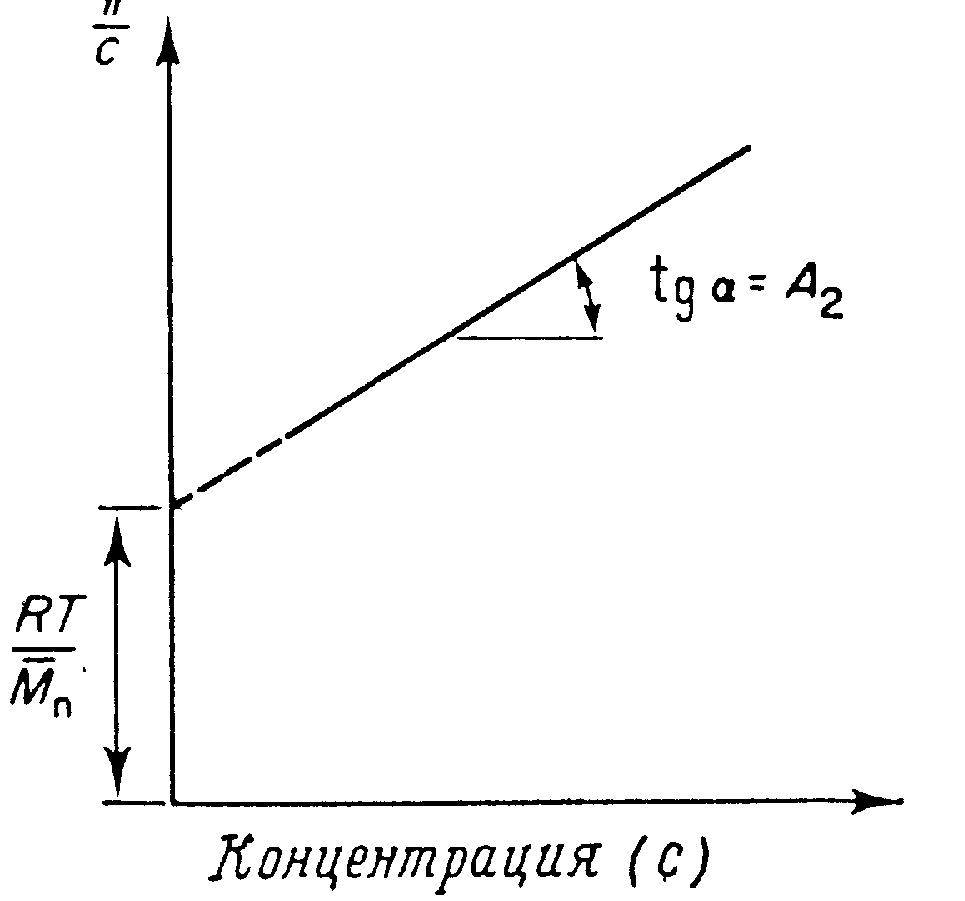
Рис. 2. Зависимость приведенного осмотического давления (р/с) от концентрации |
Для того чтобы получить ![]() в надлежащих единицах, необходимо, чтобы выражение р/с имело размерность дин*л*г-1 и R═0,08207 л*атм*моль-1*К-1 (СГС) или размерность р/с была Дж*кг-1 и R═8,314 Дж*К-1моль-1 (СИ).
в надлежащих единицах, необходимо, чтобы выражение р/с имело размерность дин*л*г-1 и R═0,08207 л*атм*моль-1*К-1 (СГС) или размерность р/с была Дж*кг-1 и R═8,314 Дж*К-1моль-1 (СИ).
Поскольку третий член (А3с2) пренебрежимо мал, то уравнение (1.2) принимает вид
р/с═R(1/ ![]() + А2с) (5)
+ А2с) (5)
тогда кривая зависимости р/с от с представляет собой прямую линию, отсекающую на ординате отрезок, равный RТ/ ![]() (рис 2). Если измерения проводятся в и-условиях, то р/с не зависит от с и равно
(рис 2). Если измерения проводятся в и-условиях, то р/с не зависит от с и равно
![]()
(6)
![]()
На практике осмотическое давление измеряют как разность высот жидкости в капиллярах с раствором и растворителем (∆h) в сантиметрах. Для экстраполяции на бесконечное разбавление необходимо знать осмотическое давление при нескольких концентрациях (например, 2,0, 4,0, 6,0 и 8,0 г/л). Среднечисловой молекулярный вес можно найти из кривой на рис. 2 или из выражениях
(7)
При обработке осмотических данных очень важно выражать экспериментальные данные в соответствующих единицах.
2. В осмометрии второй вириальный коэффициент (А2) выражается как
![]()
(8)
где сs – плотность растворителя; сp – плотность полимера, Ms - молекулярный вес растворителя; ч – параметр взаимодействия Флори.
Единицы, в которых выражается второй вириальный коэффициент, зависят от вида используемого уравнения (таблица 1.1).

Таблица 1.1Различные способы выражения приведенного осмотического давления (р/с) и второго вириального коэффициента
Второй вириальный коэффициент (А2) экспериментально можно вычислить из значений р/с для двух концентраций с1 и с2, используя выражение
![]()
(9)
[л*моль*г-1 (СГС) или м3*моль*кг-1 (СИ)].
А2 можно найти и из наклона кривой на рис. 3: tgб= A2.
3. Приведенное осмотическое давление ( р/с) для сильно концентрированных растворов полимеров выражается как
![]()
(10)
где член (1+Г2с + Г3с2 + ...) дает относительное отклонение от идеального раствора.
Вириальные коэффициенты Г2 и Г3 являются функциями системы растворитель – растворенное вещество, температуры, молекулярного веса растворенного вещества и молекулярновесового распределения.
Преобразование уравнения (1.10) дает
![]()
(11)
Зависимость ![]() от с представляет собой прямую линию, отсекающую на ординате отрезок, равный Г2 (рис 1.3). Г3 находят как тангенс угла наклона прямой: tgб= Г3.
от с представляет собой прямую линию, отсекающую на ординате отрезок, равный Г2 (рис 1.3). Г3 находят как тангенс угла наклона прямой: tgб= Г3.
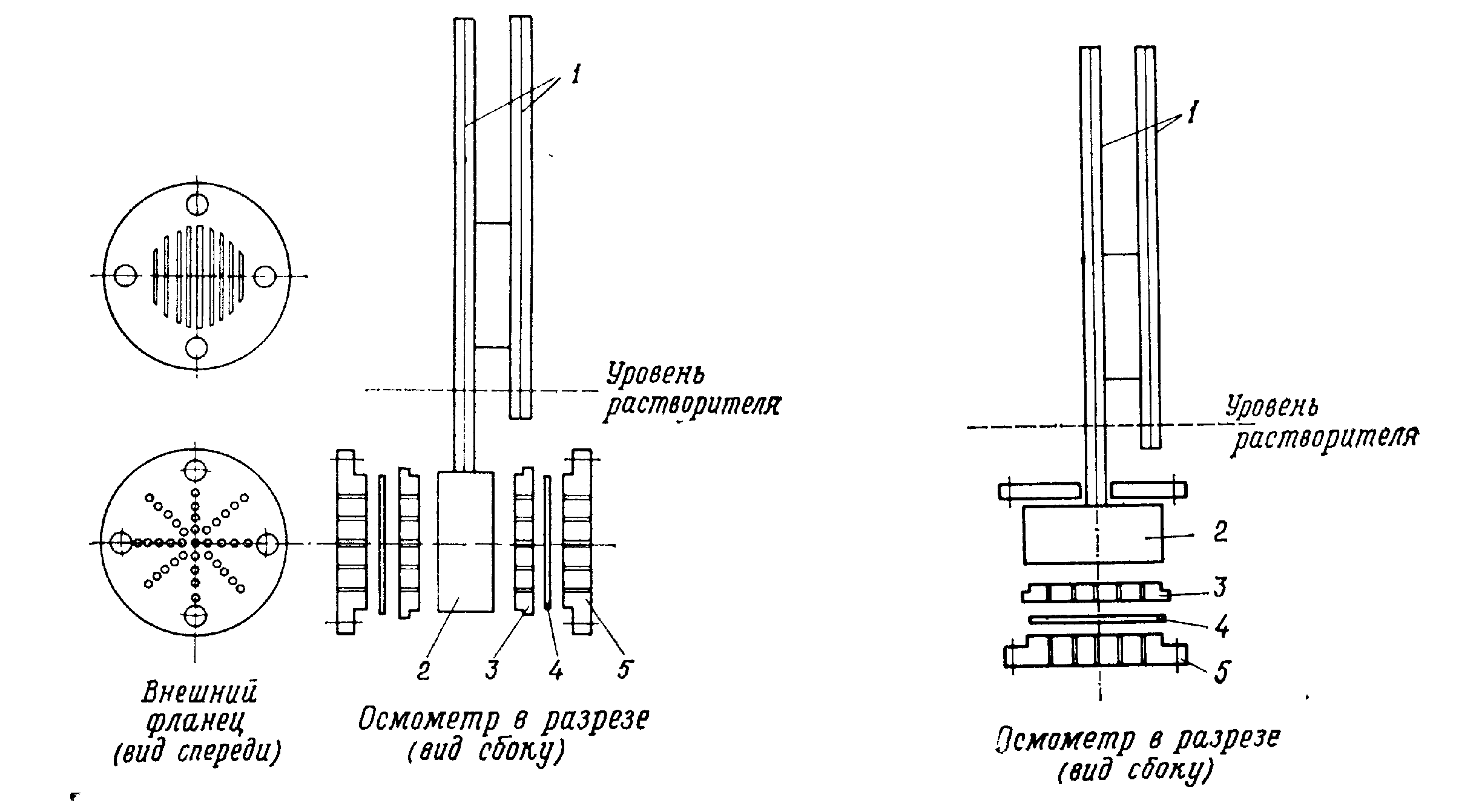
4. Мембранные осмометры можно разделить на две большие группы: статические и динамические осмометры. Статические осмометры контруируются следующих двух типов: 1) вертикальные осмометры (например, осмометр Хельфрица) (рис. 3) и 2) горизонтальнве осмометры (например, осмометр Шульца) (рис. 4).
| |
Рис. 3 Узел кюветы в вертикальном осмометре Хельфрица: 1 – капилляры, 2 – ячейка с раствором, 3 – внутренний фланец, 4 – мембрана, 5 – внешний фланец | Рис. 4 Узел кюветы в горизонтальном осмометре Шульца: 1 – капилляры, 2 – ячейка с раствором, 3 – внутренний фланец, 4 – мебрана, 5 – внешний фланец |
Статический осмометр состоит из двух ячеек: ячейки для раствора, показанной на рис. 3 и 4 и ячейки для растворителя, представляющей собой обычный стеклянный сосуд, куда помещают ячейку с раствором. Эти ячейки разделяют одна или две полупроницаемые мембраны. После заполнения одной ячейки чистым растворителем, а другой – раствором известной концентрации осмометр помещабт в термостат (±0,010С). После установления изохорногодавления измеряют разность высот жидкости в капиллярах, соединенных с каждой ячейкой. Изохронное давление – это давление, при котором суммарный объемный поток равен нулю.
Динамические осмометры конструируются в вмде автоматических приборов, измеряющих скорость течения через полупроницаемую мембрану, с регулированием давления таким образом, чтобы полезный поток был равен нулю. Важнейшим достоинством динамического метода является возможность измерения изохронного давления через большой прормежуток времени (5-10 мин) и меньший перенос растворенного вещества.
Наиболее распространены следующие осмометры:
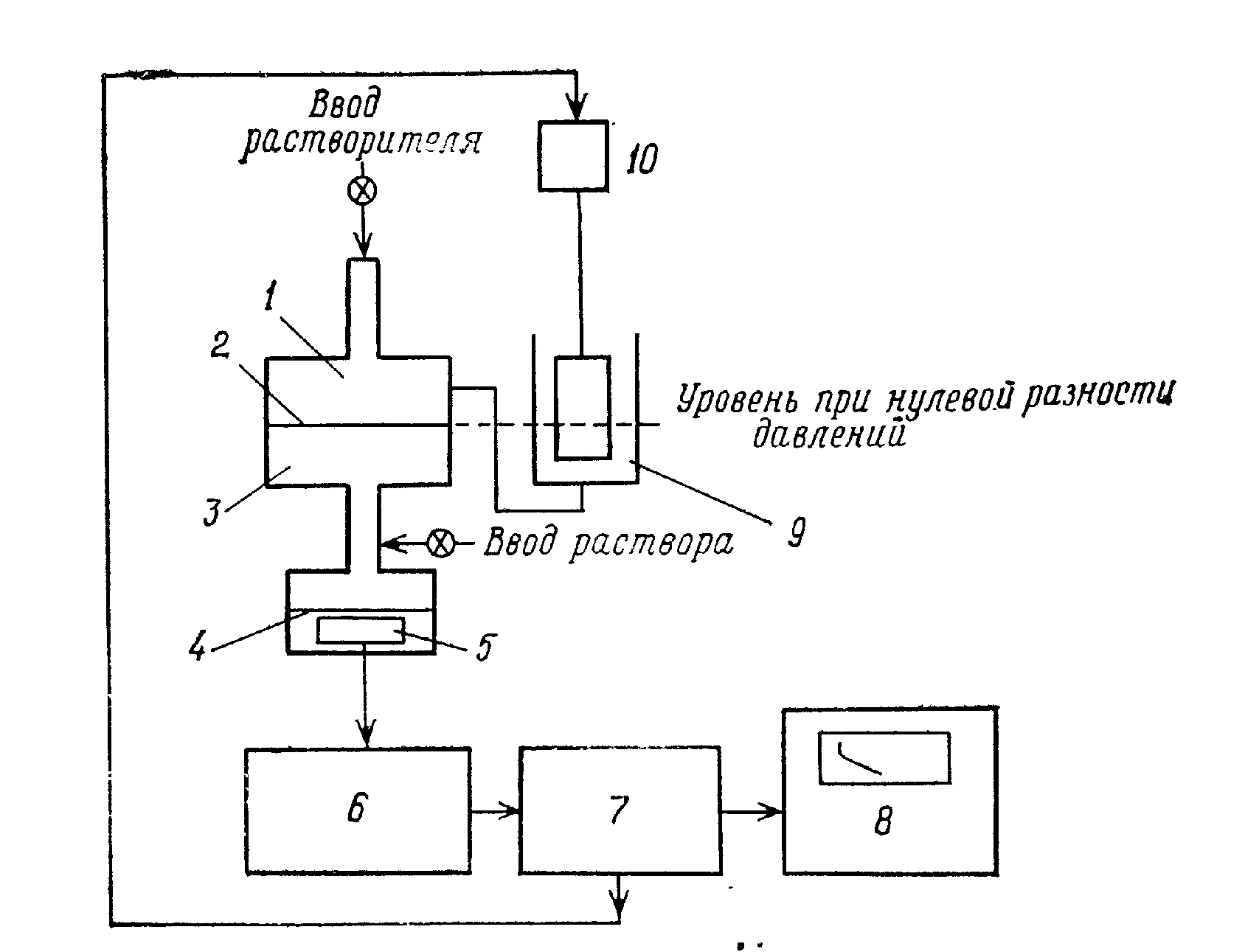
Осмометр Mechrolab(рис.5). В этом осмометре горизонтальная мембрана разделяет две ячейки: одн верхнюю для раствора и другую нижнюю для растворителя. К ячейке, содержащей растворитель, присоединен стеклянный капилляр. Один его конец соединен гибкой трубкой с емкостью, содержащей растворитель. В капилляр вводится пузырек воздуха, который прерывает световой луч, освещающий фотоячейку. Этот эффект используется для выравнивания осмотического тока с помощью сервосистемы. Характеристикой осмотического давления служит разность высот жидкости в капилляре, соединенном с ячейкой раствора, и в резервуаре с растворителем.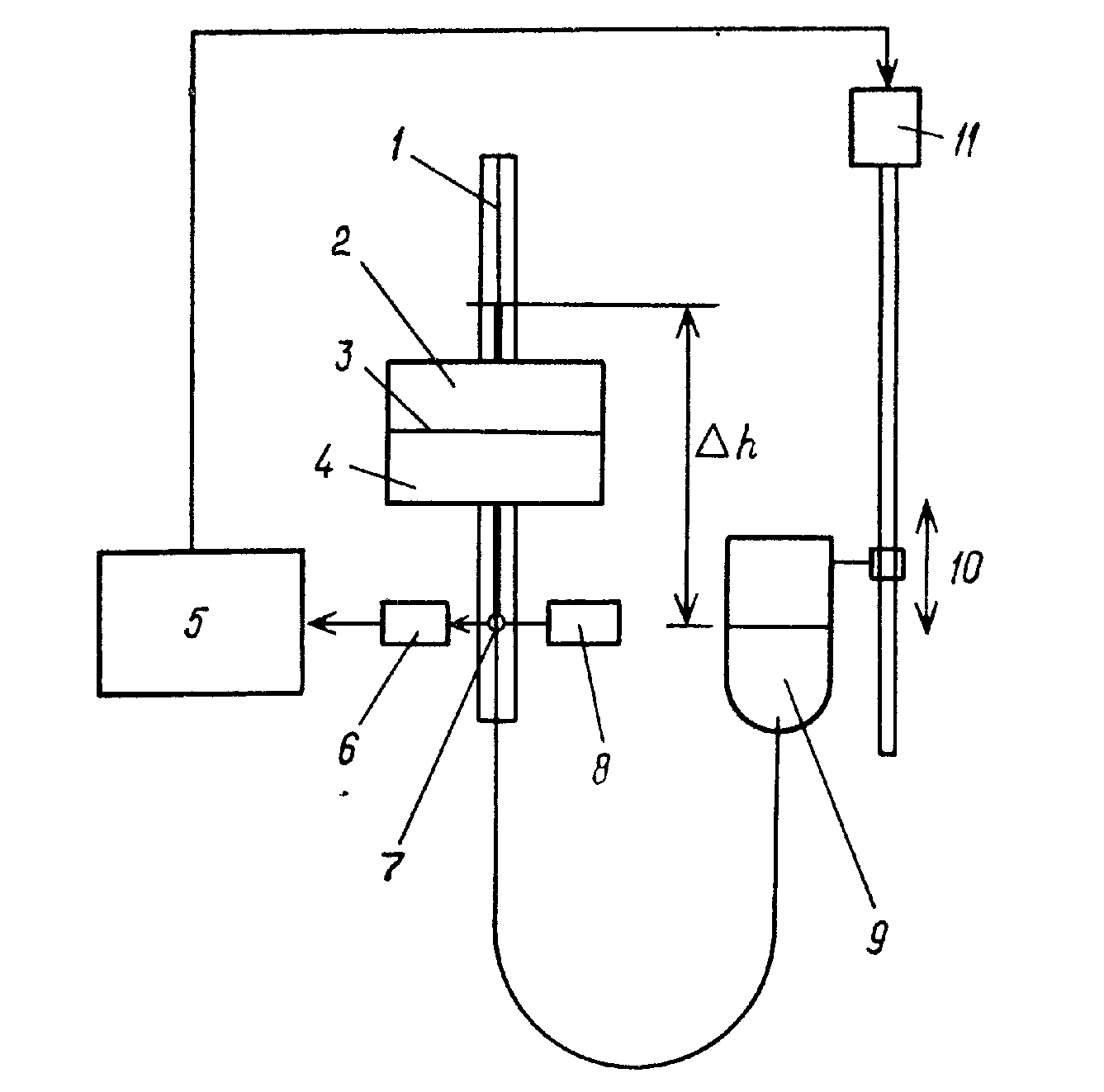

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |