Е0г = Е0Си - Е0Ят = 0,34 – (-0,76) = 1,1в.
2. Электродный потенциал металла зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста. Е = Е0 + (RT/nF)·lnС. Если внести в уравнение постоянные величины, использовать десятичный логарифм, то при Т = 298К электродный потенциал металла Е = E0 + (0,059/n) · lgC. Здесь С – молярная концентрация ионов в растворе, n - число электронов, принимающих участие в процессе.
3. Под коррозией металла понимают его разрушение под воздействием окружающей среды. Основные виды коррозии: 1. сплошная, 2. местная, 3. интеркристаллитная, 4. транскристаллитная, 5. избирательная, 6. подповерхностная. По механизму протекания коррозионного разрушения различают два типа коррозии - химическую и электрохимическую.
Химической коррозией называется разрушение металла окислением его в окружающей среде без возникновения электрического тока в системе. В этом случае происходит взаимодействие металла с составными частями среды – газами и неэлектролитами. Электрохимической коррозией называется разрушение металла в среде электролита с возникновением внутри системы электрического тока. Электрохимическую коррозию вызывают загрязнения, примеси, содержащиеся в металле. В этих случаях при соприкосновении металла с электролитом на его поверхности возникает множество котроткозамкнутых гальванических микроэлементов. При этом анодами являются частицы металла, катодами – загрязнения, примеси. На аноде происходит процесс окисления Ме - nз → Men+, на катоде происходит процесс востановления водорода или кислорода: 2 Н++ 2з → 2 Н0 – Н2 ( рН<7); О2+ 4з +2 Н2О →4 ОН - (рН>7).
Скорость коррозии тем больше, чем дальше расположены друг от друга в ряду стандартных электродных потенциалов металлы, из которых образовался гальванический элемент и чем больше влажность воздуха. Металлы высокой чистоты (метеоритное железо) коррозии не подвергаются.
Вещества ускоряющие коррозию (хлориды, фториды, сульфиды, нитраты, бромиды, йодиды), называются стимуляторами или активаторами. Вещества, замедляющие коррозию, называются ингибиторами. Полностью предотвратить коррозию невозможно, возможно лишь уменьшить скорость корродирования. Для этого используют следующие методы: защита поверхности металлов покрытиями, создание сплавов с антикоррозионными свойствами, электрохимические методы, изменение состава среды.
Основные понятия: Гальванические элементы. ЭДС.
Вопросы для самоконтроля:
1. Что такое гальванический элемент? Приведите примеры.
2. Охарактеризуйте принцип работы гальванического элемента Даниэля – Якоби.
12. Лекция
Электролиз
План
1. Электролиз, законы электролиза.
2. Коррозия металлов.
Электродные потенциалы и механизм их возникновения.
Для определения направления и полноты протекания окислительно-восстановительных реакций между окислительно-восстановительными системами в водных растворах используются значения электродных потенциалов этих систем.
Механизм возникновения электродных потенциалов, их количественное определение, процессы, которые сопровождаются возникновением электрического тока или вызваны электрическим током, изучаются особым разделом химии – электрохимией.
К электрохимическим относятся явления, возникающие на границе двух фаз с участием заряженных частиц (ионов и электронов), например, при погружении металлической пластинки в воду.
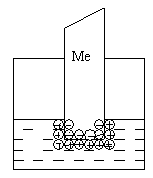
Для всех металлов характерно свойство в большей или меньшей степени растворяться в воде. При этом в воду переходят положительно заряженные ионы металла, в результате чего пластинка (из-за появления в ней избыточных электронов) заряжается отрицательно. Гидратированные катионы металла скапливаются возле поверхности пластинки на границе раздела двух фаз (металл-раствор). Возникает двойной электрический слой, характеризующийся некоторой разностью электростатических потенциалов. Как известно, энергию, которую необходимо затратить (положительный потенциал) или которую можно получить (отрицательный потенциал) при переносе единицы электричества из бесконечности в данную точку, называют электрическим потенциалом. Между пластинкой и раствором устанавливается окислительно-восстановительное равновесие:
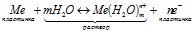 . (9.1)
. (9.1)
При погружении металла в раствор его соли также возникает двойной
электрический слой, но в этом случае возможны два механизма его образования. Если концентрация катионов металла в растворе мала или металл довольно активный, вследствие чего равновесие процесса, указанного выше, сдвинуто вправо, то металлическая пластинка заряжается отрицательно:
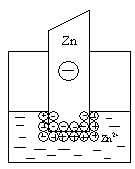
В том случае, когда концентрация катионов металла в растворе велика или металл малоактивный, равновесие указанного процесса сдвигается влево и металлическая пластинка заряжается положительно:
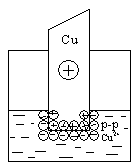
В любом случае на границе раздела двух фаз образуется двойной электрический слой. Разность (скачок) потенциалов, возникающая между металлом и жидкой фазой, называетсяэлектродным потенциалом Е. Потенциалу металла приписывается тот знак, который возникает на его поверхности в двойном электрическом слое.
Водородный электрод. Стандартные электродные потенциалы металлов. Ряд стандартных электродных потенциалов.
Для определения направления и полноты протекания окислительно-восстановительных реакций между окислительно-восстановительными системами в водных растворах используются значения электродных потенциалов этих систем.
Механизм возникновения электродных потенциалов, их количественное определение, процессы, которые сопровождаются возникновением электрического тока или вызваны электрическим током, изучаются особым разделом химии – электрохимией.
К электрохимическим относятся явления, возникающие на границе двух фаз с участием заряженных частиц (ионов и электронов), например, при погружении металлической пластинки в воду.
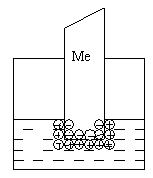
Для всех металлов характерно свойство в большей или меньшей степени растворяться в воде. При этом в воду переходят положительно заряженные ионы металла, в результате чего пластинка (из-за появления в ней избыточных электронов) заряжается отрицательно. Гидратированные катионы металла скапливаются возле поверхности пластинки на границе раздела двух фаз (металл-раствор). Возникает двойной электрический слой, характеризующийся некоторой разностью электростатических потенциалов. Как известно, энергию, которую необходимо затратить (положительный потенциал) или которую можно получить (отрицательный потенциал) при переносе единицы электричества из бесконечности в данную точку, называют электрическим потенциалом. Между пластинкой и раствором устанавливается окислительно-восстановительное равновесие:
![]() . (9.1)
. (9.1)
При погружении металла в раствор его соли также возникает двойной
электрический слой, но в этом случае возможны два механизма его образования. Если концентрация катионов металла в растворе мала или металл довольно активный, вследствие чего равновесие процесса, указанного выше, сдвинуто вправо, то металлическая пластинка заряжается отрицательно:
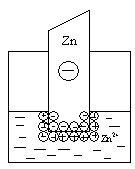
В том случае, когда концентрация катионов металла в растворе велика или металл малоактивный, равновесие указанного процесса сдвигается влево и металлическая пластинка заряжается положительно:
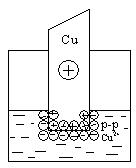
В любом случае на границе раздела двух фаз образуется двойной электрический слой. Разность (скачок) потенциалов, возникающая между металлом и жидкой фазой, называетсяэлектродным потенциалом Е. Потенциалу металла приписывается тот знак, который возникает на его поверхности в двойном электрическом слое.
Электролиз с нерастворимыми и растворимыми электродами.
Электролиз – окислительно-восстановительный процесс, протекающий при прохождении постоянного электрического тока через раствор или расплав электролита.
При электролизе энергия электрического тока превращается в химическую энергию, иначе говоря, осуществляется процесс, обратный по характеру происходящему в гальваническом элементе. Как и в случае гальванического элемента, на аноде происходит окисление, а на катоде – восстановление. Но при электролизе анодом является положительный электрод, а катодом – отрицательный.
Характер протекания электродных процессов при электролизе зависит от многих факторов, важнейшими из которых являются состав электролита, материал электродов и режим электролиза (температура, плотность тока и т. д.).
Различают электролиз расплавов и растворов электролитов.
Электролиз расплавов электролитов.
Электролиз расплава соли с использованием инертных электродов показан на следующей схеме:
Анод
При высоких температурах расплав соли диссоциирует на ионы:
![]() .
.
Прохождение электрического тока через расплав обусловлено тремя одновременно протекающими процессами:
направленное движение катионов Мg2+ к катоду, а анионов Cl - - к аноду; восстановление, происходящее на катоде:![]()
![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 |



