Состав дальтонидов выражается простыми формулами с целочисленными стехиометрическими индексами, например, MgO, HCl.
Современный взгляд на вопрос включает также наличие полной информации о структуре — в стехиометрическом соединении (истинном дальтониде) заселённости кристаллографических позиций равны единице, то есть, дефекты в макроскопических количествах отсутствуют. По одному только составу нельзя строго отнести вещество к классу дальтонидов. Например, область гомогенности оксида титана TiO включает стехиометрический состав (где соотношение компонентов точно 1:1). Однако ни при этом составе, ни при каком-либо другом не достигаются идеальные (единичные) заселённости позиций титана и кислорода. То есть, данное соединение не является дальтонидом.
Металлиды — химические соединения (обычно металл — металл, такие соединения называются интерметаллическими, реже переходный металл — неметалл), характеризующиеся металлическим типом связи. В таких соединениях не соблюдается правило формальной валентности, они имеют высокую температуру плавления (часто выше чем у индивидуальных компонентов), являются бертоллидами.
Примеры металлидов
- Металл — металл: Cu9Al4. Металл — неметалл: Ti6O. Соединения, природа связи в которых может быть металлической или ионной в зависимости от состава: GaAs, NiAs.
Основные понятия: химия как наука, предмет, задачи химии и связь с другими науками, краткая история химии, значение химических знаний для специалистов отрасли организации перевозок движения и эксплуатации транспорта, атом, молекула, атомно-молекулярное учение, молярная масса, моль, молярный объём, химический эквивалент, закон сохранения массы, закон постоянства состава, закон эквивалентов, газовые законы ( объёмных отношений, Бойля – Мариотта, Гей – Люссака, Шарля, объединённый газовый закон, Авогадро), уравнение Клайперона – Менделеева.
Вопросы для самоконтроля:
Что изучает наука химия? Расскажите об актуальных направлениях применения химии?2. Одинаковы ли понятия: «атомная масса» и « масса атома» ?Перечислите основные законы химии, которые подтверждают правильность атомистической теории.
3. Что показывает химическая формула? Какие расчёты можно производить по формуле?
4. Что показывает число Авогадро? Как можно воспользоваться этим законом для определения величин молярных масс веществ?
5. В чем смысл закона сохранения массы вещества, каково его практическое значение?
6. Сформулируйте закон постоянства состава. Как называются соединения, имеющие переменный состав? Приведите примеры.
7. Сформулируйте закон объёмных отношений. Какова его роль в развитии атомно-молекулярных представлений?
8. Сформулируйте закон эквивалентов. Дайте определение понятию «эквивалент».
9. В чем смысл законов идеальных газов? Приведите примеры.
10. Как рассчитать объёмную и молярную долю компонента в газовой смеси? Докажите равенство их, используя следствие закона Авогадро.
2. Лекция
Строение атома
План
Модели строения атома: модели Томсона, Резерфорда, Бора. Квантово-механическая модель строения атомов: атомные орбитали, квантовые числа, принцип Паули, правила Хунда и Клечковского. Строение атомных ядер и изотопов. Ионы, энергия ионизации и сродство к электрону.4. Элементарные частицы и ядерные реакции. Искусственная радиоактивность.
1. Модели строения атома: модели Томсона, Резерфорда, Бора.
Долгое время в науке господствовало мнение, что атомы не делимы. Однако в конце ЧЙЧ – начале ЧЧ века был установлен ряд фактов свидетельствующих о сложном составе атомов. Сюда относятся открытие электрона, а также открытия и изучение радиоактивности. Изучение радиоактивности подтвердило сложность состава атомов. Теперь встал вопрос о строении атома, о его внутренней структуре. Согласно модели предложенной в 1903 году Томсоном атом состоит из положительного заряда, равномерно распределенного по всему объему атому и электрона колеблющегося внутри этого заряда. Для проверки гипотезы Томсона и более точного определения внутреннего строения атома Резерфорда провел серию опытов по рассеянию б-частиц тонкими металлическими пластинками. По результатам этих опытов в 1911 году Резерфорд предложил схему строения атома. Согласно этой схеме атом состоит из положительно заряженного ядра, в котором сосредоточено преобладающая часть массы атома и вращающихся вокруг него электронов. Положительный заряд ядра нейтрализуется суммарным отрицательным зарядом электрона, следовательно, атом в целом электронейтрален. Модель Резерфорда в некоторых отношениях противоречива твердо-установленным фактам. В настоящее время существует две модели структуры атома: 1 – модель Бора; 2 – квантово-механическая модель строения атома. Согласно теории Бора электроны в атоме вращаются вокруг ядра не по любым, а только по определенным круговым орбитам, соответствующим разным значениям энергии. Он утверждал, что энергия электрона изменяется скачками, то есть энергетические состояния электронов в атоме квантованы. Энергия электроны вращающегося вокруг ядра зависит от радиуса орбиты. Электрон обладает минимальной энергией, находясь на ближайшей к ядру орбите. При поглощении кванта энергии электрон переходит на менее стабильный уровень с более высокой энергией. При этом энергия атома увеличивается, и он перейдет в возбужденное состояние. Переход электрона в обратном направлении приведет к уменьшению энергии атома и освобождению поглощенной им энергии. Бор пронумеровал уровни энергии электрона, также обнаружил, что на разных энергетических уровнях может находиться разное количество электронов: 1 уровень содержит до 2 электронов; 2 уровень - до 8 и т. д. Теория Бора хорошо подходила для простых атомов, например водород, но не для атомов с более сложной структурой.
Квантово-механическая модель строения атома: атомные орбитали, квантовые числа, принцип Паули, правила Хунда и Клечковского.
В 20-х годах ЧЧ века появилась новая теория строения атомов, основанная на представлениях квантовой механики – квантово-механическая модель атома. В основу этой модели положена квантовая теория, согласно которой электрон имеет двойственную природу, т. е. обладает свойствами частицы и также волны. Следовательно, нельзя говорить о какой-либо определенной траектории движения электрона. Можно лишь судить о той или иной вероятности пребывания его в данной точке пространства - это принцип неопределенности. По современным представлениям состояние электрона в атоме описывается с помощью 4 чисел, которые называются квантовыми.
Название | Символ | Описание | Допустимые значения |
Главное | n | Энергетический уровень орбитали | Положительные целые числа (1,2,3 и т. д.) |
Орбитальное | l | Форма орбитали | Целые числа от 0 до n-1 |
Магнитное | m | Ориентация | Целые числа от –l до +l, в том числе нулевое значение |
Спиновое | ms | Спин электрона | -1/2 и +1/2 |
n – описывает среднее расстояние от орбитали до ядра, а также энергетическое состояние электрона находящегося в атоме. n может принимать положительные целочисленные значения. Чем больше значение n, тем выше энергия электрона и больше размер электронного облака. Электроны, характеризующиеся одним и тем же значением n, образуют в атоме электронные облака одинакового размера, которые называются электронными оболочками.
l – также называется побочным и описывает форму орбитали, которая зависит от n. l может принимать целочисленные значения от 0 до n-1. Например, при n=3 возможны l=0,1,2. Орбитали имеющие одинаковые значения n, но разные значения l принято называть энергетическими подуровнями. Энергетические подуровни обозначаются разными буквами.
Обозначение энергетических подуровней
Орбитальное квантовое число | Обозначение энергетических подуровней |
0 | s |
1 | p |
2 | d |
3 | f |
4 | g |
m – описывает ориентацию в пространстве различных орбиталей, может принимать любое целочисленное значение как положительное так и отрицательное в пределах от –l до +l. Следовательно значение m зависит от значений l. Например, для l=1 возможны m= -1,0,+1. Это значит, что p-орбиталь имеет 3 разные пространственные ориентации. Энергия этих орбиталей одинакова, а ориентация в пространстве разная.
ms – описывает направление вращения электронов в магнитном поле: по часовой стрелке или против. ms может принимать только 2 значения - -1/2 и +1/2, и на каждой орбитали может находится только 2 электрона: один со спиной +1/2, а другой со спиной -1/2. Для определения состояния электрона в многоэлектронном атоме, важное значение имеет положение Паули (принцип Паули), согласно которому в атоме не может быть двух электронов, у которых все 4 квантовых числа были бы одинаковыми. Из этого следует, что каждая атомная орбиталь характеризуется определенными значениями n, l и m может быть занята не более чем двумя электронами, спины которых имеют противоположные знаки. Два таких электрона находящиеся на одной орбитали и обладающие противоположно направленными спинами, называются спаренными в отличие от одиночного, то есть неспаренного электрона, занимающего какую-либо орбиталь. Таким образом, квантовые числа используют для описания состояния электрона в вакууме. Однако существуют и более простые способы описания состояния электрона: 1 – диаграммы уровня энергии атома; 2 – электронные конфигурации.
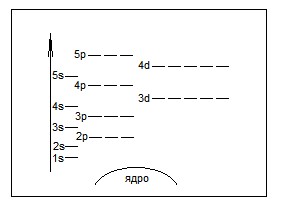
Диаграмма уровня энергии атома
Последовательность заполнения атомных орбиталей:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 |



