РО - давление при нормальных условиях, 101325 Па.
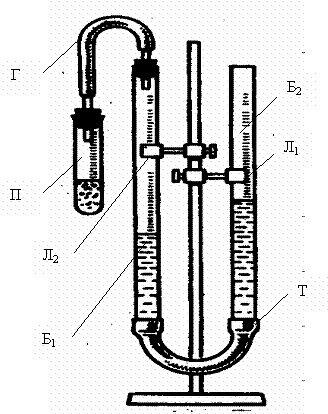
Рис.1. Лабораторная установка для определения эквивалентной массы металла
2. По закону эквивалентов рассчитать эквивалентную массу металла Э.
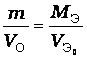 ;
; 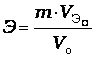 ,
,
где Мэ - эквивалентная масса металла, кг/моль
m – масса навески металла, кг
Vэо - эквивалентный объем водорода, л
Vо – объем водорода, приведенный к нормальным условиям, л
3. Рассчитать относительную погрешность опыта:
относительная погрешность 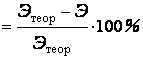 ,
,
где Этеор.- теоретическое значение эквивалентной массы металла,
Мэтеор.=МА/В.
МА - атомная масса металла
В – валентность металла.
Таблица 1
Давление насыщенного водяного пара.
Температура, оС | 18 | 19 | 20 | 21 | 22 | 23 | 24 |
Давление пара, кПа | 2,06 | 2,20 | 2,37 | 2,48 | 2,64 | 2,80 | 2,98 |
Вопросы для самопроверки:
1. Установить правильную последовательность:
Эквивалент - это …
1 моль водород атом количество
замещает которое или присоединяет вещество
2. Дополнить:
1. Масса одного эквивалента вещества называется ____________________________.
2. Масса одного эквивалента магния равна ____________
3. Имея концентрированный раствор азотной кислоты и металл, стоящий в ряду напряжений между_____________и _______________, эквивалентную массу этого металла можно экспериментально определить (название) __________________методом. Для этого необходимо провести реакции:
1) взаимодействия ________________ с __________________;
2) __________________________________ образующейся соли.
4. Вычислить эквивалентную массу металла можно, используя следующее математическое выражение закона эквивалентов ____________________.
Из этого выражения следует, что для определения эквивалентной массы металла необходимо измерить следующие физические величины:
1)________________________; 2) _________________________.
5. Чтобы рассчитать эквивалент металла по его эквивалентной массе, необходимо использовать такое соотношение:________________.
Лабораторное занятие 3
Тема: «Определение энтальпий нейтрализации. Внутренняя энергия и энтальпия»
Цель занятия: Определение энтальпии реакции нейтрализации для следующих реакций:
NaOH (р) + HCl (р) → NaCl (р) + H2O (ж)
KOH (р) + HNO3 (р) → KNO3 (р) + H2O (ж)
NH4OH (р) + CH3COOH (р) → NH4CH3COO (р) + H2O (ж)
Оборудование и реактивы:
Калориметр с мешалкой Термометр Бекмана или термометр с ценой деления 0,1°С 2N растворы: NaOН, КОН, HNO3, HC1, NH4OH, CH3COOH Секундомер (таймер) Мерные цилиндры на 50 мл для каждого раствора Технохимические (аптечные) весы с разновесамиХод работы:
Упрощенный калориметр состоит из двух стаканов. В большой стакан вставляют другой стакан меньшего размера. Стаканы не должны между собой соприкасаться. Во избежание потерь теплоты через стенки внутреннего стакана калориметра между ними помещают прокладки, внутренний стакан закрывают крышкой с тремя отверстиями в которые вставлены термометр {цена деления 0,1 оС} - мешалка и воронка для вливания растворов. Выполняются 2 опыта с сильными электролитами и 1 со слабыми.
Взвесить внутренний калориметрический стакан на технохимических весах и налить в него 50 мл 2 N раствора щелочи, отметить температуру раствора с точностью до 0,1 °С (t° щелочи). Вставить внутренний стакан с раствором щелочи во внешний стакан, закрыть его крышкой, в отверстие крышки поместить мешалку, термометр и воронку. Отмерить цилиндром 50 мл 2 N раствора кислоты и измерить его температуру (t°кислоты).
При непрерывном помешивании быстро прилить через воронку раствор кислоты к раствору щелочи. Отметить самую высокую температуру раствора - t° конечную, которую показывает термометр после смешивания растворов. Вычислить среднюю температуру растворов до реакций - t° начальную (среднее арифметическое из температур растворов кислоты и щелочи), затем рассчитать разницу: Δt° = t° кон. – t0 нач.
Таблица 1.
Система | Масса калориметрического стакана, m1,г | Масса раствора, m2, г | t0нач.,оС=1/2 (t°щел.+t° кисл.) | t° кон., оС | Δt° = t° кон. – t0 нач. | g=Δt°Cc, кДж | ΔН нейтрализации |
Дж/моль | кДж/моль | ||||||
NaOH (р) + HCl (р) | |||||||
KOH (р) + HNO3 (р) | |||||||
NH4OH (р) + CH3COOH (р) |
Вычислить g, выделяющуюся в калориметре по формуле:
g = Δt° ∙ Cc(1),
где Cc – теплоемкость системы; вычисляется как сумма теплоемкостей материала из которого изготовлены
Вопросы для самопроверки:
1. Дополнить:
1. Тепловой эффект реакции - это _________________________
___________________________________________________________________________________________________________, а энтальпия - это _____________________________________________________________
_____________________________________________________________.
2. Термохимическое уравнение реакции нейтрализации уксусной кислоты раствором аммиака можно записать следующим образом:_____________________________________________________.
Изменение энтальпии данной реакции в стандартных условиях, рассчитанное по соотношению __________________________________, равно __________кДж/моль.
3. Растворение в воде соли сопровождается _________________ энергии (_____________________ энтальпии системы), необходимой для ________________________ кристаллической решетки, и ____________________ энергии (___________________ энтальпии системы) за счет процесса ______________________________________. Таким образом, значение энтальпии растворения при стандартных условиях может быть __________________ и ______________________.
4. Энтальпией растворения называется_____________________
__________________________________________________________________________________________________________________________, она выражается в ____________________________.
5. Если растворимость соли в воде с ростом температуры уменьшается, значит процесс растворения ее сопровождается __________________________ теплоты, т. е. ________________________ значением энтальпии растворения.
Установить правильную последовательность и дополнить:
6. Экспериментально энтальпию растворения медного купороса можно определить так:
рассчитать изменение температуры системы
навеску медного купороса высыпать в воду и тщательно перемешать
налить определенный объем воды в химический стакан и измерить ее температуру
вычислить теплоту, поглощенную при растворении, по формуле _____________________________________________
измерить температуру полученного раствора сульфата меди
вычислить энтальпию растворения медного купороса по формуле ____________________________________.
3. Дополнить:
7. Чтобы рассчитать энтальпию гидратации сульфата меди, необходимо экспериментально определить энтальпию растворения ___________________________ и ________________________________. Для расчета энтальпии гидратации необходимо воспользоваться законом ________________, который применительно к данному случаю следует записать так: ___________________________________.
8. Так как при растворении 10 г CaCl2 в 200 мл воды температура раствора повысилась на 7,7К, следовательно, энтальпия растворения его равна_________кДж/моль (удельную теплоемкость раствора принять равной 4,18 Дж/г К).
Тестовые вопросы для самоконтроля:
1.В изолированных системах самопроизвольные процессы протекают в направлении:
А. уменьшения энтропии
В. увеличения энтропии
С. стремления энтропии к нулю
D. немонотонного изменения энтропии
Е. в изменении энтропии нет закономерности.
2.В реакции Fе2О3 + 2 Аl = Аl2О3 + 2 Fе выделилось 213,37 кДж теплоты и получилось 25,49 г. оксида алюминия. ( ДНобрFe2О3 = - 816,72 кДж/моль). Определить ДНобрАl2О3,кДж/моль?
А. -1670,2
В. -1285,4
С. -1080,8
D. -267,9
Е. -15,0
3.Тепловой эффект реакции FeОk.+ H2 г. = Feк. + H2Oг. ,если известно что ДНобр. н2ог.= -241,8 кДж/моль, ДНобр. FеО к. = -264,8 кДж/моль.
А. -23,0
В. -506,6
С. + 23,0
D. + 506,6
Е. -48,8.
4.Количество теплоты, выделившееся при взрыве 8,4 л гремучего газа,
если ДНобр. Н2о г.= -241,8 кДж/моль.
А. 60,5
В. 68,0
С. 76,4
D. 84,3
Е. 88,6.
5.Исходя из значений стандартных энтальпий образования, укажите наиболее устойчивое соединение:
A. Δ Н0AgCl=-127,1 кДж/моль
B. Δ Н0Н2О=- -285,8 кДж/моль
C. Δ Н0НCl=-92,3 кДж/моль
D. Δ Н0AL2O3=-1676 кДж/моль
Е. Δ Н0Al=0 кДж/моль
Лабораторное занятие 4-5
Тема: «Химическая кинетика и химическое равновесие»
Цель занятия: формирование понятий о скорости химической реакции, изучение влияния концентрации, температуры, катализатора на скорость химических реакций.
Методические рекомендации по проведению работы и обработке экспериментальных данных:
ОПЫТ 1. Влияние концентрации реагирующих веществ на скорость химических реакций.
Зависимость скорости реакции от концентрации реагирующих веществ можно изучить на примере реакции взаимодействия тиосульфата натрияNa2S203и серной кислоты концентрациях тиосульфата натрия.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 |



