Согласно де Бройлю, с каждым микрообъектом связываются, с одной стороны, корпускулярные характеристики — энергия Е и импульс р, а с другой — волновые характеристики — частота v и длина волны λ. Количественные соотношения, связывающие корпускулярные и волновые свойства частиц, такие же, как для фотонов:
Е ф =hν, р= ![]() . (33.1)
. (33.1)
Cоотношение (33.1) постулировалось не только для фотонов, но и для других микрочастиц, в частности для таких, которые обладают массой покоя. Таким образом, любой частице, обладающей импульсом, сопоставляют волновой процесс с длиной волны, определяемой по формуле де Бройля:
λ =![]() . (33.2)
. (33.2)
Это соотношение справедливо для любой частицы с импульсом р.
Вскоре гипотеза де Бройля была подтверждена экспериментально. В 1927 г. К. Дэвидсон и Л. Джермер, которые обнаружили, что пучок электронов, рассеивающийся от естественной дифракционной решетки — кристалла никеля, — дает отчетливую дифракционную картину. Дифракционные максимумы соответствовали формуле Вульфа — Брэгга, а брэгговская длина волны оказалась в точности равной длине волны, вычисленной по формуле (33.2).
Впоследствии дифракционные явления обнаружили также для нейтронов, протонов, атомных и молекулярных пучков. Открытие волновых свойств микрочастиц привело к появлению и развитию новых методов исследования структуры вещества, таких, как электронография и нейтронография, а также к возникновению новой отрасли науки — электронной оптики.
На частицы вещества переносится связь между полной энергией частицы Е частотой v волны де Бройля:
Е = hν. (33.3)
Это свидетельствует о том, что соотношение между энергией и частотой в формуле (33.3) имеет характер универсального соотношения, справедливого как для фотонов так и для любых других микрочастиц.
Т. о. всем микрообъектам присущи и корпускулярные, и волновые свойства; в то же время любую из микрочастиц нельзя считать ни частицей, ни волной в классическом понимании.
32.2. Соотношение неопределенностей Гейзенберга
Согласно двойственной корпускулярно-волновой природе частиц вещества, для описания микрочастиц используются то волновые, то корпускулярные представления. Поэтому приписывать им все свойства частиц и все свойства волн нельзя. Естественно, что необходимо внести некоторые ограничения в применении к объектам микромира понятий классической механики.
В классической механике всякая частица движется по определенной траектории, так что в любой момент времени точно фиксированы ее координата и импульс. Микрочастицы из-за наличия у них волновых свойств существенно отличаются от классических частиц. Одно из основных различий заключается в том, что нельзя говорить о движении микрочастицы по определенной траектории и неправомерно говорить об одновременных точных значениях ее координаты и импульса. Так, понятие «длина волны в данной точке» лишено физического смысла, а поскольку импульс выражается через длину волны, то отсюда следует, что микрочастица с определенным импульсом имеет полностью неопределенную координату. И наоборот, если микрочастица находится в состоянии с точным значением координаты, то ее импульс является полностью неопределенным.
В. Гейзенберг пришел к выводу, что объект микромира невозможно одновременно с любой наперед заданной точностью характеризовать и координатой и импульсом.
Согласно соотношению неопределенностей Гейзенберга, микрочастица (микрообъект) не может иметь одновременно и определенную координату (х, у, z), и определенную соответствующую проекцию импульса (рх, ру, рz), причем неопределенности этих величин удовлетворяют условиям
ΔхΔрх ≥h, ΔуΔру ≥h, ΔzΔрz ≥h, (33.4)
т. е. произведение неопределенностей координаты и соответствующей ей проекции импульса не может быть меньше величины порядка h.
Из соотношения неопределенностей (33.4) следует, что, например, если микрочастица находится в состоянии с точным значением координаты (Δх=0), то в этом состоянии соответствующая проекция ее импульса оказывается совершенно неопределенной (Δрх →∞), и наоборот.
Так как в классической механике принимается, что измерение координаты и импульса может быть произведено с любой точностью, то соотношение неопределенностей является, таким образом, квантовым ограничением применимости классической механики к микрообъектам.
В квантовой теории рассматривается также соотношение неопределенностей для энергии Е и времени t, т. е. неопределенности этих величин удовлетворяют условию
ΔЕΔ t ≥h, (33.5)
где ΔЕ — неопределенность энергии некоторого состояния системы. Δt - промежуток времени, в течение которого оно существует.
Следовательно, система, имеющая среднее время жизни Δt, не может быть охарактеризована определенным значением энергии; разброс энергии ΔЕ=h/Δt возрастает с уменьшением среднего времени жизни.
Из выражения (33.5) следует, что частота излученного фотона также должна иметь неопределенность Δν= ΔЕ/h, т. е. линии спектра должны характеризоваться частотой, равной ν± ΔЕ/h. Опыт действительно показывает, что все спектральные линии размыты; измеряя ширину спектральной линии, можно оценить порядок времени существования атома в возбужденном состоянии.
33.3. Волновая функция и ее статистический смысл
Экспериментальное подтверждение идеи де Бройля об универсальности корпускулярно-волнового дуализма, ограниченность применения классической механики к микробъектам, диктуемая соотношением неопределенностей, а также противоречие целого ряда экспериментов с применяемыми в начале XX в. теориями привели к новому этапу развития квантовой теории — созданию квантовой механики, описывающей законы движения и взаимодействия микрочастиц с учетом их волновых свойств.
В квантовой механике состояние микрочастиц описывается с помощью волновой функции, которая является основным носителем информации об их корпускулярных и волновых свойствах. Вероятность нахождения частицы в элементе объемом dV равна
dW= │Ψ│2 dV. (33.6)
Величина │Ψ│2 = dW/dV - имеет смысл плотности вероятности, т. е. определяет вероятность нахождения частицы в единичном объеме в окрестности точки с координатами х, у, z. Таким образом, физический смысл имеет не сама Ψ- функция, а квадрат ее модуля |Ψ|2, которым задается интенсивность волн де Бройля.
Вероятность найти частицу в момент времени t в конечном объеме V, равна
W= ![]() =
=![]() │Ψ│2 dV. (33.7)
│Ψ│2 dV. (33.7)
Так как │Ψ│2dV определяется как вероятность, то необходимо волновую функцию Ψ нормировать так, чтобы вероятность достоверного события обращалась в единицу, если за объем V принять бесконечный объем всего пространства. Это означает, что при данном условии частица должна находиться где-то в пространстве. Следовательно, условие нормировки вероятностей
![]() │Ψ│2 dV =1, (33.8)
│Ψ│2 dV =1, (33.8)
где данный интеграл (8) вычисляется по всему бесконечному пространству, т. е. по координатам х, у, z от - ∞ до ∞. Функция Ψ должна быть конечной, однозначной, и непрерывной.
33.4 Уравнение Шредингера
Уравнением движения в квантовой механике, описывающим движение микрочастиц в различных силовых полях, должно быть уравнение, из которого вытекали бы волновые свойства частиц. Оно должно быть уравнением относительно волновой функции Ψ (х, у, z, t), так как величина │Ψ│2 определяет вероятность пребывания частицы в момент времени в объеме.
Основное уравнение сформулировано Э. Шредингером: уравнения не выводится, а постулируется.
Уравнение Шредингера имеет вид:
- ΔΨ + U(x,y, z, t)Ψ = iħ , (33.9)
где ħ=h/(2π), т—масса частицы, Δ—оператор Лапласа, i — мнимая единица, U(x,y,z,t) — потенциальная функция частицы в силовом поле, в котором она движется, Ψ (x,y, z, t) — искомая волновая функция частицы.
Уравнение (32.9) является общим уравнением Шредингера. Его также называют уравнением Шредингера, зависящим от времени. Для многих физических явлений, происходящих в микромире, уравнение (33.9) можно упростить, исключив зависимость Ψ от времени, иными словами, найти уравнение Шредингера для стационарных состояний — состояний с фиксированными значениями энергии. Это возможно, если силовое поле, в котором частица движется, стационарно, т. е. функция U(x,y,z,t) не зависит явно от времени и имеет смысл потенциальной энергии.
∆Ψ +![]() (E-U)Ψ =
(E-U)Ψ =
Уравнение (33.10) называется уравнением Шредингера для стационарных состояний.
В это уравнение в качестве параметра входит полная энергия Е частицы. Решение уравнения имеет место не при любых значениях параметра Е, а лишь при определенном наборе, характерном для данной задачи. Эти значения энергии называются собственными. Собственные значения Е могут образовывать как непрерывный и дискретный ряд.
33.5. Частица в одномерной прямоугольной «потенциальной яме с бесконечно высокими «стенками»
Свободная частица — частица, движущаяся в отсутствие внешних полей. Так как на свободную частицу (пусть она движется вдоль оси х) силы не действуют, то потенциальная энергия частицы U (х) = соnst и ее можно принять равной нулю. Тогда полная энергия частицы совпадает с ее кинетической энергией. Энергия свободной частицы может принимать любые значения, т. е. ее энергетический спектр является непрерывным. Свободная квантовая частица описывается плоской монохроматической волной де Бройля, и все положения свободной частицы в пространстве являются равновероятными.
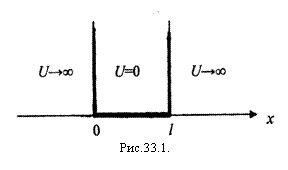 Проведем качественный анализ решений уравнения Шредингера применительно к свободной частице в одномерной прямоугольной «потенциальной яме» с бесконечно высокими «стенками» (рис.33.1). Такая «яма» описывается потенциальной энергией вида (для простоты принимаем, что частица движется вдоль оси х)
Проведем качественный анализ решений уравнения Шредингера применительно к свободной частице в одномерной прямоугольной «потенциальной яме» с бесконечно высокими «стенками» (рис.33.1). Такая «яма» описывается потенциальной энергией вида (для простоты принимаем, что частица движется вдоль оси х)
∞, х < 0
U(x) ={0, 0 ≤ х ≤ l} (33.11)
∞, х > 1
где l — ширина «ямы», а энергия отсчитывается от ее дна (рис.33.1).
Уравнение Шредингера для стационарных состояний в случае одномерной задачи запишется в виде
+ (Е - U)Ψ =0. (33.12)
По условию задачи (бесконечно высокие «стенки»), частица не проникает за пределы «ямы», поэтому вероятность ее обнаружения (а следовательно, и волновая функция) за пределами «ямы» равна нулю. На границах «ямы» (при х=0 и х=l) непрерывная волновая функция также должна обращаться в нуль. Следовательно, граничные условия в данном случае имеют вид
Ψ(0)=Ψ(l)=0. (33.13)
В пределах «ямы» уравнение Шредингера сведется к уравнению
![]() +
+ ![]() ЕΨ =0. (33.14)
ЕΨ =0. (33.14)
Стационарное уравнение Шредингера, описывающее движение частицы в «потенциальной яме» с бесконечно высокими «стенками», удовлетворяется только при собственных значениях Еп зависящих от целого числа п.
Еп= , ( n= 1, 2, 3, …). (33.15)
Следовательно, энергия Еп частицы в «потенциальной яме» с бесконечно высокими «стенками» принимает лишь определенные дискретные значения, т. е. квантуется. Квантованные значения энергии Еп - называются уровнями энергии, а число п, определяющее энергетические уровни частицы, называется главным квантовым числом. Таким образом, микрочастица в «потенциальной яме» с бесконечно высокими «стенками» может находиться только на определенном энергетическом уровне Еп, или, как говорят, частица находится в квантовом состоянии п. Частица «в потенциальной яме» с бесконечно высокими «стенками» не может иметь энергию меньшую, чем минимальная энергия, равная .
33.6. Туннельный эффект
Рассмотрим простейший потенциальный барьер прямоугольной формы (рис.33.2.а) для одномерного (по оси х) движения частицы. Для потенциального барьера прямоугольной формы высоты U ширины l можем записать
0, х < 0 (для области 1),
U(x) = {U, 0 ≤ х ≤ l} (для области 2), (33.15)
0, х > 1(для области 3),
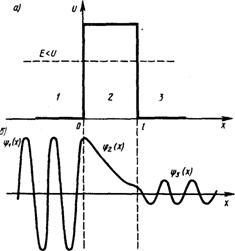 При данных условиях задачи классическая частица, обладая энергией Е, либо беспрепятственно пройдет над барьером (при Е> U), либо отразится от него (при Е< U) и будет двигаться в обратную сторону, т. е. она не может проникнуть сквозь барьер. Для микрочастицы же, даже при Е> U, имеется отличная от нуля вероятность, что частица отразится от барьера и будет двигаться в обратную сторону. При Е< U Рис.33.2.
При данных условиях задачи классическая частица, обладая энергией Е, либо беспрепятственно пройдет над барьером (при Е> U), либо отразится от него (при Е< U) и будет двигаться в обратную сторону, т. е. она не может проникнуть сквозь барьер. Для микрочастицы же, даже при Е> U, имеется отличная от нуля вероятность, что частица отразится от барьера и будет двигаться в обратную сторону. При Е< U Рис.33.2.
имеется также отличная от нуля вероятность, что частица окажется в области х>l, т. е. проникает сквозь барьер. Подобные, казалось бы, парадоксальные выводы следуют непосредственно из уравнения Шредингера, описывающего микрочастицы при условиях данной задачи.
Таким образом, квантовая механика приводит к специфическому квантовому явлению, получившему название туннельного эффекта, в результате которого микрообъект может «пройти» сквозь потенциальный барьер.
Для описання туннельного эффекта используют понятие коэффициента прозрачности D потенциального барьера, определяемого как отношение плотности потока прошедших частиц к плотности потока падающих.
Решение уравнения Шредингера для прямоугольной потенциального барьера дает формулу для коэффициента прозрачности:
D = D0 exp( - ), (33.16)
где U — высота потенциального барьера, Е — энергия частицы, l — ширина барьера, D0— постоянный множитель, который можно приравнять единице. Из этого выражения следует, что D сильно зависит от массы частицы, ширины барьера и от (U - Е); чем шире барьер, тем меньше вероятность прохождения сквозь него частицы.
С классической точки зрения прохождение частицы сквозь потенциальный барьер при Е<U невозможно, так как частица, находясь в области барьера, должна была бы обладать отрицательной кинетической энергией. Туннельный эффект является специфическим квантовым эффектом. Прохождение частицы сквозь область, в которую, согласно законам классической механики, она не может проникнуть, можно пояснить соотношением неопределенностей. Неопределенность импульса Δр на отрезке Δх=l составляет Δp>h/l. Связанная с этим разбросом в значениях импульса кинетическая энергия может сказаться достаточной для того, чтобы полная энергия частицы сказалась больше потенциальной.
Туннельное прохождение сквозь потенциальный барьер лежит в основе многих явлений физики твердого тела (например, явления в контактном слое на границе двух полупроводников), атомной и ядерной физики (например, a-распад, протекание термоядерных реакций).
ГЛАВА 34. ТЕОРИЯ АТОМА ВОДОРОДА ПО БОРУ.
КВАНТОВАЯ ТЕОРИЯ АТОМА ВОДОРОДА
34.1. Модель атома Резерфорда-Бора
Резерфорд предложил ядерную (планетарную) модель атома. Согласно этой модели, вокруг положительного ядра, имеющего заряд Ζе (Ζ — порядковый номер элемента в системе Менделеева, е — элементарный заряд), размер 10-15 – 10-14 м и массу, практически равную массе атома. В области с линейными размерами порядка 10-10 м по замкнутым орбитам движутся электроны, образуя электронную оболочку атома. Так как атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т. е. вокруг ядра должно вращаться Ζ электронов.
Считаем, что электрон движется вокруг ядра по круговой орбите радиуса r. При этом кулоновская сила взаимодействия между ядром и электроном сообщает электрону центростремительное ускорение. Второй закон Ньютона для электрона, движущегося по окружности под действием кулоновской силы, имеет вид:
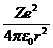 =
=![]() , (34.1)
, (34.1)
где mе, и υ — масса и скорость электрона на орбите радиуса r, ε0 — электрическая постоянная.
Уравнение (34.1) содержит два неизвестных: r и υ. Следовательно, существует бесчисленное множество значений радиуса и соответствующих ему значений скорости а значит, и энергии, удовлетворяющих этому уравнению. Поэтому величины r, υ (следовательно, и Е) могут меняться непрерывно, т. е. может испускаться любая, а не вполне определенная порция энергии. Тогда спектры атомов должны быть сплошными. В действительности же опыт показывает, что атомы имеют линейчатый спектр. Из выражения (34.1) следует, что при r~10-10 м скорость движения электронов - υ~106 м/с, а ускорение ~ 1022 м/с2. Согласно классической электродинамике, ускоренно движущиеся электроны должны излучать электромагнитные волны и вследствие этого непрерывно терять энергию. В результате электроны будут приближаться к ядру и, в конце концов, упадут на него. Таким образом, атом Резерфорда оказывается неустойчивой системой, что опять-таки противоречит действительности.
Попытки построить модель атома в рамках классической физики не привели к успеху. Преодоление возникших трудностей потребовало создания качественно новой — квантовой — теории атома.
Исследования спектров излучения разреженных газов (т. е. спектров излучения отдельных атомов) показали, что каждому газу присущ определенный линейчатый спектр, состоящий из отдельных спектральных линий или групп близко расположенных линий. Самым изученным является спектр наиболее простого атома — атома водорода.
И. Бальмер подобрал эмпирическую формулу, описывающую все известные в то время спектральные линии атома водорода в видимой области спектра:
ν= R![]() (n =3, 4, 5, ...), (34.2)
(n =3, 4, 5, ...), (34.2)
где R =3,29×1015 с-1 —постоянная Ридберга.
Из выражения (34.2) вытекает, что спектральные линии, отличающиеся различными значениями п, образуют группу или серию линий, называемую серией Бальмера.
В спектре атома водорода было обнаружено еще несколько серий.
В ультрафиолетовой области спектра находится серия Лаймана:
ν= R (n =2, 3, 4, 5, ...),
В инфракрасной области спектра были также обнаружены:
Серия Пашена ν= R 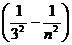 (n = 4, 5, 6,...),
(n = 4, 5, 6,...),
Серия Брэкета ν= R 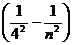 (n = 5, 6, 7,...),
(n = 5, 6, 7,...),
Серия Пфунда ν= R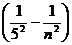 (n = 6, 7, 8,...),
(n = 6, 7, 8,...),
Серия Хэмфри ν= R 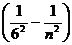 (n = 7, 8, 9,...),
(n = 7, 8, 9,...),
Все приведенные выше серии в спектре атома водорода могут быть описаны одной формулой, называемой обобщенной формулой Бальмера:
ν = R , (34.3)
где т имеет в каждой данной серии постоянное значение, т = 1, 2, 3, 4, 5, 6 (определяет серию), п принимает целочисленные значения начиная с т+1 (определяет отдельные линии этой серии).
Приведенные выше сериальные формулы подобраны эмпирически и долгое время не имели теоретического обоснования, хотя и были подтверждены экспериментально с очень большой точностью.
34.2. Постулаты Бора
Первая попытка построить качественно новую — квантовую — теорию атома предпринята Нильсом Бором. Он поставил перед собой цель связать в единое целое эмпирические закономерности линейчатых спектров, ядерную модель атома Резерфорда и квантовый характер излучения и поглощения света. В основу своей теории Бор положил два постулата.
Первый постулат Бора (постулат стационарных состояний): в атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн.
В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантованные значения момента импульса, удовлетворяющие условию
mе υ rn = n ћ (n= 1, 2, 3,…) (34. 4)
где mе, — масса электрона, υ — его скорость по n - й орбите радиуса rn, ћ=h/2π.
Второй постулат Бора (правило частот): при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией
hv = Е n - Еm (34.5)
равной разности энергии соответствующих стационарных состояний (Е n и Еm — соответственно энергии стационарных состояний атома до и после излучения (поглощения)). При Еm < Еn происходит излучение фотона (переход атома из состояния с большей энергией в состояние с меньшей энергией, т. е. переход электрона с более удаленной от ядра орбиты на более близлежащую), при Еm >Еn, —его поглощение (переход атома из состояния с меньшей энергией в состояние с большей энергией, т. е. переход электрона на более удаленную от ядра орбиту). Набор возможных дискретних частот v = (Еn - Еm)/h квантовых переходов и определяет линейчатый спектр атома.
34.3. Спектр атома водорода по Бору
Постулаты, выдвинутые Бором, позволили рассчитать спектр атома водорода и водородоподобных систем — систем, состоящих из ядра с зарядом Zе и одного электрона (например, ионы Не+ , Lі2+ ), а также теоретически вычислить постоянную Ридберга.
Рассмотрим движение электрона в водородоподобной системе, ограничиваясь круговыми стационарными орбитами.
Радиус n-й стационарной орбиты:
rn = n2 , (34.6)
где n = 1, 2, 3, ... . Из выражения (34.6) следует, что радиусы орбит растут пропорционально квадратам целых чисел.
Для атома водорода (Z=1) радиус первой орбиты электрона при п=1, называемый первым боровским радиусом, равен
r1 = а = ![]() = 52,8 пм, (34.7)
= 52,8 пм, (34.7)
Полная энергия электрона в водородоподобной системе складывается из его кинетической энергии (mеυ2/2) и потенциальной энергии в электростатическом поле ядра (-Ze2/4πε0r):
Е =(mеυ2/2) - (Ze2/4πε0r)= -½ (Ze2/4πε0r)
учли, что (mеυ2/2) = ½(Ze2/4πε0r). Учитывая квантованные для радиуса n-й стационарной орбиты значения (34.6), получим, что энергия электрона может принимать только следующие дозволенные дискретные значения:
Еn = -![]()
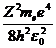 (n= 1,2,3,…), (34.8)
(n= 1,2,3,…), (34.8)
где знак минус означает, что электрон находится в связанном состоянии.
Из формулы (34.8) следует, что энергетические состояния атома образуют последовательность энергетических уровней, изменяющихся в зависимости от значения п. Целое число n в выражении (34.8), определяющее энергетические уровни атома, называется главным квантовым числом. Энергетическое состояние с п=1 является основным (нормальным) состоянием; состояния с n>1 являются возбужденными. Энергетический уровень, соответствующий основному состоянию атома, называется основным (нормальным) уровнем; все остальные уровни являются возбужденными.
Придавая n различные целочисленные значения, получим для атома водорода (Z = 1), согласно формуле (33.8), возможные уровни энергии. Энергия атома водорода с увеличением n возрастает и энергетические уровни сближаются к границе, соответствующей значению n=∞. Атом водорода обладает, таким образом, минимальной энергией (Е1=-13,55эВ) при п=1 максимальной (Е∞ =0) при п= ∞. Следовательно, значение Е∞ =0 соответствует ионизации атома (отрыву от него электрона). Согласно второму постулату Бора, при переходе атома водорода (Z= 1) из стационарного состояния п в стационарное состояние т с меньшей энергией испускается квант
hν = Е n - Еm = - , (34.9)
откуда частота излучения
ν = = R , (34.10)
где R= .
Воспользовавшись при вычислении R современными значениями универсальных постоянных, получим величину, совпадающую с экспериментальным значением постоянной Ридберга в эмпирических формулах для атома водорода.
Подставляя, например, в формулу (34.10) m =1 и п=2, 3, 4, ..., получим группу линий, образующих серию Лаймана и соответствующих переходам электронов с возбужденных уровней (n=2, 3, 4, ...) на основной (m=1). Аналогично, при подстановке m = 2, 3, 4, 5, 6 и соответствующих им значений n получим серии Бальмера, Пашена, Брэкета, Пфунда и Хэмфри.
Следовательно, по теории Бора, спектральные серии соответствуют излучению, возникающему в результате перехода атома в данное состояние из возбужденных состояний расположенных выше данного.
Спектр поглощения атома водорода является линейчатым, но содержит при нормальных условиях только серию Лаймана. Он также объясняется теорией Бора. Так как свободные атомы водорода обычно находятся в основном состоянии (стационарное состояние с наименьшей энергией при n=1), то при сообщении атомам извне определенной энергии могут наблюдаться лишь переходы атомов из основного состояния в возбужденные (возникает серия Лаймана).
Теория Бора обладает внутренними противоречиями (с одной стороны, применяет законы классической физики, а с другой — основывается на квантовых постулатах). В теории Бора рассмотрены спектры атома водорода и водородоподобных систем и вычислены частоты спектральных линий, однако эта теория не смогла объяснить интенсивности спектральных линий и ответить на вопрос: почему совершаются те или иные переходы? Серьезным недостатком теории Бора была невозможность описания с ее помощью спектра атома гелия — одного из простейших атомов, непосредственно следующего за атомом водорода.
34.4. Атом водорода в квантовой механике
Решение задачи об энергетических уровнях электрона для атома водорода (а также водородоподобных систем: иона гелия Не+) сводится к задаче о движении электрона в кулоновском поле ядра.
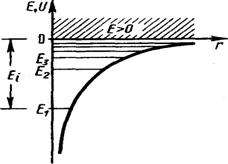 Потенциальная энергия U(r) взаимодействия электрона с ядром, обладающим зарядом Zе (для атома водорода Z= 1),
Потенциальная энергия U(r) взаимодействия электрона с ядром, обладающим зарядом Zе (для атома водорода Z= 1),
U(r) = - ![]() , (34.11)
, (34.11)
где r— расстояние между электроном и ядром. Графически функция U(r) изображена жирной кривой на рис.34.1. U(r) с уменьшением r при приближении электрона к ядру неограниченно убывает. Рис.34.1.
Состояние электрона в атоме водорода описывается волновой функцией Ψ, удовлетворяющей стационарному уравнению Шредингера:
ΔΨ + (Е + )Ψ = 0, (34.12)
где m — масса электрона, Е — полная энергия электрона в атоме. Не вдаваясь в математическое решение этой задачи, ограничимся рассмотрением важнейших результатов, которые из него следуют, пояснив их физический смысл.
1. Энергия. Такие уравнения имеют решения, удовлетворяющие требованиям однозначности, конечности и непрерывности волновой функции Ψ, только при собственных значениях энергии
Е= -![]() (п=1,2,3…) (34.13)
(п=1,2,3…) (34.13)
т. е. для дискретного набора отрицательных значений энергии.
Решение уравнения Шредингера для атома водорода приводит к появлению дискретных энергетических уровней. Возможные значения Е1, Е2,, Е3 — показаны на рис. в виде горизонтальных прямых. Самый нижний уровень Е1, отвечающий минимальной возможной энергии, основной, все остальные (Еn>Е1, п=2, 3, ...) — возбужденные. При Е<0 движение электрона является связанным — он находится внутри гиперболической «потенциальной ямы». Из рисунка следует, что по мере роста главного квантового числа п энергетические уровни располагаются теснее и при п=∞ Е∞=0. При Е>0 движение электрона является свободным; область непрерывного спектра Е>0 (заштрихована на рис.34.1) соответствует ионизованному атому. Энергия ионизации атома водорода равна
Еi = - Е1 = ![]() =13,55 эВ. (34.14)
=13,55 эВ. (34.14)
Выражение совпадает с формулой, полученной Бором для энергии атома водорода. Однако если Бору пришлось вводить дополнительные гипотезы (постулаты), то в квантовой механике дискретные значения энергии, являясь следствием самой теории, вытекают непосредственно из решения уравнения Шредингера.
Решение уравнения Шредингера, т. е. математическое описание орбитали, возможно лишь при определенных, дискретных значениях характеристик, получивших название квантовых чисел.
Главное квантовое число n определяет основной запас энергии электрона, т. е. степень его удаления от ядра, или размер электронного облака (орбитали). Оно может принимать целочисленные значения от 1 до ∞.
Состояние электрона, характеризующееся определенным значением n, называется энергетическим уровнем электрона в атоме. Электроны, имеющие одинаковые значения n, образуют электронные слои (электронные оболочки), обозначаемые цифрами 1,2,3,4,5… или соответственно буквами: K, L, M, N, O…
Наименьшее значение энергии Е соответствует n=1. Остальным квантовым состояниям отвечают более высокие значения энергий, и электроны, находящиеся на этих энергетических уровнях, менее прочно связаны с ядром.
Орбитальное (побочное или азимутальное) квантовое число l определяет орбитальный момент количества движения электрона l =![]()
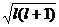 и характеризует форму электронного облака (рис.34.2). Оно принимает все целочисленные значения от 0 до (n-1). Каждому n соответствует определенное число значений орбитального квантового числа, т. е. энергетический уровень представляет собой совокупность энергетических подуровней, несколько различающихся по энергиям. Число подуровней, на которые расщепляется уровень, равно номеру уровня (т. е. численному значению n). Эти подуровни имеют следующие буквенные обозначения:
и характеризует форму электронного облака (рис.34.2). Оно принимает все целочисленные значения от 0 до (n-1). Каждому n соответствует определенное число значений орбитального квантового числа, т. е. энергетический уровень представляет собой совокупность энергетических подуровней, несколько различающихся по энергиям. Число подуровней, на которые расщепляется уровень, равно номеру уровня (т. е. численному значению n). Эти подуровни имеют следующие буквенные обозначения:
Орбитальное квантовое число:
Подуровень s p d f g
Формы орбиталей, соответствующие различным значениям l
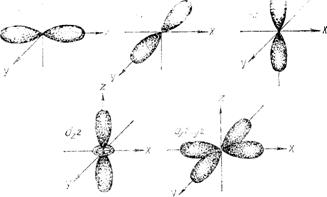


Рис.34.2
Таким образом, энергетический подуровень - это состояние электрона в атоме, характеризующееся определенным набором квантовых чисел n, l. Такое состояние электрона, соответствующее определенным значениям n и l (т. е. тип орбитали), записывается в виде сочетания цифрового обозначения n и буквенного l, например:4р (n=4; l=1); 5d (n =5; l =2).
Магнитное квантовое число ml определяет значение орбитального момента количества движения электрона L на произвольно выделенную ось z: Lz =![]() ml, т. е. характеризует пространственную ориентацию электронного облака. Оно принимает все целочисленные значения от – l до + l, например, при l=0 ml =0, при l=1 ml =-1,0,+1; при l=2 ml =-2,-1,0,+1,+2
ml, т. е. характеризует пространственную ориентацию электронного облака. Оно принимает все целочисленные значения от – l до + l, например, при l=0 ml =0, при l=1 ml =-1,0,+1; при l=2 ml =-2,-1,0,+1,+2
В общем виде любому значению при l соответствует (2l+1) значений магнитного квантового числа, т. е. (2l+1) возможных расположений электронного облака данного типа в пространстве. Следовательно, можно говорить, что число значений n указывает на число орбиталей с данным значением l. s –состоянию соответствует одна орбиталь, p - состоянию –три, d—состоянию – пять, f –состоянию семь. Все орбитали, соответствующие какому-либо состоянию, имеют одинаковую энергию и называются вырожденными.
Общее число орбиталей, из которых состоит любой энергетический уровень, равно n2, а число орбиталей, составляющих подуровень - (2l+1).
Состояние электрона в атоме, характеризующееся определенными значениями квантовых чисел n, l, ml,, т. е. определенными размерами, формой и ориентацией в пространстве электронного облака, называется атомной электронной оболочкой.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |




