Спиновое квантовое число S характеризует собственный механический момент электрона, связанный с вращением его вокруг своей оси. Оно может иметь только два значения +1/2 или –1/2.
Общая характеристика состояния электрона в многоэлектронном атоме определяется принципом Паули: в атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковы.
Следовательно, на одной орбитали могут находится не более двух электронов, отличающихся друг от друга значениями спинового квантового числа; максимальная емкость энергетического подуровня 2(2l+1) электронов, а уровня 2n2.
34.5. Спин электрона
Штерн и Герлах обнаружили, что узкий пучок атомов водорода, заведомо находящихся в s-состоянии, в неоднородном магнитном поле расщепляется на два пучка. В этом состоянии момент импульса электрона равен нулю. Магнитный момент атома, связанный с орбитальным движением электрона, пропорционален механическому моменту, поэтому он равен нулю и магнитное поле не должно оказывать влияния на движение атомов водорода в основном состоянии, т. е. расщепления быть не должно. Однако в дальнейшем при применении спектральных приборов с большой разрешающей способностью было доказано, что спектральные линии атома водорода обнаруживают тонкую структуру (являются дублетами) даже в отсутствие магнитного поля.
Для объяснения тонкой структуры спектральных линий, а также ряда других трудностей в атомной физике Д. Уленбек и С. Гаудомит предположили, что электрон обладает собственным неуничтожимым механическим моментом импульса, не связанным с движением электрона в пространстве, — спином.
Спин электрона (и всех других микрочастиц) — квантовая величина, у нее нет классического аналога; это внутреннее неотъемлемое свойство электрона, подобное его заряду и массе.
Если электрону приписывается собственный механический момент импульса (спин) Ls то ему соответствует собственный магнитный момент рms. Согласно общим выводам квантовой механики, спин квантуется по закону
Ls =ћ![]() , (34.15)
, (34.15)
где s— спиновое квантовое число.
По аналогии с орбитальным моментом импульса, проекция Lsz спина квантуется так, что вектор Ls, может принимать 2s +1 ориентации. Так как в опытах Штерна и Герлаха наблюдались только две ориентации, то 2 s +1=2, откуда s = 1/2. Проекция спина на направление внешнего магнитного поля, являясь квантованной величиной, определяется выражением
Lsz= ћms (34.16)
где ms — магнитное спиновое квантовое число; оно может иметь только два значения: ms =±1/2.
Таким образом, опытные данные привели к необходимости характеризовать электроны (и микрочастицы вообще) добавочной внутренней степенью свободы. Поэтому для полного описания состояния электрона в атоме необходимо наряду с главным, орбитальным и магнитным квантовыми числами задавать еще магнитное спиновое квантовое число.
34.6. Спектры. Спектральный анализ
Спектры излучения. Спектральный состав излучения у различных веществ имеет весьма разнообразный характер. Однако все спектры делятся на три типа: а) сплошной спектр; б) линейчатый спектр; в) полосатый спектр.
а) Сплошной (непрерывный) спектр. Накаленные твердые и жидкие тела и газы (при большом давлении) испускают свет, разложение которого дает сплошной спектр, в котором спектральные цвета непрерывно переходят один в другой. Характер непрерывного спектра и сам факт его существования определяются не только свойствами отдельных излучающих атомов, но и взаимодействием атомов друг с другом. Сплошные спектры одинаковы для разных веществ, и поэтому их нельзя использовать для определения состава вещества.
б) Линейчатый (атомный) спектр. Возбужденные атомы разреженных газов или паров испускают свет, разложение которого дает линейчатый спектр, состоящий из отдельных цветных линий. Каждый химический элемент имеет характерный для него линейчатый спектр. Атомы таких веществ не взаимодействуют друг с другом и излучают свет только определенных длин волн. Изолированные атомы данного химического элемента излучают строго определенные длины волн. Это позволяет по спектральным линиям судить о химическом составе источника света.
в) Молекулярный (полосатый) спектр. Спектр молекулы состоит из большого числа отдельных линий, сливающихся в полосы, четкие с одного края и размытые с другого. В отличие от линейчатых спектров полосатые спектры создаются не атомами, а молекулами, не связанными или слабо связанными друг с другом. Серии очень близких линий группируются на отдельных участках спектра и заполняют целые полосы. В 1860 г. немецкие ученые Г. Кирхгоф и Р. Бунзен, изучая спектры металлов, установили следующие факты:
1) каждый металл имеет свой спектр;
2) спектр каждого металла строго постоянен;
3) введение в пламя горелки любой соли одного и того же металла всегда приводит к появлению одинакового спектра;
4) при внесении в пламя смеси солей нескольких металлов в спектре одновременно появляются все их линии;
5) яркость спектральных линий зависит от концентрации элемента в данном веществе.
Спектры поглощения. Если белый свет от источника, дающей сплошной спектр, пропускается через пары исследуемого вещества и затем разлагается в спектр, то на фоне сплошного спектра наблюдаются темные линии поглощения в тех же самых местах, где находились бы линии спектра испускания паров исследуемого элемента. Такие спектры получили название атомных спектров поглощения.
Все вещества, атомы которых находятся в возбужденном состоянии, излучают световые волны, энергия которых определенным образом распределена по длинам волн. Поглощение света веществом также зависит от длины волны. Атомы поглощают излучение лишь тех длин волн, которые они могут испускать при данной температуре.
Спектральный анализ. Явление дисперсии используется в науки и технике в виде метода определения состава вещества, получившего название спектрального анализа. В основе этого метода лежит изучение света, излучаемого или поглощаемого веществом. Спектральным анализом называется метод изучения химического состава вещества, основанный на исследовании его спектров.
Спектральные аппараты. Для получения и исследования спектров используют спектральные аппараты. Наиболее простые спектральные приборы — призма и дифракционная решетка. Более точные — спектроскоп и спектрограф.
Спектроскопом называется прибор, с помощью которого визуально исследуется спектральный состав света, испускаемого некоторым источником. Если регистрация спектра происходит на фотопластинке, то прибор называется спектрографом.
Применение спектрального анализа. Линейчатые спектры играют особо важную роль, потому что их структура прямо связана со строением атома. Ведь эти спектры создаются атомами, не испытывающими внешних воздействий. Состав сложных, главным образом органических смесей анализируется по их молекулярным спектрам.
С помощью спектрального анализа можно обнаружить данный элемент в составе сложного вещества, если даже его масса не превышает 10-10 г. Линии, присущие данному элементу, позволяют качественно судить о его наличии. Яркость линий дает возможность (при соблюдении стандартных условий возбуждения) количественно судить о наличии того или иного элемента.
Спектральный анализ можно проводить и по спектрам поглощения. В астрофизике по спектрам можно определить многие физические характеристики объектов: температуру, давление, скорость движения, магнитную индукцию и др. с помощью спектрального анализа определяют химический состав руд и минералов.
Основные направления применения спектрального анализа таковы: физико-химические исследования; машиностроение, металлургия; атомная индустрия; астрономия, астрофизика; криминалистика.
Современные технологии создания новейших строительных материалов (металлопластиковые, пластиковые) непосредственно взаимосвязаны с такими фундаментальными науками как химия, физика. Данные науки используют современные методы исследования веществ. Поэтому спектральный анализ можно применять для определения химического состав состава строительных материалов по их спектрам.
ГЛАВА 35. ЭЛЕМЕНТЫ ЗОННОЙ ТЕОРИИ ТВЕРДЫХ ТЕЛ
35.1. Кристаллы. Связи между атомами и молекулами в твердых телах
Каждая частица в кристаллической решетке (ион, атом или молекула) испытывает силы межмолекулярного взаимодействия. Равновесное расположение всех частиц твердого тела в узлах кристаллической решетки соответствует минимуму свободной энергии кристалла и наиболее устойчивому его состоянию. При этом частицы в узлах решетки располагаются на некоторых равновесных расстояниях ![]() друг от друга, называемых периодом кристаллической решетки.
друг от друга, называемых периодом кристаллической решетки.
 В зависимости от того, какие частицы находятся в узлах кристаллической решетки, различают следующие четыре типа решеток: ионную, атомную, молекулярную и металлическую.
В зависимости от того, какие частицы находятся в узлах кристаллической решетки, различают следующие четыре типа решеток: ионную, атомную, молекулярную и металлическую.
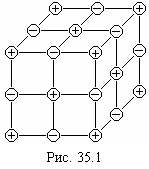
 В узлах ионной решетки чередуются отрицательные и положительные ионы. Благодаря электрическим взаимодействиям они образуют устойчивую структуру кристалла. Подавляющее большинство кристаллов имеют именно ионную решетку. Типичным примером ионной решетки является изображенная на рис. 35.1 решетка каменной соли
В узлах ионной решетки чередуются отрицательные и положительные ионы. Благодаря электрическим взаимодействиям они образуют устойчивую структуру кристалла. Подавляющее большинство кристаллов имеют именно ионную решетку. Типичным примером ионной решетки является изображенная на рис. 35.1 решетка каменной соли ![]() . В ней чередуются ионы
. В ней чередуются ионы ![]() и
и ![]() . В газообразном состоянии хлористый натрий состоит из молекул, в которых объединены попарно ионы натрия с ионами хлора. В кристалле молекулы утрачивают обособленное существование. Ионный кристалл состоит не из молекул, а из ионов. Весь кристалл в целом можно рассматривать как одну гигантскую молекулу.
. В газообразном состоянии хлористый натрий состоит из молекул, в которых объединены попарно ионы натрия с ионами хлора. В кристалле молекулы утрачивают обособленное существование. Ионный кристалл состоит не из молекул, а из ионов. Весь кристалл в целом можно рассматривать как одну гигантскую молекулу.
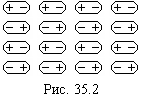
В узлах молекулярной решетки (см. рис. 35.2) размещаются полярные молекулы. Разноименно заряженные частицы двух соседних молекул притягиваются и связывают молекулы в кристаллическую решетку. Таким образом, между молекулами кристалла действуют те же силы, что и между молекулами реального газа. Эти силы называют еще силами Ван-дер-Ваальса. По сравнению с ионными, молекулярные решетки не такие прочные, они легко деформируются. Такие решетки имеют вода (лед), углекислота (сухой лед), азот, кислород, водород, а также резина, парафин, целлюлоза и многие другие кристаллы.
В атомных решетках нейтральные атомы соседних узлов связаны между собой валентными электронами. Орбиты электронов смещаются так, что электрон движется по орбите, охватывающей два соседних атома, и таким образом, связывает их между собой. Так осуществляется связь атомов в молекулах с ковалентной связью.
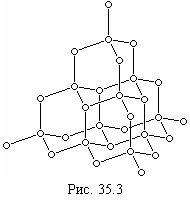 В качестве примера рассмотрим атомные решетки алмаза и графита. Эти кристаллы идентичны по своей химической природе – они построены из атомов углерода, но отличаются строением решетки. В кристалле алмаза (см. рис. 35.3) соседние атомы углерода размещены на одинаковом расстоянии 154 пм друг от друга. Они одинаково и очень тесно связаны во всех направлениях, что является причиной чрезвычайной прочности и твердости алмаза. Каждый четырехвалентный атом углерода размещается в центре правильной четырехгранной пирамиды – тетраэдра, в вершинах которой находятся четыре его ближайших соседа, с которыми он связан валентной связью. Такую же решетку, как у алмаза, имеют типичные полупроводники – германий
В качестве примера рассмотрим атомные решетки алмаза и графита. Эти кристаллы идентичны по своей химической природе – они построены из атомов углерода, но отличаются строением решетки. В кристалле алмаза (см. рис. 35.3) соседние атомы углерода размещены на одинаковом расстоянии 154 пм друг от друга. Они одинаково и очень тесно связаны во всех направлениях, что является причиной чрезвычайной прочности и твердости алмаза. Каждый четырехвалентный атом углерода размещается в центре правильной четырехгранной пирамиды – тетраэдра, в вершинах которой находятся четыре его ближайших соседа, с которыми он связан валентной связью. Такую же решетку, как у алмаза, имеют типичные полупроводники – германий ![]() и кремний
и кремний ![]() .
.
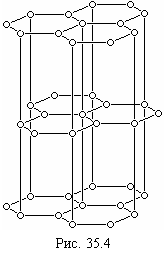 Кристаллическая решетка графита (см. рис. 35.4) имеет совершенно другое строение. Она состоит из ряда параллельных слоев атомов. Каждый слой заполнен тесно связанными между собой атомами углерода, размещенными в вершинах правильного шестиугольника на расстоянии 142 пм друг от друга. Между соседними атомами, лежащими в одном слое, осуществляется прочная валентная связь Атомы соседних слоев слабо связаны друг с другом, так как расстояние между соседними слоями более чем вдвое превышает расстояние между атомами шестиугольника и равняется 340 пм. В этом направлении связь осуществляется слабыми силами Ван-дер-Ваальса. Поэтому кристалл графита легко скалывается вдоль этих слоев (плоскостей спайности), он мягок и легко крошится. Это позволяет изготовлять из графита грифели карандашей, щетки электродвигателей, сухие смазки, используемые, например, для уменьшения трения между листами рессоры автомобиля. Поскольку лишь три валентных электрона атома углерода из четырех принимают участие в образовании валентных связей с соседними атомами, четвертый электрон оказывается слабо связанным с атомом. Именно такие электроны обеспечивают электропроводность графита, тогда как алмаз не является проводником электрического тока.
Кристаллическая решетка графита (см. рис. 35.4) имеет совершенно другое строение. Она состоит из ряда параллельных слоев атомов. Каждый слой заполнен тесно связанными между собой атомами углерода, размещенными в вершинах правильного шестиугольника на расстоянии 142 пм друг от друга. Между соседними атомами, лежащими в одном слое, осуществляется прочная валентная связь Атомы соседних слоев слабо связаны друг с другом, так как расстояние между соседними слоями более чем вдвое превышает расстояние между атомами шестиугольника и равняется 340 пм. В этом направлении связь осуществляется слабыми силами Ван-дер-Ваальса. Поэтому кристалл графита легко скалывается вдоль этих слоев (плоскостей спайности), он мягок и легко крошится. Это позволяет изготовлять из графита грифели карандашей, щетки электродвигателей, сухие смазки, используемые, например, для уменьшения трения между листами рессоры автомобиля. Поскольку лишь три валентных электрона атома углерода из четырех принимают участие в образовании валентных связей с соседними атомами, четвертый электрон оказывается слабо связанным с атомом. Именно такие электроны обеспечивают электропроводность графита, тогда как алмаз не является проводником электрического тока.
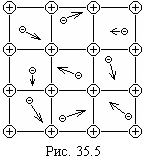 В узлах металлической решетки (см. рис. 35.5) размещены положительные ионы металла. В пространстве между узлами решетки двигаются свободные (точнее – коллективизированные) электроны. Эти электроны не принадлежат отдельным атомам, а движутся по сложным орбитам, охватывающим весь металл. Таким образом, междоузельное пространство заполнено своеобразным “электронным газом”, который стягивает, “склеивает” положительные ионы в плотную кристаллическую решетку. Наличием свободных электронов объясняется хорошая электропроводность металлов.
В узлах металлической решетки (см. рис. 35.5) размещены положительные ионы металла. В пространстве между узлами решетки двигаются свободные (точнее – коллективизированные) электроны. Эти электроны не принадлежат отдельным атомам, а движутся по сложным орбитам, охватывающим весь металл. Таким образом, междоузельное пространство заполнено своеобразным “электронным газом”, который стягивает, “склеивает” положительные ионы в плотную кристаллическую решетку. Наличием свободных электронов объясняется хорошая электропроводность металлов.
35.2. Зоны энергетических уровней электронов в кристалле
При объединении атомов в кристалл орбитали электронов внешних электронных оболочек (валентных электронов) перекрываются и образуют электронное облако, охватывающее (пронизывающее, омывающее) всю кристаллическую решетку. Каждый валентный электрон принадлежит уже не отдельному атому, а всему кристаллу в целом. Поэтому кристалл и его 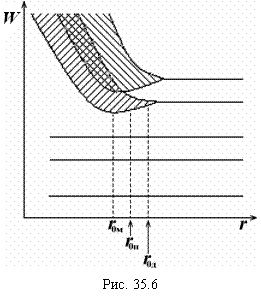 валентные электроны образуют единую квантовую систему. Электронные энергетические уровни (в том числе и незаполненные) при этом расщепляются, каждый на
валентные электроны образуют единую квантовую систему. Электронные энергетические уровни (в том числе и незаполненные) при этом расщепляются, каждый на ![]() подуровней, где
подуровней, где ![]() – общее число атомов в кристалле, образуя зону разрешенных значений энергии электронов или разрешенную зону. Разрешенные энергетические зоны разделены зонами запрещенных значений энергии электронов или запрещенными зонами. В соответствии с принципом Паули на каждом из этих подуровней может находиться не более двух электронов.
– общее число атомов в кристалле, образуя зону разрешенных значений энергии электронов или разрешенную зону. Разрешенные энергетические зоны разделены зонами запрещенных значений энергии электронов или запрещенными зонами. В соответствии с принципом Паули на каждом из этих подуровней может находиться не более двух электронов.
Деформация орбиталей и расщепление энергетических уровней происходит под действием электрических и магнитных полей соседних атомов. Действие этих полей усиливается при сближении атомов. На электроны внутренних электронных оболочек соседние атомы оказывают значительно меньшее воздействие, поэтому уширение энергетических уровней этих электронов ничтожно. На рис. 35.6 показано образование разрешенных зон, а затем и их уширение при сближении атомов в процессе формирования кристаллической решетки. Здесь ![]() – энергия электрона,
– энергия электрона, ![]() – расстояние между атомами,
– расстояние между атомами, ![]() – межатомное расстояние в недеформированном кристалле.
– межатомное расстояние в недеформированном кристалле.
Электрические свойства кристаллов определяются строением энергетических зон электронов. На рис. 35.6 верхний энергетический уровень не заполнен и при уширении образует свободную зону. Второй сверху энергетический уровень образует заполненную валентную зону. Ниже расположены практически нерасщепляющиеся заполненные энергетические уровни электронов внутренних оболочек.
Значения энергии электронов сравнительно невелики, а поэтому для их измерения часто пользуются не джоулем, а внесистемной единицей электрон-вольт (эВ). ![]() – это энергия, полученная электроном, ускоренным электростатическим полем между точками с разностью потенциалов 1 В.
– это энергия, полученная электроном, ускоренным электростатическим полем между точками с разностью потенциалов 1 В.
35.3. Проводники, полупроводники и диэлектрики по зонной теории
Полупроводники – это кристаллические вещества, у которых ширина запрещенной зоны – энергетической щели между валентной, заполненной при низкой температуре, и свободной зоной – не превышает 4 эВ. Это примерно в 100 раз больше средней тепловой энергии атомов при комнатной температуре ![]() . На рис. 35.6 полупроводникам соответствует межатомное расстояние
. На рис. 35.6 полупроводникам соответствует межатомное расстояние ![]() . У диэлектриков ширина запрещенной зоны
. У диэлектриков ширина запрещенной зоны 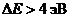 . На рис. 34.6 диэлектрикам соответствует межатомное расстояние
. На рис. 34.6 диэлектрикам соответствует межатомное расстояние ![]() . У металлов валентная зона заполнена только наполовину или в результате перекрытия заполненной валентной зоны и свободной зоны образуется частично заполненная гибридная зона. Последнему случаю соответствует межатомное расстояние
. У металлов валентная зона заполнена только наполовину или в результате перекрытия заполненной валентной зоны и свободной зоны образуется частично заполненная гибридная зона. Последнему случаю соответствует межатомное расстояние ![]() на рис. 35.6
на рис. 35.6
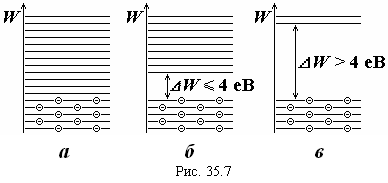 Частично заполненная разрешенная зона металла (см. рис. 35.7а) называется зоной проводимости, потому что зазор между подуровнями в пределах разрешенной зоны
Частично заполненная разрешенная зона металла (см. рис. 35.7а) называется зоной проводимости, потому что зазор между подуровнями в пределах разрешенной зоны ![]() , под действием внешнего электрического полем электроны могут ускоряться, переходя на более высокие подуровни в пределах зоны проводимости. Электроны валентной зоны диэлектрика (см. рис. 35.7в) не могут ускоряться внешним электрическим полем, потому что в валентной зоне нет свободных подуровней, на которые они могли бы перейти, а анергию, достаточную для преодоления запрещенной зоны и перехода в свободную зону внешнее электрическое поле не может им сообщить. В полупроводниках при температурах близких к абсолютному нулю (см. рис. 35.7б) имеет место та же ситуация, что и в диэлектриках.
, под действием внешнего электрического полем электроны могут ускоряться, переходя на более высокие подуровни в пределах зоны проводимости. Электроны валентной зоны диэлектрика (см. рис. 35.7в) не могут ускоряться внешним электрическим полем, потому что в валентной зоне нет свободных подуровней, на которые они могли бы перейти, а анергию, достаточную для преодоления запрещенной зоны и перехода в свободную зону внешнее электрическое поле не может им сообщить. В полупроводниках при температурах близких к абсолютному нулю (см. рис. 35.7б) имеет место та же ситуация, что и в диэлектриках.
35.4. Собственная проводимость полупроводников
 В полупроводниках, в отличие от диэлектриков, для перехода электрона из валентной зоны в зону проводимости нужна сравнительно небольшая энергия (
В полупроводниках, в отличие от диэлектриков, для перехода электрона из валентной зоны в зону проводимости нужна сравнительно небольшая энергия (![]() ). Такой переход возможен благодаря тепловому возбуждению при комнатных температурах, а также под действием света, достаточно сильного внешнего электрического поля и других факторов. Электроны, попавшие в свободную зону полупроводника, могут принимать участие в электропроводности, перемещаясь между незанятыми подуровнями. Поэтому свободную зону полупроводника, в которую перескочили электроны из валентной зоны, называют зоной проводимости. Движение электронов зоны проводимости полупроводника под действием внешнего электрического поля создает электронную проводимость.
). Такой переход возможен благодаря тепловому возбуждению при комнатных температурах, а также под действием света, достаточно сильного внешнего электрического поля и других факторов. Электроны, попавшие в свободную зону полупроводника, могут принимать участие в электропроводности, перемещаясь между незанятыми подуровнями. Поэтому свободную зону полупроводника, в которую перескочили электроны из валентной зоны, называют зоной проводимости. Движение электронов зоны проводимости полупроводника под действием внешнего электрического поля создает электронную проводимость.
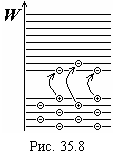
Электроны, переброшенные в зону проводимости, освобождают в валентной зоне энергетические уровни. Эти незаполненные электронами энергетические состояния (вакансии) в валентной зоне называются дырками. Электроны валентной зоны могут теперь участвовать в электропроводности, перемещаясь между подуровнями, освободившимися в верхней части валентной зоны. Электропроводность, обусловленную перемещением электронов валентной зоны, удобнее рассматривать как движение дырок. Поэтому она называется дырочной электропроводностью. На рис. 35.8 показано, как в результате перескока электрона из валентной зоны в зону проводимости возникают электроны проводимости в зоне проводимости и дырки в валентной зоне.
Согласно классическим представлениям, при объединении атомов металла в кристалл все валентные электроны отрываются от атомов и, хаотически перемещаясь между атомами кристаллической решетки, образуют электронный газ. Валентные электроны диэлектрика от атомов не отрываются, а отдельные валентные электроны полупроводников могут отрываться от атомов при тепловом возбуждении или под действием других факторов. На месте оторванного электрона образуется вакансия – дырка. Под действием внешнего электрического поля валентный электрон может перескочить из соседнего атома и заполнить вакансию. Этот процесс удобно трактовать как перемещение дырки на соседний атом. Таким образом, под движением дырки мы понимаем перемещение положительного заряда, обусловленное переходами “связанных” электронов валентной зоны.
Электропроводность чистых полупроводников, обусловленную направленным движением свободных электронов зоны проводимости и встречным перемещением связанных электрических зарядов – дырок валентной зоны, называют собственной проводимостью.
35.5. Уровень Фéрми
 Распределение электронов по уровням валентной зоны и зоны проводимости описывается функцией Фéрми–Дирáка, задающей вероятность того, что состояние с энергией
Распределение электронов по уровням валентной зоны и зоны проводимости описывается функцией Фéрми–Дирáка, задающей вероятность того, что состояние с энергией ![]() занято электроном
занято электроном
![]() , (35.1)
, (35.1)
где ![]() – постоянная Больцмана,
– постоянная Больцмана, ![]() – абсолютная температура,
– абсолютная температура, ![]() – энергия уровня Фéрми, вероятность нахождения на котором электрона
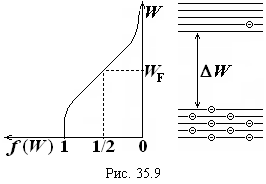
– энергия уровня Фéрми, вероятность нахождения на котором электрона ![]() . График этой функции, совмещенный с энергетической диаграммой полупроводника, показан на рис. 35.9.
. График этой функции, совмещенный с энергетической диаграммой полупроводника, показан на рис. 35.9.![]()
35.6. Температурная зависимость электропроводности полупроводников
Закон Ома в дифференциальной форме
![]() (35.2)
(35.2)
содержит удельное сопротивление ![]() или удельную электропроводность
или удельную электропроводность ![]() . Удельное сопротивление характеризует преобразование энергии электрического тока в теплоту. Плотность тока в металле
. Удельное сопротивление характеризует преобразование энергии электрического тока в теплоту. Плотность тока в металле
![]() , (35.3)
, (35.3)
где ![]() – концентрация электронов проводимости,
– концентрация электронов проводимости, ![]() – элементарный заряд,
– элементарный заряд, ![]() – средняя скорость направленного движения электронов,
– средняя скорость направленного движения электронов, ![]() – подвижность электронов проводимости, равная средней скорости направленного движения, приобретаемой электронами под действием электрического поля единичной напряженности. Из (35.2) и (35.3) получаем
– подвижность электронов проводимости, равная средней скорости направленного движения, приобретаемой электронами под действием электрического поля единичной напряженности. Из (35.2) и (35.3) получаем
![]() . (35.4)
. (35.4)
В металлах подвижность ![]() электронов с повышением температуры уменьшается, так как в результате возрастания амплитуды тепловых колебаний атомов электроны чаще с ними сталкиваются, а поэтому между столкновениями ускоряются внешним полем до меньших скоростей. Концентрация
электронов с повышением температуры уменьшается, так как в результате возрастания амплитуды тепловых колебаний атомов электроны чаще с ними сталкиваются, а поэтому между столкновениями ускоряются внешним полем до меньших скоростей. Концентрация ![]() электронов проводимости в металлах от температуры не зависит. Поэтому с повышением температуры удельная электропроводность
электронов проводимости в металлах от температуры не зависит. Поэтому с повышением температуры удельная электропроводность ![]() металлов уменьшается, а удельное сопротивление возрастает.
металлов уменьшается, а удельное сопротивление возрастает.
Удельную электропроводность чистого (беспримесного) полупроводника, называемая собственной удельной электропроводностью,
![]() , (35.5)
, (35.5)
где ![]() ,
, ![]() – концентрации, а
– концентрации, а ![]() и
и ![]() – подвижности электронов проводимости и дырок, соответственно.
– подвижности электронов проводимости и дырок, соответственно.
В беспримесных полупроводниках уровень Фéрми лежит приблизительно посередине запрещенной зоны. Поэтому для электронов зоны проводимости, располагающихся вблизи дна зоны проводимости, показатель степени в (35.1)
![]() . (35.6)
. (35.6)
С учетом того, что ![]() , вероятность заполнения электронами состояний зоны проводимости
, вероятность заполнения электронами состояний зоны проводимости
![]() . (35.7)
. (35.7)
Количество электронов, перешедших в зону проводимости, а следовательно, и количество дырок, образовавшихся в валентной зоне, будет пропорционально вероятности (35.7).
В полупроводниках, так же как и в металлах, с повышением температуры подвижности электронов ![]() и дырок
и дырок ![]() возрастают, но концентрация носителей вследствие перехода все новых электронов из валентной зоны в зону проводимости растет значительно быстрее. В результате удельная электропроводность полупроводника растет:
возрастают, но концентрация носителей вследствие перехода все новых электронов из валентной зоны в зону проводимости растет значительно быстрее. В результате удельная электропроводность полупроводника растет:
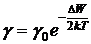 , (35.8)
, (35.8)
 где
где ![]() – основание натуральных логарифмов,
– основание натуральных логарифмов, ![]() – ширина запрещенной зоны,
– ширина запрещенной зоны, ![]() – постоянная Больцмана,
– постоянная Больцмана, ![]() – абсолютная температура,
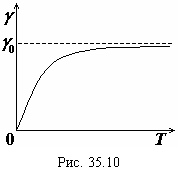
– абсолютная температура, ![]() – предельное значение удельной электропроводности полупроводника при устремлении температуры в бесконечность, когда населенности валентной зоны и зоны проводимости электронами практически выравнивается. Таким образом, удельная электропроводность полупроводника с повышением температуры возрастает по экспоненциальному закону (см. рис. 35.10).
– предельное значение удельной электропроводности полупроводника при устремлении температуры в бесконечность, когда населенности валентной зоны и зоны проводимости электронами практически выравнивается. Таким образом, удельная электропроводность полупроводника с повышением температуры возрастает по экспоненциальному закону (см. рис. 35.10).
Температурная зависимость сопротивления полупроводника имеет вид:
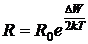 , (35.9)
, (35.9)
где ![]() – предельное значение сопротивления полупроводника при устремлении температуры в бесконечность. При низких температурах удельное сопротивление полупроводника весьма велико и он практически является изолятором, а при очень высоких температурах удельное сопротивление становится почти таким же, как у металлов.
– предельное значение сопротивления полупроводника при устремлении температуры в бесконечность. При низких температурах удельное сопротивление полупроводника весьма велико и он практически является изолятором, а при очень высоких температурах удельное сопротивление становится почти таким же, как у металлов.
К полупроводникам принадлежат кристаллы многих элементов таблицы Менделеева (кремний Si, германий Ge, селен Se и др.), закись меди ![]() , сернистый свинец
, сернистый свинец ![]() и многие другие химические элементы. Современна микроэлектроника практически полностью базируется на кремнии. Атом кремния имеет порядковый номер в периодической системе Менделеева
и многие другие химические элементы. Современна микроэлектроника практически полностью базируется на кремнии. Атом кремния имеет порядковый номер в периодической системе Менделеева ![]() . Поэтому заряд ядра атома кремния равняется
. Поэтому заряд ядра атома кремния равняется ![]() и в состав атома входит 14 электронов. Четыре из них образуют наиболее удаленную от ядра электронную
и в состав атома входит 14 электронов. Четыре из них образуют наиболее удаленную от ядра электронную  оболочку. Эти четыре электрона сравнительно слабо связаны с ядром. Они обеспечивают четыре ковалентные связи кремния в химических соединениях и поэтому называются валентными электронами. Остальные десять электронов вместе с ядром образуют остов атома, имеющий заряд
оболочку. Эти четыре электрона сравнительно слабо связаны с ядром. Они обеспечивают четыре ковалентные связи кремния в химических соединениях и поэтому называются валентными электронами. Остальные десять электронов вместе с ядром образуют остов атома, имеющий заряд ![]() . Четыре валентных электрона движутся вокруг остова и образуют облако отрицательного заряда. На рис. 35.11 показано схематическое изображение атома кремния с его четырьмя ковалентными связями.
. Четыре валентных электрона движутся вокруг остова и образуют облако отрицательного заряда. На рис. 35.11 показано схематическое изображение атома кремния с его четырьмя ковалентными связями.
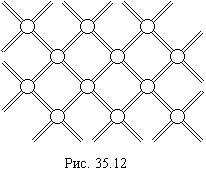 В кристаллической решетке кремния каждый атом окружен четырьмя ближайшими соседями. Упрощенная плоская схема размещения атомов изображена на рис. 35.12. Связь двух соседних атомов осуществляется парой электронов, обеспечивающих так называемую парно-электронную, или ковалентную связь. Изображенная картина соответствует чистому кремнию при очень низкой температуре. В этом случае все валентные электроны задействованы в образовании связей между атомами и не могут принимать участие в электропроводности.
В кристаллической решетке кремния каждый атом окружен четырьмя ближайшими соседями. Упрощенная плоская схема размещения атомов изображена на рис. 35.12. Связь двух соседних атомов осуществляется парой электронов, обеспечивающих так называемую парно-электронную, или ковалентную связь. Изображенная картина соответствует чистому кремнию при очень низкой температуре. В этом случае все валентные электроны задействованы в образовании связей между атомами и не могут принимать участие в электропроводности.
 При повышении температуры кристалла тепловые колебания решетки приводят к разрыву некоторых ковалентных связей. Вследствие этого часть электронов, задействованных ранее в образовании ковалентных связей, отщепляются и становятся электронами проводимости. При наличии внешнего электрического поля они перемещаются против поля и создают электрический ток.
При повышении температуры кристалла тепловые колебания решетки приводят к разрыву некоторых ковалентных связей. Вследствие этого часть электронов, задействованных ранее в образовании ковалентных связей, отщепляются и становятся электронами проводимости. При наличии внешнего электрического поля они перемещаются против поля и создают электрический ток.
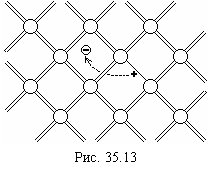
Уход электрона, ранее принимавшего участие в образовании ковалентной связи, приводит к появлению вакансии – “дырки” (см. рис. 35.13). Возникновение дырок создает дополнительную возможность для перенесения заряда. Действительно, при наличии дырки валентный электрон соседнего атома под действием внешнего электрического поля может перейти на место дырки. Тогда в этом месте восстановится ковалентная связь, но зато возникнет дырка в позиции, из которой перешел валентный электрон, заполнивший вакансию. В эту новую дырку сможет перейти валентный электрон из другого соседнего атома и т. д. Вследствие этого ток будет поддерживаться не только электронами проводимости, но и валентными электронами, которые перемещаться точно так же, как и электроны проводимости, против электрического поля. Дырки же будут перемещаться в направлении электрического поля, то есть так, как двигались бы положительно заряженные частицы. Таким образом, в полупроводниках возможны два типа электропроводности: электронный, осуществляемый движением электронов проводимости, и дырочный, обусловленный движением дырок.
Наряду с переходами электронов из связанного состояния в свободное (из валентной зоны в зону проводимости) происходят и обратные переходы, когда электрон проводимости заполняет одну из вакансий и превращается в валентный электрон (возвращается из зоны проводимости в валентную зону). Этот процесс называют рекомбинацией электрона и дырки. В равновесном состоянии устанавливается такая концентрация электронов (и точно такая же концентрация дырок), при которой за единицу времени происходит одинаковое число прямых и обратных переходов.
35.7. Примесная проводимость
Теперь рассмотрим такой кристалл кремния, в котором небольшая часть атомов в узлах решетки замещена атомами другого химического элемента. Рассмотрим вначале случай, когда атомы примеси имеют больше валентных электронов, чем атомы кремния. Такими примесями могут быть элементы пятой группы периодической системы, такие как фосфор (Р), мышьяк (Аs), сурьма (Sb). Четыре из пяти валентных электронов примесного атома задействованы в ковалентных связях с четырьмя ближайшими соседними атомами кремния, а пятый электрон будет “лишним”. Кулоновская сила притяжения этого электрона к примесному атому в кристалле ослабляется в ![]() раз (диэлектрическая проницаемость, для кремния
раз (диэлектрическая проницаемость, для кремния ![]() ). Соответственно уменьшается энергия ионизации примесного атома от нескольких электрон-вольт до нескольких десятых электрон-вольта. Поэтому в кристаллах с примесями уже при температурах, значительно меньших комнатной, когда собственная проводимость еще ничтожно мала, примесные атомы отдают свои “лишние” электроны, которые при этом становятся электронами проводимости. Поэтому примеси, поставляющие электроны в зону проводимости кристалла, называют донорными. Атомы примеси становятся при этом неподвижными положительными ионами. На рис. 35.14 они изображены в виде квадратиков. Поскольку с потерей примесным атомом пятого электрона ковалентные связи в решетке кремния не нарушаются, то донорные примеси не создают дырок в заполненной зоне кристалла. Электропроводность полупроводников с примесями, обусловленную свободными электронами, поставляемыми донорными атомами, называют примесной проводимостью
). Соответственно уменьшается энергия ионизации примесного атома от нескольких электрон-вольт до нескольких десятых электрон-вольта. Поэтому в кристаллах с примесями уже при температурах, значительно меньших комнатной, когда собственная проводимость еще ничтожно мала, примесные атомы отдают свои “лишние” электроны, которые при этом становятся электронами проводимости. Поэтому примеси, поставляющие электроны в зону проводимости кристалла, называют донорными. Атомы примеси становятся при этом неподвижными положительными ионами. На рис. 35.14 они изображены в виде квадратиков. Поскольку с потерей примесным атомом пятого электрона ковалентные связи в решетке кремния не нарушаются, то донорные примеси не создают дырок в заполненной зоне кристалла. Электропроводность полупроводников с примесями, обусловленную свободными электронами, поставляемыми донорными атомами, называют примесной проводимостью ![]() типа.
типа.
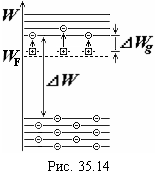 Из-за того, что концентрация примесных атомов мала по сравнению с концентрацией атомов кремния, примесные атомы в кристалле размещаються на больших расстояниях друг от друга и практически не взаимодействуют между собой. Каждый примесный атом в кристалле можно рассматривать как изолированный от других атомов примеси. По этой причине энергетические уровни примесных атомов не расщепляются в зоны. Энергия ионизации донорных примесей определяет энергетический интервал
Из-за того, что концентрация примесных атомов мала по сравнению с концентрацией атомов кремния, примесные атомы в кристалле размещаються на больших расстояниях друг от друга и практически не взаимодействуют между собой. Каждый примесный атом в кристалле можно рассматривать как изолированный от других атомов примеси. По этой причине энергетические уровни примесных атомов не расщепляются в зоны. Энергия ионизации донорных примесей определяет энергетический интервал ![]() между донорным уровнем и дном зоны проводимости (см. рис. 35.14). Ширина запрещенной зоны кремния
между донорным уровнем и дном зоны проводимости (см. рис. 35.14). Ширина запрещенной зоны кремния ![]() , энергетический интервал в случае, если примесь – мышьяк,
, энергетический интервал в случае, если примесь – мышьяк, ![]() .
.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |




