где показатель адиабаты 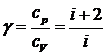 . Уравнение Пуассона может быть записано еще в таком виде:
. Уравнение Пуассона может быть записано еще в таком виде: ![]() ,
, 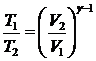
или ![]() , т. е.
, т. е. 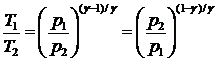 .
.
Работа, совершаемая при адиабатическом изменении объема газа
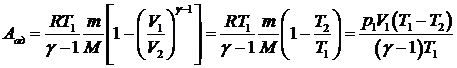 ,
,
где р1 и V1 – давление и объем газа при температуре Т1.
Коэффициент полезного действия (КПД) тепловой машины
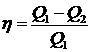 ,
,
где ![]() – количество теплоты, полученное рабочим телом от нагревателя,
– количество теплоты, полученное рабочим телом от нагревателя, ![]() – количество теплоты, отданное холодильнику. Для идеального цикла Карно
– количество теплоты, отданное холодильнику. Для идеального цикла Карно
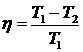 ,
,
где ![]() и Т2 – термодинамические температуры нагревателя и холодильника.
и Т2 – термодинамические температуры нагревателя и холодильника.
Энтропия – термодинамическая функция, выражающая состояние системы и степень беспорядка в ней
![]() ,
,
где k – постоянная Больцмана, W – вероятность состояния системы.
Разность энтропии 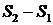 двух состояний 2 и 1 определяется формулой
двух состояний 2 и 1 определяется формулой
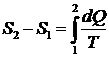 .
.
Изменение энтропии (∆S) при нагревании тела от температуры Т1 до Т2:
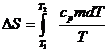 .
.
Второе начало термодинамики – энтропия изолированной системы не может убывать
![]() .
.
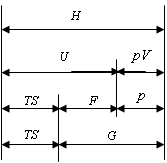 Связь между основными термодинамическими функциями и параметрами
Связь между основными термодинамическими функциями и параметрами
Н = U + рV,
U = F + ТS,
G = F + рV,
где Н – энтальпия; U – внутренняя энергия; G – свободная энергия Гиббса; F – свободная энергия
Гельмгольца, ТS и рV – связанные энергии, вносящие вклад в различные превращения в системе (фазовые превращения, химические реакции, адиабатные явления и др.).
Фазовыми переходами I рода называются такие превращения, при которых скачком меняется первая производная от термодинамической функции.
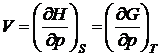 ;
; 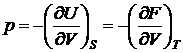 ;
;
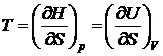 ;
; 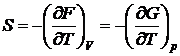 .
.
Под фазовыми переходами I рода понимают фазовые превращения, сопровождающиеся поглощением или выделением скрытой теплоты и скачкообразным изменением удельного объема DV ¹ 0 и энтропии DS ¹ 0.
К фазовым переходам I рода относятся кристаллизация, плавление, парообразование, конденсация, полиморфные переходы и пр.
Основным уравнением, характеризующим фазовые переходы I рода, является уравнение Клапейрона-Клаузиуса
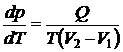 ,
,
где ![]() и
и ![]() – объемы одной и второй фаз.
– объемы одной и второй фаз.
Зависимость температуры фазовых превращений от давления:
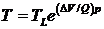 .
.
Плавление – это превращение кристаллического тела в жидкое состояние при температуре плавления ТL.
Теплота плавления
Q = Lm,
где L – удельная теплота плавления, m – масса тела.
Кристаллизация – это процесс перехода вещества из жидкого состояния в твердое кристаллическое при охлаждении.
Полиморфизм – свойство одного и того же вещества пребывать при определенных условиях в разных кристаллографических модификациях.
Полиморфные превращения – это переход одной фазы твердого вещества в другую фазу того же вещества.
Теплота кипения (парообразования)
![]() ,
,
где r – удельная теплота парообразования.
Теплота сгорания топлива
![]() ,
,
где q – удельная теплота сгорания топлива.
Изменение энтропии при фазовом превращении
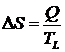 или
или 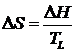 ,
,
где Q, ![]() – теплота и энтальпия фазового превращения,
– теплота и энтальпия фазового превращения, ![]() – температура фазового превращения.
– температура фазового превращения.
Изменение энергии Гиббса системы при нагревании тела, при постоянном давлении
![]() ,
,
где ![]() ,
, ![]() – начальная температура тела,
– начальная температура тела, ![]() – изменение энтальпии.
– изменение энтальпии.
Изменение энергии Гиббса при кристаллизации переохлажденной жидкости, при постоянном давлении
![]() ,
,
где ![]() (
(![]() ) – переохлаждение,
) – переохлаждение, ![]() – температура плавления,
– температура плавления, ![]() – энтальпия плавления.
– энтальпия плавления.
Минимальный размер кристаллика lk и работа его образования Ak из переохлажденной жидкости при кристаллизации. Для кристаллика кубической формы
![]() ,
, 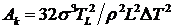 ,
,
где ![]() – переохлаждение,
– переохлаждение, ![]() – температура плавления,
– температура плавления, ![]() – удельная теплота плавления,
– удельная теплота плавления, ![]() – плотность,
– плотность, ![]() – межфазное поверхностное натяжение.
– межфазное поверхностное натяжение.
Скорость массовой кристаллизации жидкой фазы
![]() .
.
Линейная скорость затвердевания жидкой фазы
![]() ,
,
где ![]() – коэффициент теплопроводности,
– коэффициент теплопроводности, ![]() – площадь растущей поверхности,
– площадь растущей поверхности, ![]() – градиент температуры.
– градиент температуры.
Фазой называется часть системы, которая имеет границу раздела и может быть отделена от общей системы механическим путем. Число фаз обозначают буквой Ф. Фазами могут считаться газообразное, жидкое, твердое состояния и др. Так, в системе лёд-вода при 0°С имеются две фазы (Ф = 2).
Компонент – независимая часть системы, имеющая свою химическую формулу, т. е. компонент – это индивидуальное вещество. Числе компонентов обозначается буквой К в системе, например, лед-вода К = 1, компонентом является химическое соединение ![]() , а число фаз Ф = 2.
, а число фаз Ф = 2.
Термодинамическая степень свободы системы определяется числом независимых переменных (давление – р, температура – Т, концентрация – С и т. д.), которые можно изменять в определенных пределах, не нарушая равновесия. Чисто степеней свободы обозначается буквой i.
Закономерности всех изменений системы в зависимости от внутренних и внешних условий подчиняются правилу фаз Гиббса
![]() ,
,
где В – число внешних воздействий (температура, давление и т. д.).
Обычно для простых веществ, сплавов и растворов принимают два внешних фактора: температуру и давление. В этом случае В = 2, а правило фаз Гиббса пишут в виде
![]() .
.
Если же за внешний фактор принять один из этих параметров (либо температуру, либо давление), тогда В = 1:
![]() .
.
Например, в системе лед-вода при атмосферном давлении и при температуре 0°С:
![]() ,
,
т. е. система такая существует, но она не имеет степеней свободы.
Если ![]() система называется нонвариантной, если
система называется нонвариантной, если ![]() – моновариантной, если
– моновариантной, если ![]() – бивариантной. При
– бивариантной. При ![]() система существовать не может.
система существовать не может.
С учетом химических реакций между компонентами системы число независимых компонентов ![]() уменьшается в зависимости от числа уравнений У, с помощью которых можно связать концентрации веществ. В этом случае правило фаз будет иметь вид:
уменьшается в зависимости от числа уравнений У, с помощью которых можно связать концентрации веществ. В этом случае правило фаз будет иметь вид:
І = ![]() – Ф + В,
– Ф + В,
где ![]() = К – У.
= К – У.
Сплавами называют твердые вещества, полученные путем расплавления двух или нескольких компонентов и последующей кристаллизации.
По характеру взаимодействия компонентов различают такие сплавы как твердые растворы, механические смеси и химические соединения.
Диаграмма состояния – это график зависимости температуры плавления и кристаллизации сплава в зависимости от состава.
Концентрация – величина, определяющая содержание компонента в смеси, растворе, сплаве. Способы выражения концентрации различны.
Относительная массовая концентрация ![]() – отношение массы компонента mi к общей массе смеси
– отношение массы компонента mi к общей массе смеси
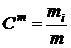 .
.
Примеры решения задач
Пример 1. Сколько молекул воздуха находится в комнате, которая имеет размеры 8´4´3 м3, при температуре t = 18°С и давлении р = 0.97∙105 Па?
Решение
V = 8´4´3 м3 t = 18°С р = 0.97∙105 Па | Состояние газа некоторой массы определяется тремя термодинамическими параметрами: давлением р, объемом V и температурой Т. Связь между этими параметрами (уравнение Менделеева-Клапейрона) для газа: , (1) |
Ν – ? |
где ![]() =
=![]() – количество вещества или
– количество вещества или ![]() = ,
= ,
где NA – число Авогадро которое равно: NA = 6.02∙1023 моль-1, N – количество молекул воздуха в комнате.
Запишем уравнение (1) в виде
рV = ![]() RТ. (2)
RТ. (2)
Из (2) найдем количество молекул воздуха в комнате:
N = ![]() . (3)
. (3)
Проверим размерности величин:
[Ν] = 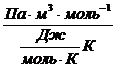 =
=![]() =
=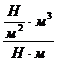 = 1.
= 1.
Подставим значения заданных величин в формулу (3):
N = 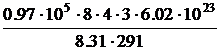 = 23·1026.
= 23·1026.
Ответ: N = 23·1026.
Пример 2. Определить среднюю кинетическую энергию <Wk> поступательного движения молекул газа, который находится под давлением 0.1 Па. Концентрация молекул газа равна 1013 см–3.
Решение
Р = 0.1 Па n = 1013 см–3 = 1019 м–3 | Рассмотрим изотермический процесс Т = соnst, согласно которому средняя кинетическая энергия |
<Wk> – ? |
поступательного движения определяется формулой
<Wk> = ![]() kT.
kT.
Кроме энергии неизвестна также температура газа. Давление при температуре Т равно р = nkТ. Тогда Т = ![]() .
.
Поставим полученное выражение в уравнение для энергии и найдем среднюю кинетическую энергию поступательного движения молекул газа
<Wk> = ![]() k
k![]() = ,
= ,
где k = 1.38·10–23 Дж/К.
Проверим единицы измерения
[<Wk>] =![]() =
= ![]() =Н ·м = Дж.
=Н ·м = Дж.
Поставляя значения заданных величин, получим
<Wk> = 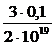 =1.5∙10-20Дж.
=1.5∙10-20Дж.
Ответ: <Wk> = 1.5∙10-20Дж.
Пример 3. Кислород, который занимает при давлении 1 МПа объем 5 л, расширяется в 3 раза. Определить конечное давление и работу, совершенную газом. Рассмотрите следующие процессы: 1) изобарный; 2) изотермический, 3) адиабатный.
Решение
р1 = 1 МПа = 106Па V1 = 5 л = 5·10–3 м3 V1 = 5 л = 5·10–3 м3 V2 = 3 V1 М = 32·10–3 кг/моль 1) р = соnst 2) Т = соnst 3) Q = 0 | 1) Рассмотрим изобарный процесс р1= р2, р2 = 106 Па. Работа, которую выполняет газ при расширении равна: А = р1ΔV или А = р1ΔV = р1(V2 – V1). Так как V2 = 3V1, то работа А = р1 (3 V1 – V1)=2 р1V1. Подставим значения заданных величин: А = 2·106 ·5·10–3 = 104 Дж. 2) Рассмотрим изотермический процесс Т = соnst, |
Р2 – ? А – ? |
согласно которому р1V1 = р2V2.
Отсюда р2=![]() .
.
Проверка размерностей: [р2] = Па ·![]() = Па.
= Па.
Подставим значения заданных величин
р2 = = 0.33·106 Па.
Найдем работу по расширению газа из уравнения:
А = ![]() = р1V1
= р1V1![]()
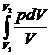 = р1V1ln
= р1V1ln![]() .
.
Проверка размерностей: [А] = Па ·м3![]() =
=![]() ·м3 = Н·м = Дж.
·м3 = Н·м = Дж.
Подставим значения заданных величин:
А = 106 ·5·10–3 ln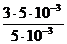 = 5.5·103 Дж.
= 5.5·103 Дж.
3) Рассмотрим адиабатный процесс Q = 0. Согласно первому закону термодинамики 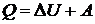 ,
, ![]() . Запишем уравнение Пуассона
. Запишем уравнение Пуассона ![]() = соnst для данного случая:
= соnst для данного случая:
![]() .
.
Из уравнения найдем давление р2:
р2 = р1 ,
где ![]() – коэффициент адиабаты, который равен
– коэффициент адиабаты, который равен ![]() =
=![]() , і – число степеней свободы молекул, для кислорода і = 5 (двухатомный газ).
, і – число степеней свободы молекул, для кислорода і = 5 (двухатомный газ).
Проверка единиц измерения: [р] = Па·![]() = Па.
= Па.
Подставим значения заданных величин:
р2 = 106 или р2 = –1.4 = 0.21·106 Па.
Работа при адиабатическом процессе совершается за счет изменения внутренней энергии
ΔU =![]() СV ΔТ.
СV ΔТ.
Т. к. А = –ΔU и СV = , то работа по расширению газа ![]() .
.
Из уравнения Менделеева-Клапейрона для массы т газа для двух состояний найдем разницу 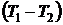 :
:
р1V1 = ![]() RТ1 и р2V2 =
RТ1 и р2V2 = ![]() RТ2,
RТ2,
R (Т1 – Т2) = (р1 V1 – р2 V2).
Тогда работа А = (р1V1 – р2V2).
Проверка единиц измерения [А] = Па·м3 =![]() ·м3 = Н·м = Дж.
·м3 = Н·м = Дж.
Подставляя значения данных величин, получим
А = (106 ·5·10–3 – 106 ·3·5·10–3) = –4.63·10-3 Дж.
Ответ: 1) р2 = 106 Па, А = 104 Дж.
2) р2 = 0.33·106 Па, А = 5.5·103 Дж.
3) р2 = 0.21·106 Па, А = –4.63·10–3 Дж.
Пример 4. В емкость, в которой находится 2 кг воды и 0.5 кг льда при температуре 0°С, пропускают водяной пар, который имеет температуру 150°С. После того как лед растаял температура в емкости стала 30°С. Какова масса пропущенного пара? Теплоемкость емкости Сп = 630 ![]() .
.
Решение
mв = 2 кг mл = 2 кг tп = 0°С = 273 К t = 30°С = 303 К tк = 100°С = 373 К св = 4.19 сп = 1.97 λ = 0.33 r = 2.26 Сп = 630 | Количество теплоты, которое отдает пар при охлаждении до температуры конденсации Q1 = сп mп (Тп – Тк). Количество теплоты, которое отдает пар при конденсации Q2 = r mп. Количество теплоты, которое отдает сконденсированная вода при ее охлаждении до температуры Т: Q3 = св mп (Тк – Т). Количество теплоты, которое получил лед при таянии Q4 = λ∙mл. Количество теплоты, которое получила вода, которая находится в емкости при ее нагревании до температуры Т: Q5 = св (mв + mл)(Т – Тп). |
mп – ? |
Количество теплоты, которое получила емкость при ее нагревании до температуры Т:
Q6 = сс mс(Т – Тп) = Сп(Т – Тп).
Составляем уравнение теплового баланса
Q1 + Q2 + Q3 = Q4 + Q5 + Q6,
или
сп mп (Тп – Тк) + r mп + св mп (Тк – Т) =
= λ mл +св (mв + mл )(Т – Тп) + сс mс(Т – Тп).
Из последнего равенства найдем массу пара:
mп = [λ mл + св (mв + mл)(Т – Тп)+ Сп (Т – Тп)]/[сп(Тп – Тк)+ r + св(Тк – Т)].
Проверим размерности:
mп =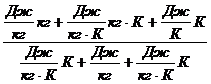 = кг.
= кг.
Подставим значения данных величин
mп =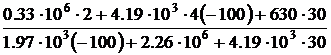 = 0.19 кг.
= 0.19 кг.
Ответ: mп = 0.19 кг.
Пример № 6. Вычислите изменение энтропии в процессе затвердевания переохлажденного в количестве 1 моль бензола при 268 К, если при 278 К
![]() = 9956 Дж/моль,
= 9956 Дж/моль, ![]() = 127.3 Дж/(моль×К),
= 127.3 Дж/(моль×К), ![]() = 123.6 Дж/(моль×К); P = const = 1.01×105 Па.
= 123.6 Дж/(моль×К); P = const = 1.01×105 Па.
Решение
Этот процесс необратим, поэтому мысленно проводим данный процесс обратимо в три стадии:
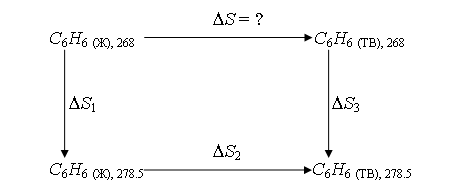
Тогда DS = DS1 + DS2 + DS3.
Значения DS1 и DS3 вычисляем по уравнению 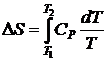 ; DS2 – по уравнению
; DS2 – по уравнению ![]() . Тогда
. Тогда
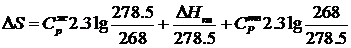 ,
,
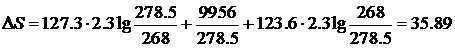 Дж/(моль×К).
Дж/(моль×К).
Ответ: ![]() Дж/(моль×К).
Дж/(моль×К).
Пример 7. Найти число термодинамических степеней свободы для двухкомпонентного сплава, находящегося в жидко-твердом состоянии при постоянном давлении.
Решение
Число компонент в этой системе К = 2, число фаз Ф = 2, число внешних воздействий B = l. В этом случае i = 2 – 2 + 1 = 1, т. е. имеется одна переменная. Значит для сплава фиксированного состава, равновесие между жидкой и твердой фазой при p = Const сохраняется в интервале температур (Т ¹ Const).
Пример 8. Проанализировать диаграмму состояния бинарной системы с неограниченной взаимной растворимостью компонентов в твердом и жидком состояниях, построенную методом термического анализа (рис. 2.1).
Решение
Рассмотрим охлаждение расплава, обозначенного фигуративной точкой М. При температуре Tа в точке а0 начинается кристаллизация твердого раствора и образуется двухфазная система, состоящая из расплава состава х0, находящегося в равновесии с твердым раствором состава х3. В интервале температур от Та до Тс число степеней свободы равно единице (i = 3 – 2 = 1) и каждой температуре соответствуют определенные составы жидкого и твердого раствора.
Например, система состава х0 в фигуративной точке b0 состоит из двух фаз: жидкого раствора состава х1 (точка b1) и твердого раствора состава х2 (точка b2).
Согласно правилу рычага для фигуративной точки b0
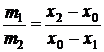 ,
, 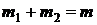 ,
,
где m – масса сплава; m1 и m2 – массы расплава и твердого раствора. Полное затвердевание расплава произойдет при температуре Tс; при этом состав х0 твердого раствора (точка с0) соответствует составу х0 исходного расплава а0. Т. к. на диаграмме состояния нет точек, в которых в равновесии находились бы три фазы и число степеней свободы было бы равно нулю, то на кривой охлаждения (рис. 2.1, б) нет горизонтальных участков. Путь кристаллизации изображается кривой Ма0b1c1.
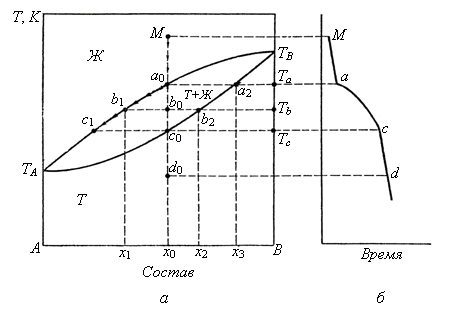
Рис. 2.1. Диаграмма состояния системы с неограниченной растворимостью компонентов
в твердом состоянии: а – без экстремальных точек; б – кривая охлаждения
Пример 9. Найти плотность ![]() сплава, если известны массы m1, m2 и плотности
сплава, если известны массы m1, m2 и плотности ![]() и
и ![]() компонентов.
компонентов.
Решение
![]() ,
, ![]() ,
, 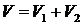 ,
,
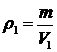 ,
, 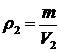 ,
,
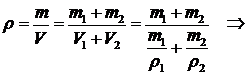
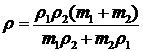 .
.
Например, для сплава олова и свинца при 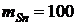 г,
г, ![]() г и
г и 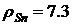 г/см3,
г/см3, 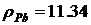 г/см3 имеем
г/см3 имеем ![]() 8.28 г/см3.
8.28 г/см3.
КОНТРОЛЬНАЯ РАБОТА 2
ТЕОРЕТИЧЕСКИЕ ВОПРОСЫ
2.1. Основные положения молекулярно-кинетической теории. Идеальный газ. Атом. Молекула. Атомная и молекулярная масса вещества. Плотность. Количество вещества. Моль вещества. Молярная масса. Закон Авогадро.
2.2. Законы идеального газа. Изохорный, изобарный, изотермический процессы. Абсолютная шкала температур. Объединенный газовый закон (вывод). Закон Менделеева-Клапейрона (вывод). Закон Дальтона.
2.2. Основное уравнение молекулярно-кинетической теории газов. Средняя скорость хаотического движения молекул. Средне-квадратичная скорость молекул. Вывод основного уравнения молекулярно-кинетической теории идеальных газов. Средняя кинетическая энергия молекул. Температура – как мера средней кинетической энергии молекул.
2.3. Распределение молекул по скоростям и энергиям. Распределение Максвелла (вывод уравнений). Наиболее вероятная скорость, средне-арифметическая и средне-квадратичная скорость молекул.
2.4. Распределение Больцмана (вывод). Барометрическая формула. Среднее число столкновений и средняя длина свободного пробега молекулы.
2.5. Явление переноса. Теплопроводность газов. Закон Фурье. Плотность теплового потока. Коэффициент теплопроводности.
2.6. Диффузия. Закон Фика. Коэффициент диффузии. Внутреннее трение (вязкость). Закон Ньютона для внутреннего трения. Динамическая и кинематическая вязкость. Формула Стокса.
2.7. Предмет термодинамики. Термодинамическая система. Внутренняя энергия. Число степеней свободы для молекулы. Работа газа при изменении его объема. Количество теплоты для нагревания тела. Удельная теплоемкость. Молярная теплоемкость. Единицы измерения теплоты и теплоемкости. Теплота сгорания топлива.
2.8. Первое начало термодинамики. Теплоемкости при постоянном давлении и при постоянном объеме. Уравнение Майера.
2.9. Взаимное превращение тепловой энергии в другие виды энергии. Превращение тепловой энергии в механическую. Коэффициенты полезного действия этих превращений. Теплота сгорания топлива.
2.10. Применение первого начала термодинамики к изопроцессам: изохорный процесс, изобарный процесс, изотермический процесс. Графики изопроцессов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 |



