2.11. Адиабатный процесс. Вывод уравнения Пуассона. Диаграмма адиабатного процесса. Адиабата.
2.12. Второе начало термодинамики. Круговой процесс. Обратимый и необратимый процессы. Прямой и обратный циклы. Нагреватель, рабочее тело, холодильник. Формулировка второго закона термодинамики (по Клаузиусу).
2.13. Цикл Карно. Схема цикла (изотермы и адиабаты) и ее анализ. Вывод КПД идеальной тепловой машины. Теорема Карно. Неравенство Клаузиуса. Общее выражение второго закона термодинамики.
2.14. Энтропия. Свойства энтропии. Физический смысл энтропии. Статистическое толкование второго начала термодинамики. Примеры вычисления энтропии для изопроцессов. Третье начало термодинамики.
2.15. Реальные газы. Силы межмолекулярного взаимодействия. Уравнение Ван-дер-Ваальса. Изотермы реального газа. Критическая температура.
2.16. Насыщенный и ненасыщенный пар. Влажность воздуха. Гигрометры и психрометры.
2.16. Свойства жидкостей. Поверхностное натяжение. Коэффициент поверхностного натяжения. Сила поверхностного натяжения. Работа сил поверхностного натяжения жидкости. Явление смачивания и несмачивания. Капиллярные явления.
2.17. Фазовые превращения. Твердое, жидкое и газообразное состояние вещества. Плавление, кристаллизация, кипение, испарение, конденсация, сублимация, полиморфные превращения. Удельная теплота плавления. Удельная теплота парообразования. Термический анализ. Термограмма.
2.18. Термодинамика фазовых превращений. Фаза. Компонент. Правило фаз Гиббса. Примеры выполнения правила фаз.
2.19. Термодинамические функции и параметры: внутренняя энергия, энтропия, свободная энергия Гиббса, свободная энергия Гельмгольца. Связь между ними. Уравнение Клапейрона-Клаузиуса.
2.20. Фазовые превращения I рода. Плавление. Кристаллизация жидкой фазы. Диаграмма плавкости. Переохлаждение. Кинетика кристаллизации. Параметры кристаллизации. Изменение энергии Гиббса при фазовом превращении первого рода. Критический размер и работа образования зародыша (первого кристаллика, образующегося при кристаллизации).
2.21. Полиморфные превращения. Полиморфизм. Изоморфизм. Полиморфные превращения. Графики нагревания и охлаждения вещества с учетом полиморфных превращений. Кинетика полиморфных превращений.
2.22. Сплавы. Типы сплавов: твердые растворы, механические смеси. Сплавы с промежуточным химическим соединением. Сплавы с ограниченной и неограниченной растворимостью. Плавление и кристаллизация сплавов. Физика сплавов.
2.23. Диаграмма состояния для непрерывного ряда твердых растворов. Диаграмма состояния. Ликвидус. Солидус. Построение кривых нагревания и охлаждения сплавов непрерывного ряда твердых растворов. Расшифровка диаграммы. Применение правила фаз Гиббса для сплавов. Твердые растворы внедрения и твердые растворы замещения.
2.24. Диаграмма состояния механических смесей. Диаграмма состояния. Ликвидус. Солидус. Эвтектика. Построение кривых нагревания и охлаждения механических смесей. Расшифровка диаграммы. Применение правила фаз Гиббса для сплавов.
2.25. Диаграмма состояния с образованием химического соединения. Диаграмма состояния. Ликвидус. Солидус. Эвтектика. Дистектика. Построение кривых нагревания и охлаждения сплавов с образованием химического соединения. Расшифровка диаграммы. Применение правила фаз Гиббса для сплавов.
ЗАДАЧИ
2.1. Найти молярную массу М и массу mМ одной молекулы поваренной соли.
2.2. Определить концентрацию n молекул кислорода, находящегося в сосуде вместимостью V = 2 л. Количество вещества ![]() кислорода равно 0.2 моль.
кислорода равно 0.2 моль.
2.3. Определить количество вещества ![]() водорода, заполняющего сосуд объемом V = 3 л, если концентрация газа в сосуде n = 2∙1018 м–3.
водорода, заполняющего сосуд объемом V = 3 л, если концентрация газа в сосуде n = 2∙1018 м–3.
2.4. В баллоне вместимостью V = 3 л содержится кислород массой m = 10 г. Определить концентрацию молекул газа.
2.5. Определить количество вещества ![]() и число молекул азота массой m = 0.2 кг.
и число молекул азота массой m = 0.2 кг.
2.6. В баллоне находится газ при температуре 15°С. Во сколько раз уменьшится давление газа, если 40% его выйдет из баллона, а температура при этом понизится на 8°С?
2.7. В комнате площадью S = 20 м2 и высотой h = 2.5 м температура воздуха повысилась с Т1 = 288 К до Т2 = 298 К. Давление постоянно и равно р = 100 кПа. На сколько уменьшилась масса воздуха ∆m в комнате?
2.8. Газ при давлении 0.2 МПа и температуре 15°С имеет объем 5 л. Чему равен объем этой массы при нормальных условиях?
2.9. При увеличении абсолютной температуры идеального газа в 2 раза давление газа увеличилось на 25%. Во сколько раз при этом изменился объем?
2.10. В баллоне находится газ при температуре Т1 = 400 К. До какой температуры Т2 надо нагреть, чтобы его давление увеличилось в 1.5 раза?
2.11. Два сосуда одинакового объема содержат кислород. В одном сосуде давление р1 = 2 МПа и температура Т1 = 800 К, а в другом р2 = 2.5 МПа, Т2 = 200 К. Сосуды соединили трубкой и охладили находящийся в них кислород до температуры Т = 200 К. Определить установившееся в сосудах давление.
2.12. Определить плотность ![]() водяного пара, находящегося под давлением р = 2.5 кПа и имеющего температуру Т = 250 К.
водяного пара, находящегося под давлением р = 2.5 кПа и имеющего температуру Т = 250 К.
2.13. Определить внутреннюю энергию U водорода, а также среднюю кинетическую энергию <Wk> молекулы этого газа при температуре Т = 300 К, если количество вещества ![]() этого газа равно 0.5 моль.
этого газа равно 0.5 моль.
2.14. Количество вещества гелия ![]() = 1.5 моль, температура Т = 120 К. Определить суммарную кинетическую энергию Wk поступательного движения всех молекул этого газа.
= 1.5 моль, температура Т = 120 К. Определить суммарную кинетическую энергию Wk поступательного движения всех молекул этого газа.
2.15. Определить среднюю квадратичную скорость <uкв> молекулы газа, заключенного в сосуд вместимостью V = 2 л под давлением р = 200 кПа. Масса газа m = 0.3 г.
2.16. При какой температуре средняя кинетическая энергия <Wk> поступательного движения молекулы газа равна 4.14∙10–21Дж?
2.17. Определить показатель адиабаты ![]() идеального газа, который при температуре Т = 350 К и давлении р = 0.4 МПа занимает объем V = 300 л и имеет теплоемкость CV = 857 Дж/К.
идеального газа, который при температуре Т = 350 К и давлении р = 0.4 МПа занимает объем V = 300 л и имеет теплоемкость CV = 857 Дж/К.
2.18. В сосуде вместимостью V = 6 л находится при нормальных условиях двухатомный газ. Определить теплоемкость CV этого газа при постоянном объеме.
2.19. Трехатомный газ под давлением р = 240 кПа и температуре t = 20°C занимает объем V = 10 л. Определить теплоемкость Ср этого газа при постоянном давлении.
2.20. Одноатомный газ при нормальных условиях занимает объем V = 5 л. Вычислить теплоемкость Ср этого газа при постоянном объеме.
2.21. На какой высоте h давление воздуха составляет 75% от давления на уровне моря? Температуру воздуха считать постоянной и равной t = 0°С.
2.22. На какой высоте h плотность газа вдвое меньше его плотности на уровне моря? Температуру газа считать постоянной и равной t = 0°С. Задачу решить для: а) воздуха, б) водорода.
2.23. Определить среднюю длину свободного пробега <![]() > молекулы азота в сосуде вместимостью V = 5 л. Масса газа m = 0.5 г. При каком давлении р средняя длина свободного пробега <
> молекулы азота в сосуде вместимостью V = 5 л. Масса газа m = 0.5 г. При каком давлении р средняя длина свободного пробега <![]() > молекул азота равна 1 м, если температура газа t = 10°C?
> молекул азота равна 1 м, если температура газа t = 10°C?
2.24. Кислород находится под давлением р = 133 нПа при температуре Т = 200 К. вычислить среднее число <![]() > столкновений молекулы кислорода при этих условиях за время
> столкновений молекулы кислорода при этих условиях за время ![]() = 1 с.
= 1 с.
2.25. Найти коэффициент диффузии D водорода при нормальных условиях, если средняя длина свободного пробега <![]() > = 0.16 мкм.
> = 0.16 мкм.
2.26. Найти массу m азота, прошедшего вследствие диффузии через площадку S = 0.01 м2 за время t = 10 с, если градиент плотности в направлении, перпендикулярном к площадке, ![]() . Температура азота t = 27°С. Средняя длина свободного пробега молекул азота <
. Температура азота t = 27°С. Средняя длина свободного пробега молекул азота <![]() > = 10 мкм.
> = 10 мкм.
2.27. Найти вязкость ![]() азота при нормальных условиях, если коэффициент диффузии для него
азота при нормальных условиях, если коэффициент диффузии для него ![]() .
.
2.28. Найти коэффициент диффузии D и вязкость ![]() воздуха при давлении р = 101.3 кПа и температуре t = 10°С. Диаметр молекул воздуха равен 0.3 нм.
воздуха при давлении р = 101.3 кПа и температуре t = 10°С. Диаметр молекул воздуха равен 0.3 нм.
2.29. Найти теплопроводность ![]() водорода, вязкость которого
водорода, вязкость которого 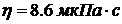 .
.
2.30. Найти теплопроводность ![]() воздуха при давлении р = 100 кПа и температуре t = 10°С. Диаметр молекул воздуха
воздуха при давлении р = 100 кПа и температуре t = 10°С. Диаметр молекул воздуха ![]() = 0.3 нм.
= 0.3 нм.
2.31. Какое количество теплоты ![]() теряет помещение за время t = 1 ч через окно за счет теплопроводности воздуха, заключенного между рамами? Площадь каждой рамы S = 4 м2, расстояние между ними d = 30 см. Температура помещения t = 18°С, температура наружного воздуха t2 = –20°С. Диаметр молекул воздуха
теряет помещение за время t = 1 ч через окно за счет теплопроводности воздуха, заключенного между рамами? Площадь каждой рамы S = 4 м2, расстояние между ними d = 30 см. Температура помещения t = 18°С, температура наружного воздуха t2 = –20°С. Диаметр молекул воздуха ![]() 0.3 нм. Температуру воздуха между рамами считать равной среднему арифметическому температур помещения и наружного воздуха. Давление р = 101.3 кПа.
0.3 нм. Температуру воздуха между рамами считать равной среднему арифметическому температур помещения и наружного воздуха. Давление р = 101.3 кПа.
2.32. Между двумя пластинами, находящимися на расстоянии d = 1 мм друг от друга, находится воздух. Между пластинами поддерживается разность температур ∆T = 1 К. Площадь каждой пластины S = 0.01 м2. Какое количество теплоты Q передается за счет теплопроводности от одной пластины к другой за время t = 10 мин? Считать, что воздух находится при нормальных условиях. Диаметр молекул воздуха ![]() 0.3 нм.
0.3 нм.
2.33. Определить количество теплоты ![]() , которое надо сообщить кислороду объемом V = 50 л при его изохорном нагревании, чтобы давление газа повысилось на ∆р = 0.5 МПа.
, которое надо сообщить кислороду объемом V = 50 л при его изохорном нагревании, чтобы давление газа повысилось на ∆р = 0.5 МПа.
2.34. При изотермическом расширении азота при температуре Т = 280 К объем его увеличился в два раза. Определить: 1) совершенную при расширении газа работу А; 2) изменение ∆U внутренней энергии; 3) количество теплоты ![]() , полученное газом. Масса азота m = 0.2 кг.
, полученное газом. Масса азота m = 0.2 кг.
2.35. Азот массой m = 0.1 кг был изобарно нагрет от температуры T1 = 300 K до температуры Т2 = 400 К. Определить работу А, совершенную газом, полученную им теплоту ![]() и изменение ∆U внутренней энергии азота.
и изменение ∆U внутренней энергии азота.
2.36. Какая работа А совершается при изотермическом расширении водорода массой m = 5 г, взятого при температуре Т = 290 К, если объем газа увеличился в три раза.
2.37. Идеальный газ совершает цикл Карно при температурах теплоприемника Т2 = 290 К и теплоотдатчика Т1 = 400 К. Во сколько раз увеличится коэффициент полезного действия ![]() цикла, если температура теплоотдатчика возрастет до
цикла, если температура теплоотдатчика возрастет до ![]() = 600 К?
= 600 К?
2.38. Определить работу А2 изотермического сжатия, совершающего цикл Карно, КПД которого ![]() = 0.4, если работа изотермического расширения равна А1 = 8 Дж.
= 0.4, если работа изотермического расширения равна А1 = 8 Дж.
2.39. Газ, совершающий цикл Карно, отдал теплоприемнику теплоту Q2 = 14 кДж. Определить температуру Т1 теплоотдатчика, если при температуре теплоприемника Т2 = 280 К работа цикла А = 6 кДж.
2.40. Газ, являясь рабочим веществом в цикле Карно, получил от теплоотдатчика теплоту Q1 = 4.38 кДж и совершил работу А = 2.4 кДж. Определить температуру теплоотдатчика, если Т2 = 273 К.
2.41. В цикле Карно газ получил от теплоотдатчика теплоту Q1 = 500 Дж и совершил работу А = 100 Дж. Температура теплоотдатчика Т1 = 400 К. Определить температуру Т2 теплоприёмника.
2.42. После опускания в воду, имеющую температуру 10°С, тела, нагретого до 100°С, через некоторое время установилась общая температура 40°С. Какой станет температура воды, если, не вынимая первого тела, в нее опустили еще одно такое же тело, нагретое до 100°С?
2.43. В сосуд, содержащий 1.5 кг воды при 15°С, впускают 200 г водяного пара при 100°С. Какая общая температура установится после конденсации пара?
2.44. Алюминиевый чайник массой 400 г, в котором находится 2 кг воды при 10°С, помещают на газовую горелку с КПД 40%. Какова мощность горелки, если через 10 мин вода закипела, причем 20 г воды выкипело?
2.45. Сколько дров надо сжечь в печке с КПД 40%, чтобы получить из 200 кг снега, взятого при температуре –10°С, воду при 20°С?
2.46. КПД плавильной печи 20%. Какое количество угля марки А-2 нужно сжечь, чтобы нагреть 3 т серого чугуна от 283 К до температуры плавления?
2.47. Вода падает с высоты 1200 м. Насколько повысится температура воды, если на ее нагревание затрачивается 60% работы силы тяжести.
2.48. Насколько нагреется при штамповке кусок стали массой 1.5 кг от удара молотом весом 3920 Н, если скорость молота в момент удара 7 м/с, а на нагревание стали затрачивается 60% энергии молота?
2.49. Стальной молот массой 12 кг падает на лежащую на наковальне железную пластинку массой 0.2 кг. Высота падения молота 1.5 м. Считая, что на нагревание пластинки затрачивается 40% кинетической энергии молота, вычислить, насколько нагреется пластинка после 50 ударов молота.
2.50. С какой средней скоростью движется автомобиль, двигатель которого при развиваемой мощности 76.5 кВт израсходовал на пути 120 км 14 л бензина? КПД двигателя 32%. Теплота сгорания бензина ![]() Дж/кг.
Дж/кг.
2.51. Какое количество бензина потребуется для двигателя автомобиля, чтобы проехать 300 км, если масса машины 5 т, КПД двигателя 22%, а сопротивление движению составляет 0.05 веса машины? Найти силу тяги и мощность, развиваемую при скорости 108 км/ч.
2.52. Идеальная тепловая машина работает по циклу Карно. При этом 80% теплоты, полученной от нагревателя, передается холодильнику, температура которого 0°С. Определить температуру нагревателя и коэффициент полезного действия.
2.53. Два свинцовых шара одинаковой массы движутся со скоростями ![]() и
и ![]() навстречу друг другу. Определить повышение температуры шаров ∆t в результате неупругого удара.
навстречу друг другу. Определить повышение температуры шаров ∆t в результате неупругого удара.
2.54. Температура нагревателя идеальной тепловой машины 117°С, а холодильника 27°С. Количество теплоты, получаемое машиной от нагревателя за 1 с, равно 60 кДж. Вычислить КПД машины, количество теплоты, отадваемое холодильнику в 1 с, и мощность машины.
2.55. Найти массу m воды, вошедшей в стеклянную трубку с диаметром канала d = 0.8 мм, опущенной в воду на малую глубину. Считать смачивание полным.
2.56. Какую работу А надо совершить при выдувании мыльного пузыря, чтобы увеличить его объем от V1 = 8 см3 до V2 = 16 см3? Считать процесс изотермическим.
2.57. Глицерин поднялся в капиллярной трубке диаметром канала d = 1 мм на высоту h = 20 см. Определить поверхностное натяжение ![]() глицерина. Считать смачивание полным.
глицерина. Считать смачивание полным.
2.58. Две капли ртути радиусом r = 1.2 мм каждая слились в одну большую каплю. Определить энергию, которая выделится при этом слиянии. Считать процесс изотермическим.
2.59. Диаграмма состояния воды в координатах Р и Т представлена на рис. 2.1. Дайте характеристику всех линий на ней (ОА, ОВ, ОК), и «тройной» точки О и всех областей, ограниченных этими линиями. Примените правило фаз Гиббса для точки О на диаграмме состояния воды (рис. 2.1).
2.60. Пользуясь уравнением Клапейрона-Клаузиуса, вывести формулу зависимости температуры плавления от давления.
2.61. При плавлении льда при 0°С теплота плавления 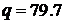 ккал/кг, объем льда в расчете на 1 кг равен 1.091 л/кг, а объем воды 1 л/кг. Найти давление, при котором температура плавления льда изменится на один градус.
ккал/кг, объем льда в расчете на 1 кг равен 1.091 л/кг, а объем воды 1 л/кг. Найти давление, при котором температура плавления льда изменится на один градус.
2.62. Рассчитать изменение давления необходимого для изменения температуры плавления льда 1°С. При 0°С ![]() Дж/г, удельные объемы жидкой воды и льда равны
Дж/г, удельные объемы жидкой воды и льда равны ![]() см3/г,
см3/г, 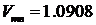 см3/г.
см3/г.
2.63. Рассчитать изменение энтропии ![]() 1 кг воды в результате замерзания при –5°С.
1 кг воды в результате замерзания при –5°С. ![]() кДж/моль, ср (льда) = 34.7 Дж/моль×К, ср (воды) = 75.3 Дж/моль×К. Объяснить, почему энтропия при замерзании уменьшается, хотя процесс – самопроизвольный.
кДж/моль, ср (льда) = 34.7 Дж/моль×К, ср (воды) = 75.3 Дж/моль×К. Объяснить, почему энтропия при замерзании уменьшается, хотя процесс – самопроизвольный.
2.64. Вычислить изменение энтропии при превращении льда в воду при 0°С, нагреве воды до 100°С и ее превращении в пар (т. е. при испарении) при 100°С.
2.65. Определить изменение энтропии ![]() при нагревании льда от 0°К до 0°С и его плавлении, если известна зависимость теплоемкости этого тела от температуры.
при нагревании льда от 0°К до 0°С и его плавлении, если известна зависимость теплоемкости этого тела от температуры.
2.66. Пользуясь выражениями для изменения свободной энергии Гиббса ΔG, энтропии ΔS и энтальпии ΔН при кристаллизации, найдите зависимость ΔG от предкристаллизационного переохлаждения ![]() .
.
2.67. Чему равна движущая сила затвердевания никеля при переохлаждении на 50 градусов?
2.68. Вычислить критический размер зародыша кристалла висмута, образовавшегося из переохлаждённого расплава, объём зародыша и площадь его поверхности. Принять форму зародыша за сферу, а величину переохлаждения ![]() = 30 градусов.
= 30 градусов.
2.69. Вычислить работу образования критического зародыша кристалла висмута, образовавшегося из переохлаждённого расплава. Принять форму зародыша за сферу, а величину переохлаждения ![]() = 30 градусов.
= 30 градусов.
2.70. Примените правило фаз Гиббса для трех точек, лежащих в областях ограниченных линиями ОА, ОВ, ОК на диаграмме состояния воды (рис. 2.2).
2.71. На рис. 2.3 приведена диаграмма состояния серы в координатах давление – температура. Охарактеризуйте все линии и точки их пересечения на этой диаграмме.
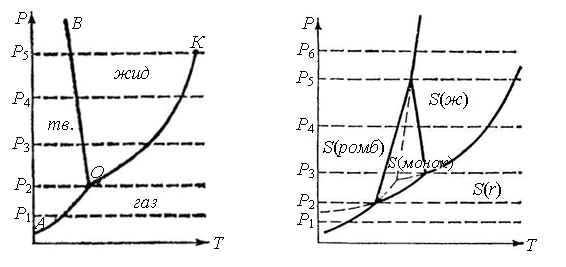 |
Рис. 2.2. Рис. 2.3.
2.72. Найдите число степеней свободы для механической смеси, состоящей из кристаллов олова и цинка при нормальном давлении.
2.73. При нормальном давлении железо и никель образуют непрерывный ряд твердых растворов. Найдите для них число степеней свободы и объясните полученный результат.
2.74. Золото и серебро образуют непрерывный ряд твердых растворов. Чему равно число степеней свободы этой системы и сплава 20%Au + 80%Ag.
2.75. По данным температурам ликвидуса, солидуса и концентрациям построить диаграмму состояния бинарного сплава. Охарактеризовать полученную диаграмму состояния. Для 5 выбранных сплавов данной диаграммы состояния построить кривые охлаждения: 3 кривые охлаждения для произвольных сплавов и 2 кривые охлаждения для сплавов с концентрациями 100% компонента А и 100% компонента В.
Системы | Молярное содержание компонента В, % | Температура ликвидуса, К | Температура солидуса, К |
Cu-Ni | 100 | 1726 | |
80 | 1673 | 1620 | |
60 | 1623 | 1523 | |
30 | 1473 | 1420 | |
0 | 1083 |
2.76. По данным температурам ликвидуса, солидуса и концентрациям построить диаграмму состояния бинарного сплава. Охарактеризовать полученную диаграмму состояния. Для 5 выбранных сплавов данной диаграммы состояния построить кривые охлаждения: 2 кривые охлаждения для сплавов с концентрациями 100% компонента А и 100% компонента В, 1 кривую охлаждения для эвтектического сплава, 1 кривую охлаждения для сплава в доэвтектической области, 1 кривую охлаждения для сплава в заэвтектической области.
Системы | Молярное содержание компонента В, % | Температура ликвидуса, К | Температура солидуса, К |
KCl-SnCl2 | 100 | 512 | |
90 | 496 | ||
75 | 481 | ||
65 | 473 | ||
60 | 460 | ||
47,5 | 583 | ||
30 | 853 | ||
0 | 1050 |
2.77. Определить массовую концентрацию компонентов смеси, если известны плотности компонентов ![]() ,
, ![]() и смеси
и смеси ![]() .
.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 |



