1.5. ЗАКЛЮЧЕНИЕ ПО ОБЗОРУ ЛИТЕРАТУРЫ
Бактерии Pseudomonas aeruginosa при инфицировании восприимчивых видов реализуют факторы вирулентности, связанные с синтезом экзотоксинов (гемотоксин, лейкоцидин, цитотоксины) и эндотоксина липополисахаридной природы, что обусловливает многообразие клинических проявлений болезней, вызываемых данной группой бактерий. Установлено, что популяции бактерий P. aeruginosa, выделенные из объектов внешней среды, характеризуются психрофильностью, метаболической пластичностью, ростом на обедненных средах с сохранением вирулентности Особенностью псевдомонад является наличие широкого спектра факторов вирулентности (Bodey G. RP. et al., 1983; Rocha C. L. et al., 2003; Scharmann W. 1976). Адгезия P. aeruginosa к абиотическим поверхностям обусловлена неспецифическими взаимодействиями (например, за счет разницы заряда), адгезия к живым тканям осуществляется путем контакта с рецепторами эукариотической клетки (,1985; , 1988; DholakiaP. M., 1985). Сравнительное электронно-микроскопическое исследование штаммов P. aeruginosa показало, что клетки вирулентных штаммов имеют слизеподобную капсулу, в которой различимы два слоя – внутренний ригидный, тесно связанный с клеточной стенкой, и наружный, более тонкий, гомогенный. На поверхности наружного слоя были обнаружены множественные мелкие шаровидные образования (, 1983). Данные образования определяют адгезивные свойства, обеспечивающие прикрепление бактерий к различным субстратам. Клетки авирулентных штаммов слизеподобной капсулой не обладают и имеют типичную для большинства грамотрицательных бактерий структуру. В присутствии очищенного полисахарида слизи адгезивные свойства мукоидных штаммов P. aeruginosa повышаются на 30-50 % (Ramphai R., 1985). На основании анализа данных литературы сделано заключение, что функционирование факторов патогенности имеет общие закономерности, связанные со способностью к опознаванию специальных рецептов, взаимодействию и как следствие, проявлению адгезивных свойств, колонизации эпителия, затем нарушению функций иммунной системы, диссеминации возбудителей в ткани и органы, развитию инфекционно-аллергических реакций, длительной персистенции возбудителей в организме.
Учитывая, биологию микроорганизмов семейства Pseudomonaceae, методы обнаружения бактерий построены по общему принципу: посев исследуемого материала на плотные дифференциально-диагностические среды для выделения псевдмонад («Cetrimide agar»), кроме того, для выделения псеввдомонады, неразведенные пробы засевают в среды обогащения (селенитовый бульон). Грамотрицательные культуры микроорганизмов пересевают в пробирки со скошенным мясопептонным агаром, для дальнейшего изучения ферментативных, антигенных и патогенных свойств.
Pseudomonas aeruginosa способны к формированию биопленок на поверхностях, контактирующих с водой. Эти биопленки считаются потенциально опасными, так как могут содержать и другие патогены. Кроме того, они приводят к повреждению поверхностей, к которым прикрепляются, демонстирует высокую резистентность и проявляет рост устойчивости к антибиотикам. aeruginosa обладает множественной лекарственной устойчивостью (, 1988; , 1999; , 1986; Clements J. A., 1962; Sonntag C., 1986) и даже способна к контаминации растворов антибиотиков. Это является характерной и важной особенностью псевдомонадов.
Среди различных видов рода Pseudomonas, P. aeruginosa является самым распространенным возбудителем порчи пищевых продуктов. Известно, что P. aeruginosa особенно часто выделяются из богатых белками пищевых продуктов (мясо, птица, рыба) (Ali Luzan A., 1982; Bower et al., 1996; Iroha I. R. et al.,2011), хранившихся при низких температурах (Gram et al., 2002). Употребление пищевых продуктов, контаминированных P. aeruginosa, при наличии предрасполагающих факторов может привести к инфекциям мочеполовой и дыхательной систем, дерматитам, инфекции мягких тканей и бактериемии. Описаны вспышки пищевых токсикоинфекций псевдомонадной этиологии и обнаружение P. aeruginosa в пищевых продуктах, что характеризует последние как возможный источник пищевой токсикоинфекции (Huang Meizi. et al.,2003; Shen Ying. et al.,2010; He Lanxiang, et al.,2012). Острые кишечные инфекции псевдомонадной этиологии клинически протекают в виде диарей той или иной тяжести, особенно тяжело у детей, пожилых людей и больных хроническими заболеваниями, а при пищевых токсикоинфекциях со всеми признаками этиопатогенеза этого типа заболеваний. Факторы вирулентности P. aeruginosa включают детерминанты, позволяющие вызывать заболевания различных видов восприимчивых организмов и детерминаты, специфичные для определенного вида. При инфицировании эволюционно различных видов восприимчивых организмов P. aeruginosa экспрессирует разные факторы патогенности, вызывая проявление соответствующих клинических признаков.
ГЛАВА 2. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЙ
Работа выполнена в период с 2011 по 2015 гг. на кафедре «Ветеринарная медицина» ФГБОУ ВПО «МГУПП», часть исследований в лаборатории «Санитарная микробиология» ФГБНУ «ВНИИВСГЭ».
В работе использовали паспортизированные штаммы: P. aeruginosa ATCC 9027; P. fluorescens; P. putida; A. hydrophila; S. enteritidis; S. typhimurium № 000; E. coli 0141:K87:K88, № 000; K. pneumonia; C. freundii №33/57; E. aerogenes CCM 2531; Y. enterocolitica 09, № 000, полученные из коллекции ФГУ ВГНКИ, Государственного НИИ стандартизации и контроля медицинских биологических препаратов им. . С целью выделения бактерий исследовали 6 проб фарша из мяса птицы и 5 проб фарша из свинины, 5 проб фарша из говядины; 10 проб живых рыб (карпа); 8 проб свежих креветок.
С целью изучения морфологии бактерий и изменчивости бактерий при воздействии антибактериальных препаратов использовали микроскоп «H604 TTrinocularUnico» (США); цифровой видеоокуляр «DCM510 SCOPE» (Германия); стереоскопический микроскоп «БИОМЕД МС – 1 Стерео» (Россия); электронный микроскоп «Hitachi-800» со сканирующей приставкой (Япония).
2. 1. Методы индикации и идентификации Pseudomonas aeruginosa
Пробы пищевых продуктов для бактериологических исследований отбирали в количествах, предусмотренных нормативными документами: ГОСТ 26668-85 (СТСЭВ 3013-81) «Продукты пищевые и вкусовые. Методы отбора проб для микробиологического анализа»; ГОСТ 7269-79 «Мясо. Методы от-бра образцов и органолептические методы определения свежести»; СанПиН 2.3.2.1078-01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов». Отбор проб воды проводили согласно методик отбора проб на гидрохимические (Методики гидрохимических исследований проб из рыбохозяйственных водоемов № 000 – 6а от 01.01.2001 г. М: печатный цех МСХ СССР. 1983. 37 с.) и бактериологические исследования (ГОСТ Р 51592 – 2000. Вода. Общие требования к отбору проб).
Исследования проводили в соответствии с «Методическими рекомендациями обнаружение и идентификация Pseudomonas aeruginosa в объектах окружающей среды (пищевых продуктах, воде, сточных жидкостях) (1984), ГОСТ 10444.15-94 «Продукты пищевые. Методы определения количества мезофильных аэробных и факультативно-анаэробных микроорганизмов»; ГОСТ 30519-97 (ГОСТ Р 50474-93) «Продукты пищевые. Методы выявления и определения количества бактерий группы кишечных палочек (колиформных бактерий)»; ГОСТ Р 54755-2011 «Продукты пищевые. Методы выявления и определения количества бактерий вида Pseudomonas aeruginosa». При определении чувствительности бактерий к антибактериальным препаратам использовали методы диффузии в агар и серийных разведений в 0,7%-ном МПА (МУК 4.2.1890-04. Определение чувствительности микроорганизмов к антибактериальным препаратам).
С учетом биологии микроорганизмов P. aeruginosa бактериологическое исследование feces, продуктов животного происхождения и окружающей среды осуществляли с использованием одних и тех же сред обогащения и плотных питательных сред.
На первом этапе проводили высевы на МПА. Гемолитические свойства микроорганизмов изучали на агаре Хоттингера с добавлением 5,0 % цельной крови барана, через 24 ч культивирования при 37°С. Учет проводили на 2, 5, 7 и 10-е сутки. Пробы пищевых продуктов помимо среды обогащения высевали на среду МПА и агар с цетримидом. Чашки с посевами инкубировали при 22-28 °С и производили просмотр через 24-48 ч. С плотной среды характерные колонии псевдомонад пересевали в пробирку со скошенным агаром или в чашку с МПА и проводили дальнейшую идентификацию. Для определения формы бактериальных клеток, расположения относительно друг друга, размера и способности к окраске анилиновыми красителями (тинкториальные свойства) готовили мазки из чистых бульонных и агаровых культур, окрашивали по Граму. Ферментативные свойства изучали на средах Гисса с мальтозой. Для определения присутствия оксидазы использовали ОКСИ-тест. Для подтверждения редукции нитратов проводили посевы в пробирки с нитратной среды, через 48 ч культивирования при 37°С добавляли 1,0 %-ный водный раствор крахмала и затем 10,0 %-ный раствор серной кислоты. Появление тёмно-синего окрашивания – положительный результат. Схема бактериологического выделения и идентификации Pseudomonas aeruginosa, предложенная , . Посев на накопительную среду УСХИ (37°С 24-48 часов). Перенос бактериальной суспензии на элективную среду КМ УСХИ (37°С – 24 часа). Пересев выделенных колоний на ацетамидный агар, питательный агар с хлоридом бария, МПА (42°С – 24 часа). По результатам культивирования - идентификация выделенной культуры (рис. 5). Схема бактериологического выделения и идентификации Pseudomonas aeruginosa, предложенная по ГОСТу Р 54755 – 2011 (рис.1).
Основными дифференциальными признаками бактерий Pseudomonas aeruginosa являются: аэробные не образующие спор грамотрицательные оксидазоположительные палочки, образующие пигменты флюоресцин и пиоционин, не ферментирующие мальтозу, вывающие редукцию нитратов. 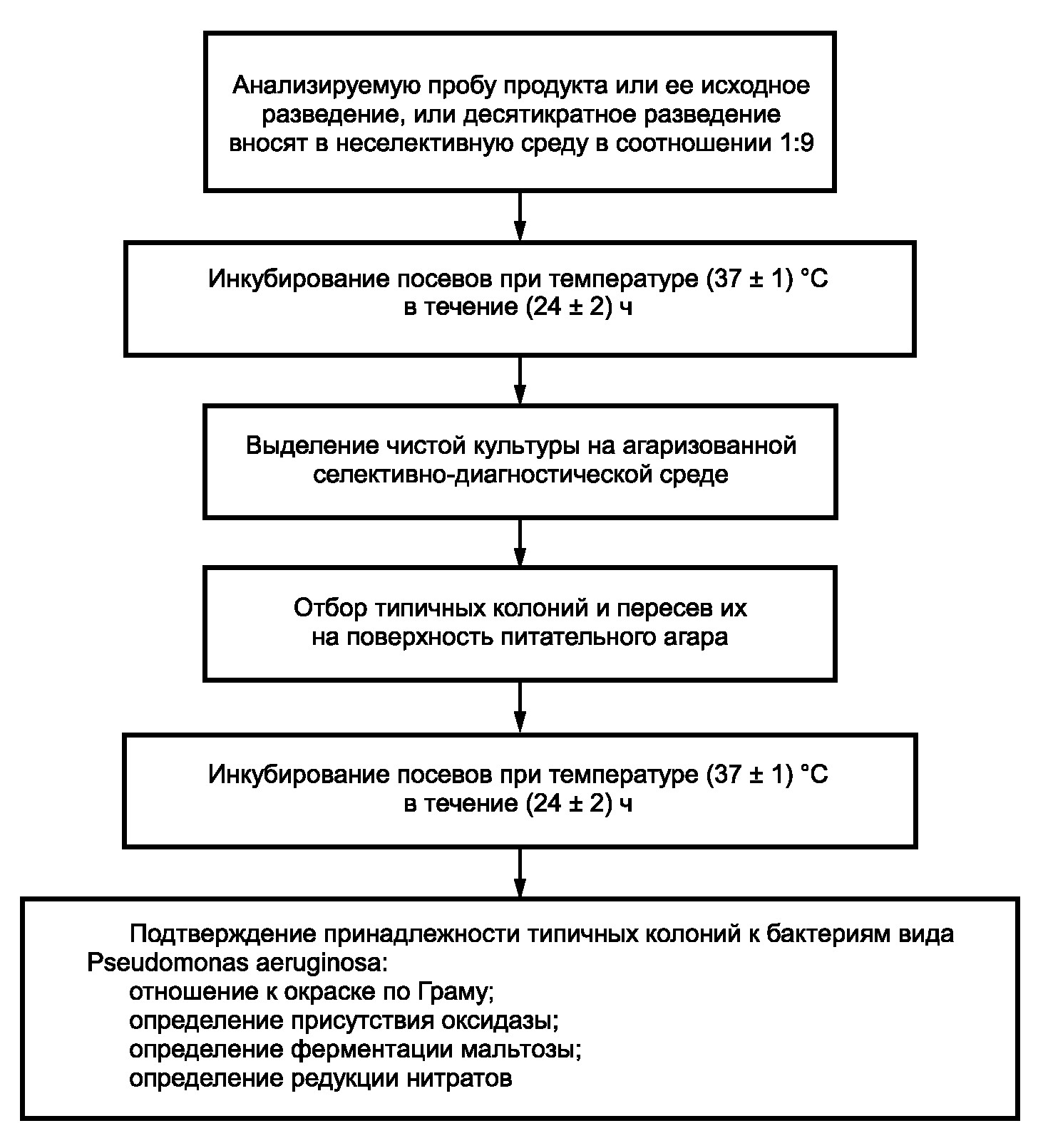
Рис. 1. Схема бактериологического исследования на наличие бактерий P. aeruginosa

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



