Спиновое квантовое число, ms – параметр, характеризующий угловой момент импульса электрона.
Сплав – система, образующаяся при кристаллизации расплавленной смеси металлов.
Сопряженная система - система, в которой имеет место чередование простых и кратных связей, либо соседство атома, имеющего вакантную р-орбиталь или неподеленную пару р-электронов
Стандартная энтальпия образования, ![]() – тепловые эффекты реакций образования веществ в стандартном состоянии (298,150К и давлении 1 атм).
– тепловые эффекты реакций образования веществ в стандартном состоянии (298,150К и давлении 1 атм).
Стереоизомеры – соединения, имеющие одинаковое химическое строение, но отличающиеся расположением атомов в пространстве
Тепловой эффект реакции – изменение энергии системы при протекании в ней химической реакции при условии, что система не совершает никакой другой работы, кроме работы расширения.
Теплоемкость – количество теплоты, которую необходимо затратить для нагревания 1 г или 1 моль вещества на 1 градус (или на один кельвин).
Теплота (энтальпия) образования, ![]() – тепловой эффект реакции образования 1 моль сложного вещества из простых веществ.
– тепловой эффект реакции образования 1 моль сложного вещества из простых веществ.
Химическое равновесие – состояние системы, при котором скорости прямой и обратной реакций равны.
Химическая коррозия – разрушение металла в результате химического взаимодействия с окружающей средой.
Щелочные металлы – общее название элементов главной подгруппы I группы, в которую входят литий, натрий, калий, рубидий, цезий и франций.
Энергетический эффект реакции – тепловой эффект реакции.
Энергия гидратации ионов – количество энергии, выделяющееся при взаимодействии ионов с молекулами воды, когда свободные ионы переходят в водный раствор.
Энтальпия – одна из важнейших термодинамических функций, характеризующих состояние вещества.
Энтропия – термодинамическая функция, являющаяся мерой хаотичности, неупорядоченности системы.
Электрометаллургия – катодное восстановление металлов из растворов или расплавов их солей.
Электролиз – совокупность реакций, происходящих в растворах или расплавах электролитов при прохождении через них постоянного электрического тока.
Электронная конфигурация – распределение электронов по орбиталям.
Электрохимическая коррозия – разрушение металла под действием окружающей среды в результате возникновения гальванических пар.
Электрофильные реакции – реакции, в которых образование новой связи осуществляется за счет электронов субстрата
Электрофильные реагенты – это катионы или молекулы, содержащие атомы с незаполненными электронными орбиталями, действие которых связано с приобретением электронной пары в ходе реакции
Энергия связи – энергия, необходимая для разрыва химической связи.
Эффект сопряжения или мезомерный эффект (М) – процесс передачи электронного влияния заместителя по сопряженной системе р-связей.
Функциональная группа – структурный фрагмент молекулы, характеризующий свойства соединений данного класса
Химическая номенклатура – совокупность названий индивидуальных химических веществ, их групп и классов, а также правила составления их названий
Ядро – положительно заряженная частица, в которой практически сосредоточена вся масса атома. Заряд ядра атома элемента равен его порядковому номеру.
Лекции
Модуль 1. Основные законы.
Введение. Основные понятия и законы химии
Введение. Атомно - молекулярное учение Основные стехиометрические законы химии Законы газового состояния.Введение. Атомно-молекулярное учение.
Химия является одной из естественных наук.
Весь окружающий нас мир представляет собой движущуюся материю в ее бесконечно разнообразных формах и проявлениях.
Две такие формы проявления материи – это вещества и поля.
Вещество – это вид материи, состоящей из дискретных частиц, имеющих массу покоя. Например, молекул, атомов, электронов, атомных ядер. Поле – это такая форма существования материи, которая характеризуется, прежде всего, энергией. Посредством поля осуществляется связь и взаимодействие между частицами вещества.
Химия изучает качественный и количественный состав вещества. Качественный состав показывает из каких химических элементов состоит данное вещество, количественный состав указывает в каких количественных соотношениях находятся составляющие его элементы.
Задачей химии является изучение строение вещества, т. е. выяснение, из каких частиц состоит данное вещество, с помощью каких сил связаны между собой эти частицы и как они расположены в пространстве.
Химия изучает также физические и химические свойства веществ. Физические свойства: внешний вид вещества, его температуры плавления и кипения, способность проводить тепло и электрический ток, агрегатное состояние (твердое, жидкое, газообразное). Химические свойства вещества характеризуют его способность превращаться в другие вещества. Такие превращения называются химическими реакциями.
Важной задачей химии является разработка методов получения веществ, обладающих необходимыми свойствами, т. е. методов синтеза химических веществ.
Таким образом, химия изучает состав, строение, свойства и превращения веществ. Также она занимается разработкой методов их получения и очистки.
В настоящее время известно около 10 млн. различных природных и искусственно полученных веществ. В истории химии можно выделить несколько периодов.
Первый период. Зарождение и развитие химического искусства (с древнейших времен до середины XVII века).
Второй период. Становление химии как науки (со второй половины XVII в. до конца XVIII в.).
Третий период. Развитие химической науки на основе кислородной теории и атомно-молекулярного учения (с конца XVIII в. до 60-х гг. XIX в.)
Четвертый период. Превращение химии в современную науку (с 60-х годов XIX в.).
В конце XIX в. внимание химиков все больше привлекается к исследованию химических реакций и законов, которым они подчиняются. Развивается физическая химия, основы которой были заложены . Появилась химическая теория растворов , были исследованы свойства разбавленных растворов, была создана теория электролитической диссоциации, развивались стереохимия и термодинамика, учение о скорости химических реакций и катализе.
Как одна из отраслей естествознания химия тесно связана с другими науками (биохимия, геохимия, физическая химия, космохимия, электрохимия и др.)
В настоящее время не существует ни одной отрасли техники и технологии, где не используются химические вещества и не осуществляются химические процессы. Применение законов химии позволяет совершенствовать существующие и создавать новые процессы, технологии и материалы.
Вот несколько актуальных направлений применения химии:
1) новые источники энергии (получение ракетного топлива, ядерного горючего, создание устройств для преобразования солнечной энергии в электрическую, разработка новых химических источников электрического тока);
2) новые материалы (производство синтетических материалов; создание новых оптико-волокнистых материалов; разработка микроэлектроники и молекулярной электроники, основанных на физико-химических процессах);
3) проблемы сельскохозяйственного производства (повышение урожайности сельскохозяйственных культур за счет развития производства минеральных удобрений, разработки средств борьбы с болезнями растений и их вредителями; увеличение продовольственных ресурсов и сырья для легкой промышленности за счет производства синтетических тканей, красителей, заменителей жиров и т. д.);
4) охрана окружающей среды (разработка методов обнаружения и количественного определения вредных примесей; создание безотходных или малоотходных производств; разработка способов обезвреживания и утилизации промышленных и бытовых отходов).
Атомно - молекулярное учение
Атомы – мельчайшие химические частицы, являющиеся пределом химического разложения любого вещества.
Химический элемент представляет собой вид атомов с одинаковым положительным зарядом ядра.
Другими словами, атом – это наименьшая частица химического элемента, сохраняющая все его химические свойства.
В настоящее время известно 117 химических элементов, из которых 92 встречаются в природе.
Абсолютное большинство различных веществ состоит из молекул.
Молекула – наименьшая частица вещества, способная существовать самостоятельно и сохраняющая его основные химические свойства.
Массы атомов химических элементов чрезвычайно малы: ~ 10-27 – 10-25 кг. В химии пользуются относительными значениями масс атомов (Ar, где r – «относительный», от англ. relative).
Относительная атомная масса – это масса атома, выраженная в атомных единицах массы. За атомную единицу массы принята 1/12 часть массы атома нуклида ![]() :
:
1 а. е.м. = 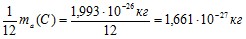 .
.
Относительная атомная масса – величина безразмерная.
Соответственно, относительная молекулярная масса Mr вещества – это масса его молекулы, выраженная в а. е.м.
Единицей измерения количества вещества (n) является моль.
Моль – количество вещества, содержащее столько структурных элементарных единиц (атомов, молекул, ионов, электронов и т. д.), сколько содержится атомов в 0,012 кг изотопа углерода 12С.
Число атомов NA в 0,012 кг углерода, или в 1 моль, легко определить следующим образом:
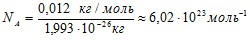 .
.
Величина NAназываетсяпостоянной Авогадро.
Вещество – это конкретный вид материи, обладающий определенными физическими и химическими свойствами, состав которого может быть выражен химической формулой.
Химической реакцией называется процесс превращения одних веществ в другие.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 |



