1. Соединения, содержащие амино - и карбоксильную группы, называются аминокислотами. В зависимости от расположения функциональных групп, различают б, в, г - аминокислоты.
2. Способы получения аминокислот:
1. Замена галогена в галогензамещенных кислотах на аминогруппу при действии избытка аммиака
2. действием цианида аммония на альдегиды и кетоны
3. присоединение аммиака к альфа, бетта-непредельным кислотам.
4. действие альдегидов и аммиака на малоновую кислоту
5. восстановление нитрозамещенных кислот.
3. Химические свойства
1. образование соелй с кислотами и основаниями
2. реакции по карбоксильной группе
А) образование сложных эфиров
Б) образование амидов
В) образование аминов
3. Реакции по аминогруппе
А) взаимодействие с хлорангидридами
Б) взаимодействие с алкилами
В) взаимодействие с азотистой кислотой
Г) взаимодействие с бензойным альдегидом.
4. образование дикетопиперазинов, непредельных кислот и лактамов при нагревании.
Вопросы для самоконтроля:
1. выведите все изомеры аминокислот состава С4Н9О2N. Назовите их
В чем проявляется амфотерность аминокислот? Приведите примеры.
3. напишите схему образования дипептида из молекулы глицина и молекулы аланина.
Рекомендуемая литература:
1. ачала органической химии. М., Химия, 1974
2.рганическая химия. Высшая школа. 1990
3.Роберт Дж., сновы органической химии. М., 1978
Лекция 14 – Углеводы
Содержание
1. Классификация углеводов
2. строение углеводов
3. Химические свойства
1.
Моносахариды | Дисахариды С12Н22О11 | Полисахариды |
Тетрозы С4Н8О4 Эритроза Триоза Пентозы С5Н10О5 Арабиноза Ксилоза Рибоза Гексозы С6Н12О6 Глюкоза Манноза Галактоза Фруктоза | Сахароза Мальтоза Лактоза Целлобиоза | (С5Н8О4)n Пентозаны (С6Н10О5)n Целлюлоза Крахмал Гликоген |
2. Существуют альдегидные и циклические форму углеводов
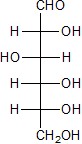
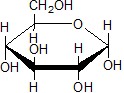
Д-глюкоза (альдегидная форма) циклическая форма
3. Химические свойства:
1. восстановление
2. окисление.
3. присоединение синильной кислоты
4. реакция с фенилгидразином
5. алкилирование
6. ацилирование
7. расщепление углеродной цепи
8. эпимеризация моносахаридов
9. действие кислот
Вопросы для самоконтроля:
1. напишите структурные формулы альдогексозы, альдогептозы, кетопентозы, кетогептозы.
2. Что такое циклическая б-форма и циклическая в-форма моносахаридов?
3. Напишите схему синтеза альдогексоз из L-арабинозы окиснитрильным способом.
Рекомендуемая литература:
1. ачала органической химии. М., Химия, 1974
2.рганическая химия. Высшая школа. 1990
3.Роберт Дж., сновы органической химии. М., 1978
Лекция 15 - Основные группы биологически активных соединений и важнейших метаболитов
Содержание:
1. Белки, строение, функции
2. Нуклеиновые кислоты, строение, функции
Белки являются основным органическим веществом, из которого построены клетки животного организма (в растительных клетках белка содержится меньше).
Функции белков в организме универсальны: ферментативная, структурная, рецепторная, сократительная, защитная, транспортная, регуляторная.
При взаимодействии двух молекул б-аминокислот происходит реакция между аминогруппой одной молекулы и карбоксильной группы - другой. 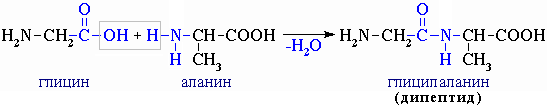
Молекулярные массы различных белков (полипептидов) составляют от 10 000 до нескольких миллионов. Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Несмотря на многочисленность белков, в их состав входят остатки лишь 22 ?-аминокислот.
Функции белков в природе универсальны:
- каталитические (ферменты); регуляторные (гормоны); структурные (кератин шерсти, фиброин шелка, коллаген); двигательные (актин, миозин); транспортные (гемоглобин); запасные (казеин, яичный альбумин); защитные (иммуноглобулины).
Выделяют 4 уровня структурной организации белков.
Нуклеиновые кислоты осуществляют хранение, воспроизводство и реализацию генетической информации, управляют точным ходом биосинтеза белков в клетках. Нуклеиновые кислоты - это биополимеры, макромолекулы которых состоят из многократно повторяющихся звеньев - нуклеотидов. Поэтому их называют также полинуклеотидами.
В состав нуклеотида - структурного звена нуклеиновых кислот - входят три составные части:
1. азотистое основание - пиримидиновое или пуриновое
2. моносахарид - рибоза или 2-дезоксирибоза;
3. остаток фосфорной кислоты.
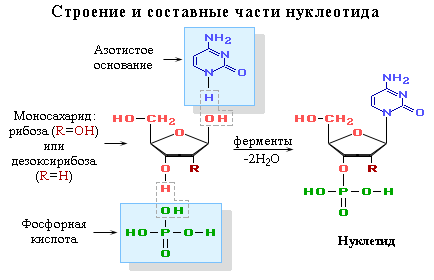
Нуклеотид - фосфорный эфир нуклеозида. В состав нуклеозида входят два компонента: моносахарид (рибоза или дезоксирибоза) и азотистое основание
Вопросы для самоконтроля:
1. Напишите проекционные формулы оксикарбонильной формы моносахаридов, входящих в состав нуклеиновых кислот: D-рибозы, 2-дезокси-D-рибозы.
2. Напишите формулы дезоксирибонуклеозидов: 2-дезоксицитидина, 2-дезокситимидина.
3. напишите схемы образования и формулы аденозина, 2-дезоксигуанозина.
Рекомендуемая литература:
1. ачала органической химии. М., Химия, 1974
2. рганическая химия. Высшая школа. 1990
3. Роберт Дж., сновы органической химии. М., 1978
Лабораторные занятия
Лабораторное занятие 1 – Алканы
Цель занятия: Изучение свойств алканов
Ход занятия: Опыт 1. Бромирование углеводородов
В сухую пробирку помещают 1 мл исследуемого углеводорода (или смеси углеводородов) и добавляют по каплям при легком встряхивании раствор брома. Если желтая окраска не исчезает на холоду, то смесь слегка нагревают. Устанавливают, сопровождается ли исчезновение окраски, обусловленной присутствием свободного брома, образованием бромистого водорода — газа, имеющего резкий запах, дымящего на воздухе (особенно при внесении в пробирку палочки, смоченной аммиаком) и окрашивающего влажную синюю лакмусовую бумажку в красный цвет. Выделение бромистого водорода хорошо заметно на темном фоне при встряхивании пробирки, если слегка подуть над ее отверстием.
Опыт 2. Окисление углеводородов перманганатом калия (реакция Вагнера)
К 1 мл исследуемого вещества добавляют сначала равный объем раствора соды и затем постепенно по каплям при сильном взбалтывании раствор перманганата калия до прекращения изменения внешнего вида смеси.
Опыт 3. Взаимодействие углеводородов с концентрированной серной кислотой
К 1 мл вещества (смеси углеводородов) добавляют 1 мл концентрированной серной кислоты и сильно, но осторожно взбалтывают несколько минут, охлаждая пробирку в воде. Отмечают различное отношение насыщенных и ненасыщенных углеводородов к концентрированной серной кислоте.
Опыт 4. Взаимодействие углеводородов с концентрированной азотной кислотой
К 1 мл исследуемого вещества добавляют 1 мл концентрированной азотной кислоты и встряхивают смесь сначала осторожно, затем энергично в течение нескольких минут. Отмечают различное отношение насыщенных и ненасыщенных углеводородов к примененному реактиву.
Опыт 5. Образование и свойства метана
Небольшие количества метана и этилена удобно получать в пробирке со вставленной на пробке (или на резиновом колечке) короткой газоотводной трубкой. К последней присоединяют каучуковую трубочку длиной 10—12 см со стеклянным наконечником. Такая гибкая конструкция для отвода газа облегчает дальнейшую работу.
В сухую пробирку помещают несколько граммов тщательно растертой в ступке смеси из 1 вес. ч. какого-либо безводного ацетата и 2 вес. ч. натронной извести. Укрепляют пробирку горизонтально и, присоединив газоотводную трубку, нагревают смесь в пробирке пламенем горелки сначала осторожно, затем сильно. Опуская газоотводную трубку в отдельные пробирки с бромной водой и раствором перманганата калия, устанавливают, изменяется ли окраска этих реактивов выделяющимися пузырьками газообразного углеводорода происходит ли бромирование метана или его окисление. Не прекращая нагревания, собирают метан в наполненную" водой пробирку, опрокинутую в стакан или ванну с водой. Затем вынимают газоотводную трубку из воды и прекращают нагревание. Закрыв пробирку пальцем, подносят ее к пламени горелки и открывают. Метан спокойно сгорает голубоватым пламенем. После этого можно поджечь метан и у конца газоотводной трубки. При внесении в пламя горящего метана фарфоровой пластинки (чашки, крышки от тигля) на ней не образуется черного пятна сажи.
Вопросы для самоконтроля:
1. Какие типы реакции характерны алканам и алкенам?
2. Как протекает реакции галогенирования алканов и алкенов?
3. Какие соединения образуются при окислении алканов и алкенов?
Лабораторное занятие 2 – Алкены
Цель занятия: Изучение образования и свойств алкенов
Ход занятия: Опыт 1. Бромирование углеводородов
В сухую пробирку помещают 1 мл исследуемого углеводорода (или смеси углеводородов) и добавляют по каплям при легком встряхивании раствор брома. Если желтая окраска не исчезает на холоду, то смесь слегка нагревают. Устанавливают, сопровождается ли исчезновение окраски, обусловленной присутствием свободного брома, образованием бромистого водорода — газа, имеющего резкий запах, дымящего на воздухе (особенно при внесении в пробирку палочки, смоченной аммиаком) и окрашивающего влажную синюю лакмусовую бумажку в красный цвет. Выделение бромистого водорода хорошо заметно на темном фоне при встряхивании пробирки, если слегка подуть над ее отверстием.
Опыт 2. Окисление углеводородов перманганатом калия (реакция Вагнера)
К 1 мл исследуемого вещества добавляют сначала равный объем раствора соды и затем постепенно по каплям при сильном взбалтывании раствор перманганата калия до прекращения изменения внешнего вида смеси.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 |



