2. Реакция комплексообразования:
Ni2+ + 6NH4OH = [Ni2+(NH3)6]2+ + 6H2O
Взаимодействие с молекулами растворителя. Это процессы гидратации, гидролиза, образования оксоанионов и оксокатионов.Вопросы для самоконтроля
Охарактеризуйте физические и химические свойства, характерные для всех металлов. Напишите электронные формулы одноатомных катионов, образуемых магнием, марганцем, цезием, железом, галлием, серебром. Какой из перечисленных катионов может окислить железо до Fe2+:Sn2+, Ni2+, Cu2+, K+, Al3+, Ag+. Составьте уравнения реакций: а) окисления меди разбавленной и концентрированной азотной кислотой; б) окисления цинка концентрированной серной кислотой; в) взаимодействия олова с концентрированным раствором щелочи; г) восстановления оксида меди(II) углем. Почему явление комплексообразования для d-элементов характернее, чем для s - и p-элементов?Рекомендуемая литература:
1. , Неорганическая химия,2012 с. 209-226;
2. Задачи и упражнения по общей химии,1988,с. 215- 255;
3. Общая и неорганическая химия, 1997, с.
Модуль 1.
3 ЛАБОРАТОРНЫЕ ЗАНЯТИЯ
Лабораторное занятие № 1. Химические свойства кислот, оснований, солей, оксидов и их получения
Цель занятия: Изучить основные химические свойства классов неорганических соединений
Оксиды
ОПЫТ №1 Получение оксидов непосредственным окислением элементов. Поместить на металлическую ложечку кусочек серы и нагреть в пламени спиртовки. Как только сера загорится внести ложечку в банку, не касаясь дна и стенок. Когда сера сгорит, ложечку вынуть, в банку налить немного дистиллированной воды и взболтать. Испытать раствор лакмусом. Написать уравнение реакции. Каков характер оксида? Сделайте вывод.
ОПЫТ №2 Получение оксидов разложением солей. В сухую пробирку поместить немного основного карбоната меди ((СиОН)2С03). Держа пробирку в наклонном положении, нагреть до полного разложения соли. Какого цвета вещество остается? Что выделяется на холодных стенках пробирки? Написать уравнение реакции. Сделайте вывод.
ОПЫТ №3 Получение оксидов разложением гидроксидов.
На раствор сульфата меди действуем избытком щелочи, получаем гидроксид меди. Полученный осадок нагреть. Объяснить почернение осадка и написать уравнение реакции. Сделайте вывод.
ГИДРОКСИДЫ
ОПЫТ №4 Взаимодействие с кислотами. В пробирку налейте несколько капель раствора гидроксида натрия. Добавьте 1 -2 капли фенолфталеина, затем по каплям приливайте раствор соляной кислоты. Что наблюдается? Напишите уравнение реакции. Сделайте вывод.
К ислоты
ОПЫТ №5 Взаимодействие кислот с металлами. В пробирку с 3-4 мл. серной кислоты (разб.) опустить кусочек цинка, пробирку нагреть до кипения. Что наблюдается? Написать уравнение реакции. Сделайте вывод.
Соли
ОПЫТ №6 Взаимодействие двух различных солей. К 1 мл. раствора сульфата натрия прилить 1 мл. раствора хлорида бария. Что наблюдается? Написать уравнение реакции. Сделайте вывод.
Вопросы для самопроверки и защиты лабораторной работы:
Дайте определения с позиций теории электролитической диссоциации кислотам, основаниям и солям. Классифицируйте неорганические соединения по составу (бинарные и многоэлементные) и по свойствам (функциональным признакам)ЛАБОРАТОРНОЕ ЗАНЯТИЕ № 2
Определение эквивалентной массы металла
Цель работы: Определить эквиваленты активных металлов, способных вытеснять водород из разбавленных кислот: магния, цинка, алюминия, хрома, марганца и др.
Определение эквивалента металла производится в приборе, собранном из
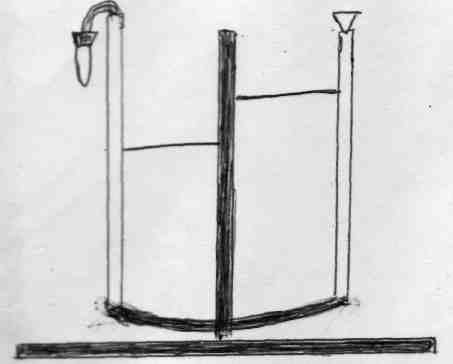
двух бюреток (см. рисунок), закрепленных в лапках штатива. Бюретки соединяют между собой резиновой трубкой. Перед опытом бюретки заполняются водой так, чтобы уровень воды был чуть ниже нулевого деления. Собранный прибор проверяют на герметичность. Для этого к бюретке присоединяют пробирку, а бюретку с открытым концом опускают вниз на 15-20 см, если прибор герметичен, то уровень в закрытой бюретке, после незначительного понижения, остается без изменения.
Убедившись в герметичности прибора, бюретки устанавливают так, чтобы вода в них была на одном уровне, и приступают к опыту.
В пробирку налить через воронку 4-5 мл разбавленной соляной кислоты /1:3/ и добавить 3 капли раствора сульфата меди. Следите, чтобы верхняя часть пробирки была сухой. Получите у лаборанта навески металла и запишите массу в лабораторную тетрадь. Металл поместите в верхнюю часть пробирки (пробирку при этом держать возможно ближе к горизонтальному положению). Закройте пробирку резиновой пробкой, слегка смоченной водой, и снова проверьте герметичность прибора. Закрепите бюретки так, чтобы положение воды в них было на одном уровне. Отметьте уровень воды в бюретке с пробиркой и запишите в тетрадь. Чтобы правильно замерить уровень воды в бюретке, глаз наблюдателя должен находится на одном уровне с нижним менисом воды.
Наклоните пробирку так, чтобы металл упал в кислоту. Выделяющийся газ при воздействии металла с кислотой (водород) вытесняет воду из бюретки. Когда весь металл растворится, отметьте уровень воды в бюретке с пробиркой и запишите его в таблицу.
Отметить показания барометра и термометра и записать их в тетрадь.
ФОРМА ЗАПИСИ
Масса металла ______________ m (г) Уровень воды в бюретке с пробиркой:а) до опыта V1_______________ (мл)
б) после опыта V2____________ (мл)
в) температура опыта t0________
Атмосферное давление Р aтм______(мм рт. ст.)
Давление насыщенного пара Р пар_____(мм рт. ст.)ВЫЧИСЛЕНИЯ
Объем выделившегося водорода V, H2 = V2 –V1 (мл) Абсолютная температура Т=273 + t0 Давление водорода РН 2 = Р aтм - Рпар (мм рт. ст.) Объем эквивалента водорода при нормальных условиях:V Н2 = 22,4л/2 = 11,2 л = 11200 (мл)
Объем выделившегося водорода, приведенный к нормальным условиям:V0*P0 = V*P V0 = PH2 * VH2* 273 = PH2 * VH2
Т0 Т 760* Т 2,78*Т
6. Эквивалентная масса металла:
M = V0 Эмет = m*Vэ H2 = m*11200
Эмет VэН2 V0 V0
7. Показав результаты преподавателю и узнав точное значение
эквивалентной массы металла, рассчитайте относительную ошибку опыта в процентах:
П = (Этеор.-Э эксп.).100%
Этеор.
Вопросы для самопроверки и защиты лабораторные работы:
1.. От чего зависит эквивалент химического элемента?
2. Как находят эквиваленты сложных веществ?
3. Что такое эквивалент и эквивалентная масса вещества?
4. Одинакова ли эквивалентная масса железа в хлоридах железа (ІІ, ІІІ)?
5. На нейтрализацию 25 мл соляной кислоты с титром 0,036 израсходовано 1,3 г соды, найти эквивалент соды. Ответ: 53г/моль
Модуль 3
ЛАБОРАТОРНОЕ ЗАНЯТИЕ №3
Определение энтальпии нейтрализации.
Цель занятия: Определение энтальпии реакции нейтрализации для реакции нейтрализации:
Оборудование и реактивы:
Калориметр с мешалкой, Термометр Бекмана или термометр с ценой деления 0,1°С 2н. растворы: NaOН, КОН, HNO3, HC1, NH4OH, CH3COOH4. Секундомер (таймер).
5. Мерные цилиндры на 50 мл для каждого раствора.
6. Технохимические (аптечные) весы с разновесами
Ход работы:
Упрошенный калориметр состоит из двух стаканов. В большой стакан вставляют другой стакан меньшего размера. Стаканы не должны между собой соприкасаться Во избежание потерь теплоты через стенки внутреннего стакана калориметра между ними помещают прокладки, внутренний стакан закрывают крышкой с тремя отверстиями в которые вставлены термометр {цена деления 0,1 оС}- мешалка и воронка для вливания растворов. Выполняется 2 опыта с сильными электролитами и 1 со слабыми.
Взвесить внутренний калориметрический стакан на технохимических весах и налить в него 50 мл 2 н. раствора щелочи, отметить температуру раствора с точностью до 0,1 °С (t° шелочи ). Вставить внутренний стакан с раствором шелочи во внешний стакан, закрыть его крышкой, в отверстие крышки поместить мешалку, термометр и воронку. Отмерить цилиндром 50 мл 2 н. раствора кислоты и измерить его температуру ( кислоты).
При непрерывном помешивании быстро прилить через воронку раствор кислоты к раствору щелочи, отметить самую высокую температуру раствора -1 и конечную, которую показывает термометр после смешивания растворов. Вычислить среднюю температуру растворов до реакций - t° начальную (среднее арифметическое из температур растворов кислоты и щелочи), затем рассчитать разницу; Δ t° = t° кон. – t0 нач
Принимая плотность раствора и его удельную теплоемкость равными единице, а удельную теплоемкость стекла равной 0,18 кал/г⋅град, вычисляют по формуле q = ( t2 – t1)Σ c количество выделившегося теплоты, где t2 и t1 конечная и начальная температуры в калориметре; Σ c – теплоемкость системы – сумма теплоемкостей калориметрического сосуда и находящегося в нем вещества, равная c1m1 + c2m2 ; с1 и с2 - удельные теплоемкости стекла и жидкости; m1 и m2 – массы калориметрического стакана и жидкости, находящейся в калориметрическом сосуде.
Для пересчета теплового эффекта на моль вещества пользуются формулой: ΔH = q⋅M/m, где ΔH – тепловой эффект, рассчитанный на моль; m – навеска вещества, взятого для калориметрического опыта; М – молекулярная масса вещества. Тепловой эффект реакции нейтрализации равен – 57кДж/моль, рассчитайте относительную ошибку опыта в процентах:
П = (ΔH теор.- ΔH эксп.)⋅100%
ΔHтеор.
Вопросы для самопроверки и защиты лабораторной работы:
Что называется теплотой образования химического соединения? Привести примеры применения закона Гесса для химических реакций, протекающих через промежуточные стадии Теплоты образования NO и NO2 равны соответственно +21,6 и 7,43 ккал. Будет ли реакция 2NO + O2 = 2NO2 экзотермической или эндотермической и чему равен ее тепловой эффект? Ответ:- 14,13 ккал.ЛАБОРАТОРНОЕ ЗАНЯТИЕ №4

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 |



