1. Показать на примере значения рН для водных растворов средней соли.
2. В каком случае водный раствор средней соли имеет кислую среду.
3. Покажите, как взаимосвязаны между собой рН, рОН.
4. Вычислите концентрацию инов водорода и рН среды, если концентрация гидроксид иона равна 10-8 моль/л и определите характер среды.
Модуль 5
ЛАБОРАТОРНОЕ ЗАНЯТИЕ № 8
Окислительно-восстановительные реакции (ОВР)
Цель работы: Показать оксилительные и восстановительные свойства веществ, показать влияние среды на ход протекания реакций
Опыт № 1. Окислительные свойства бихромата калия.
Налить в пробирку 1-2 мл бихромата калия (К2Сг207), добавить к нему около 1 мл разбавленной серной кислоты (H2S04) и прилить равный объем раствора KI. Наблюдайте пожелтение раствора вследствии выделение йода. Напишите уравнение ОВР. Составьте электронные схемы, обозначив окислитель и восстановитель.
Опыт №2. Восстановительные свойства сульфата желез(ІІ)
Налить в пробирку 1-2 мл перманганатата калия (КМп04). добавить к нему около 2-х мл разбавленной серной кислоты (H2S04) и прилить равный объем раствора FeS04. Наблюдайте обесцвечивание раствора. Напишите уравнение ОВР. Составьте электронные схемы, обозначив окислитель и восстановитель.
Опыт №3. Вытеснение меди из раствора
Налить в пробирку 3-4 мл сульфата меди (CuS04). Зачистить наждачной бумагой железную гвоздь и опустить его в раствор CuS04 Наблюдайте появление выделяемого медно-красного осадка на железном гвозде. Напишите уравнение ОВР. Составьте электронные схемы, обозначив окислитель и восстановитель.
Опыт №4. Окислительные свойства марганцевогокислого калия в зависимости от реакции среды.
A)реакция в кислой среде. Налейте в пробирку 1-2 мл раствора КМп04 и около
2 –х мл разбавленной серной кислоты. Прилейте раствор сернисто-кислого натрия Na2S03 и наблюдайте полное обесцвечивание окраски вследствие образования MnS04. Составьте уравнение реакции, пользуясь таблицей окислителей - восстановителей и принимая во внимание, что Na2S03 окисляется в Na2S04.
Б) реакция в щелочной среде. Налейте в пробирку 1-2 мл раствора КМп04 и около 2-х мл КОН. Прилейте раствор сернисто-кислого натрия Na2S03 и наблюдайте появление зеленой окраски вследствие образования марганцовистого калия К2Мп04. Составьте уравнение реакции.
B)реакция в нейтральной среде. Налейте в пробирку 1-2 мл раствора КМпО4 и прибавьте около 2-х мл Н20. Прилейте раствор сернисто - кислого натрия Na2S03. Наблюдайте выделение бурого осадка диоксида марганца - Мп02. Составьте уравнение реакции, учитывая, что в число исходных веществ входит вода а в число продуктов реакции-гидроксид калия, почему? До каких продуктов восстаноавливается КМп04 в зависимости от реакции среды?
Вопросы для самопроверки и защиты лабораторной работы:
1. Приведите примеры, где элементы в молекулах могут быть только окислителем, только восстановителем, и окислителем, и восстановителем.
2. Дайте определение ОВР, окислитель, восстановитель, окисление, восстановление.
3. Назовите методы для уравнивания ОВР, покажите на примере реакции между соляной кислотой и диоксидом марганца.
ЛАБОРАТОРНОЕ ЗАНЯТИЕ № 9
Гальванический элемент
Цель работы: На основе таблицы окислительно-восстановительных потенциалов составить гальванические элементы и рассчитать э. д.с.
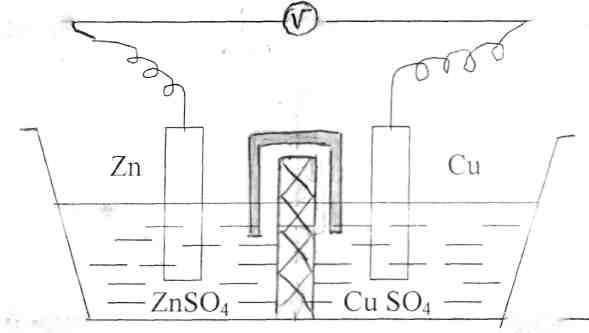
Устройство для непосредственного преобразования энергии химической реакции в электрическую энергию называется гальваническим элементом. Рассмотрим работу медно-цинкового гальванического элемента. Элемент составлен из цинковой пластины, погруженной в раствор сульфата цинка и медной пластины, погруженной в раствор сульфата меди. Оба раствора соприкасаются друг с другом. Рисунок: Схема медно-цинкового гальванического элемента
Они разделены перегородкой из пористого материала, пропускающего сульфат-ионы. При работе гальванического элемента протекает суммарная реакция: Zn + CuSO4 = ZnS04 + Сu
Здесь процессы окисления и восстановления разделены в пространстве, и чтобы осуществить процесс восстановления ионов меди, электроны от окислителя переходят по проводнику, т. е. создают ток по внешней цепи. Цинковый электрод источник электронов, поступающих во внешнюю цепь, принято называть отрицательным (анод), а медный электрод - положительным (катод). Уравнения электродных процессов, протекающих при работе гальванического элемента: анодный процесс, окисление: Zn - 2ё = Zn
катодный процесс, восстановление: Си+2 + 2ё = Си °
Гальванический элемент можно записать в виде краткой электрохимической схемы:
А(-) Zn/ ZnS04// CuSO, /Cu (+) К
А (-) Zn / Zn+2 // Си+2 / Си ° (+) К
где одна черта означает границу между электродами и раствором, две черты - границу между растворами, в скобках знаки электродов, причем анод записывается слева, катод - справа. Необходимое условие работы гальванического элемента - разность потенциалов его электродов. Электрод с меньшим потенциалом является анодом. Электродвижущая сила гальванического элемента (Э. Д.С.) - величина положительная и определяется как разность потенциалов катода и анода.
Э. Д.С = ЕК-Еа
ХОД РАБОТЫ:
Опыт 1. Составление гальванических элементов.
Один из микростаканчиков заполнить I M раствором сульфата цинка, другой - I M раствором сульфата меди. Соединить стаканчики электролитным мостиком, заполненным насыщенным раствором хлорида калия в смеси с агар-агаром. Опустить в раствор сульфата цинка узкую цинковую пластинку, а в раствор сульфата меди - медную. Соединить электрическим проводом опущенные пластинки с гальванометром или другим регистрирующим прибором. Наблюдать отклонение стрелки гальванометра, указывающее на возникновение электрического тока.
Опыт 2. Составление концентрационного гальванического элемента. Наполнить микростаканчики раствором сульфата цинка разной концентрации: первый стаканчик -1 M ZnS04, второй - 0,01 M ZnS04.Соединить стаканчики электролитным мостиком. Опустить в каждый стаканчик цинковые полоски и соединить их проводом с гальванометром. Отклоняется ли стрелка гальванометра? Написать уравнения химических реакций, протекающих на электродах гальванических элементов, и суммарное уравнение химической реакции в результате которой возникает электрический ток в данном элементе. В каком направлении перемещаются электроны во внешней цепи? Выписать из приложения к лабораторному практикуму числовые значения стандартных электродных потенциалов меди и цинка и вычислить ЭДС медно - цинкового элемента. Какие ионы и в каком направлении перемещаются в растворе? Вычислить ЭДС серебрянного концентрационного гальванического элемента. Представить преподавателю отчет письменный на утверждение о проделанной работе.
Вопросы для самопроверки и защиты лабораторной работы:
1. Гальванический элемент (ГЭ) состоит из металлического цинка, погруженного в 0,1М раствора нитрата цинка, и металлического свинца, погруженного в 0,02М раствора свинца. Составьте схему ГЭ, запишите уравнения электродных процессов и вычислите электродвижущую силу (ЭДС) этого процесса.
2. Дайте определение электродному потенциалу, водородному электроду, электродвижущей силе, гальваническому элементу.
3. Никелевые пластины опущены в водные растворы солей: сульфата магния, хлорида натрия, хлорида цинка, нитрата свинца. С какими солями никель будет реагировать?
ЛАБОРАТОРНОЕ ЗАНЯТИЕ № 10
Электролиз растворов
Цель работы: Записывать схему электродных процессовна катоде и аноде при электролизе
В электролизер с раствором КІ, NaCl опустите графитовые углероды и присоедините их к источнику постоянного тока. В около катодное пространство прилейте несколько капель фенолфталеина. Объясните изменение цвета раствора около катода и анода (в случае электролиза КІ), а в случае элктролиза NaCl выделение газа у анода.
По окончании опыта анод промойте раствором тиосульфата натрия для удаления иода, а затем дистиллированной водой. Иодные остатки слейте в специальную банку. В лабораторном журнале нарисуйте электролизер, напишите уравнения электролиза.
Модуль 6
ЛАБОРАТОРНОЕ ЗАНЯТИЕ №11
Комплексные соединения
Цель занятия: Изучить свойства комплексных соединений.
Опыт № 1. Получение комплексных солей
Налить в пробирку 2 мл сульфата меди и по каплям прибавить раствор аммиака. Наблюдать образование осадка основной соли меди (CuOH)2S04 . Написать молекулярное и ионное уравнения реакции. К полученному осадку прилить избыток раствора аммиака. Получается раствор, содержащий комплексный ион [Cu(NH3)4]2+. .Написать молекулярное и ионное уравнение реакции образования комплексной соли.
Опыт №2. Диссоциация железоаммониевых квасцов
Налить в три пробирки по 2 мл раствора железоаммониевых квасцов (NH4)2Fe2(S04)4 В одну пробирку добавить несколько капель роданистого калия. Наличие какого иона в растворе взятой соли указывает появление красно-бурой окраски. В другую пробирку добавить несколько капель концентрированного раствора щелочи. Слегка нагреть. На наличие, какого иона указывает запах аммиака. В третью пробирку добавить 1 мл раствора хлорида бария. Какое вещество выпадает в осадок? На присутствие, какого иона в растворе указывает образование этого осадка? Составить уравнение диссоциации железоаммониевых квасцов. Написать молекулярные и ионные уравнения реакций, происходящих во всех трех пробирках. Какой солью, двойной или комплексной является данная соль?
Опыт №3. Диссоциация гексациано - феррата (III) калия.
Налить в две пробирки по 2мл раствора красной кровяной соли K3[Fe (CN)6]. В одну из них добавить несколько капель щелочи, в другую роданистого калия. Сравнить результаты опытов №2 и №3 и указать, какой солью, двойной или комплексной является гексациано-феррат (III) калия. Составить уравнение диссоциации этой соли.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 |



