Вопросы для самоконтроля:
Как в промышленности получают винилиденхлорид? Где находит применение винилиденхлорид? Из каких других исходных веществ и каким способом можно получить винилиденхлорид?Лабораторное занятие 8 – Изготовление непрозрачного органического стекла
Цель занятия: изготовление органического стекла
Ход занятия: При слабом нагревании на водяной бане в метилметакрилате растворяют полистирол, затем в раствор вводят перекись бензоила и загружают приготовленный раствор в трехгорлую колбу и нагревают содержимое колбы на водяной бане с обратным холодильником, перемешивая непрерывно при 70-80 0С до образования сиропообразного продукта. Полученный продукт охлаждают, разливают в формы и окончательно полимеризуют в термостате при повышении температуры с 55 до 1000 С в течение 4-6 ч до получения твердых образцов органического стекла молочно-белого цвета. Для извлечения органического стекла формы размачивают при 700С в воде в течение 0,5-1 ч и разнимают.
Вопросы для самоконтроля:
Гле в промышленности используют органическое стекло? Какое соединение является мономером для получения органического стекла? Напишите уравнения реакции получения стекла.Лабораторное занятие 9, 10 – Получение и анализ поливинилацетата
Цель занятия: 1. получение поливинилацетата этерификацией поливинилового спирта уксусным ангидридом, 2 анализ ПВА
Ход занятия: Опыт №1. Получение поливинилацетата.
В круглодонную колбу емкостью 100 см3, снабженную обратным холодильником, помещают 4,5г поливинилового спирта, 60 г уксусного ангидрида, 4,5 г ацетата натрия и нагревают в течение 1,5-2 ч на водяной бане, а затем на электрической плитке до полного растворения полимера. Полученный раствор тонкой струей при непрерывном перемешивании вливают в большой стакан, наполненный на ѕ горячей водой. Раствор приливают порциями по 5-10 см3. Высажденный полимер переносят в чашку Петри. Затем меняют горячую воду в стакане и выделяют следующие порции полимера описанным способом. Осажденный полимер промывают водой на воронке Бюхнера до нейтральной реакции промывных вод по метиловому оранжевому. Для полного удаления уксусной кислоты промытый полимер растворяют в небольшом количестве ацетона и осаждают его горячей водой вышеописанным способом. Полученный полимер размельчают и сушат в сушильном шкафу при 50-600С.
Опыт №2. Анализ поливинилацетата.
Определяют растворимость исходного поливинилового спирта и полученного сополимера и содержание ацетатных групп. Для определения растворимости небольшое количество полимера (0,1-0,2 г) помещают в пробирки и добавляют в каждую пробирку по 3-5 см3 соответствующий растворитель (ацетон, вода, тетрахлорид углерода). Затем в течение 0,5-1 ч наблюдают за изменениями, происходящими с полимерами. Результаты сводят в таблицу.
Полимер | Вода | Ацетон | Тетрахлорид углерода |
Определение содержания ацетатных групп. Метод основан на щелочном омылении ацетатных групп в полимере с последующим титрованием избытка щелочи соляной кислотой.
![]()
В круглодонную колбу помещают 0,3-2 г измельченного и высушенного поливинилацетата, взвешенного с точностью до 0,0002 г и приливают из бюретки 50 см3 0,5 н. раствора гидроксида натрия. К колбе присоединяют холодильник, закрытый сверху пробкой с хлоркальциевой трубкой, и нагревают на кипящей водяной или песчаной бане в течение 5-6 ч. После охлаждения содержимое колбы титруют в присутствии фенолфталеина 0,5н. раствором соляной кислоты до исчезновения розовой окраски. Параллельно проводят контрольный опыт. По результатам анализа двух проб принимают среднее значение.
Содержание ацетатных групп находят Х (%) находят по формуле:
![]()
Где V1 и V2 – объем 0,5 н раствора соляной кислоты, израсходованного на титрование контрольной и анализируемой пробы соответственно, см3; f – поправочный коэффициент 0,5 н раствора соляной кислоты; 0,0295 – количество ацетатных групп, соответствующее 1 см3 точно 0,5 н. раствора соляной кислоты, г; g – навеска, г.
По результатам анализа рассчитывают содержание в сополимере винилацетатных звеньев Х1 (%) по формуле:
![]()
где 0,043 – количество винилацетата, соответствующее см3 точно 0,5 н. раствора соляной кислоты, г.
Вопросы для самоконтроля:
Почему поливинилацетат нельзя получить полимеризацией виниплацетата? С какими мономерами винилацетат способен сополимеризоваться? Каким методом определяют содержание ацетатных групп?Лабораторное занятие 11, 12 – Поликонденсация фенола и формальдегида в щелочной среде (получение резольных смол)
Цель работы: синтезировать термореактивную фенолоформальдегидную смолу и рассчитать ее выход на загруженный фенол.
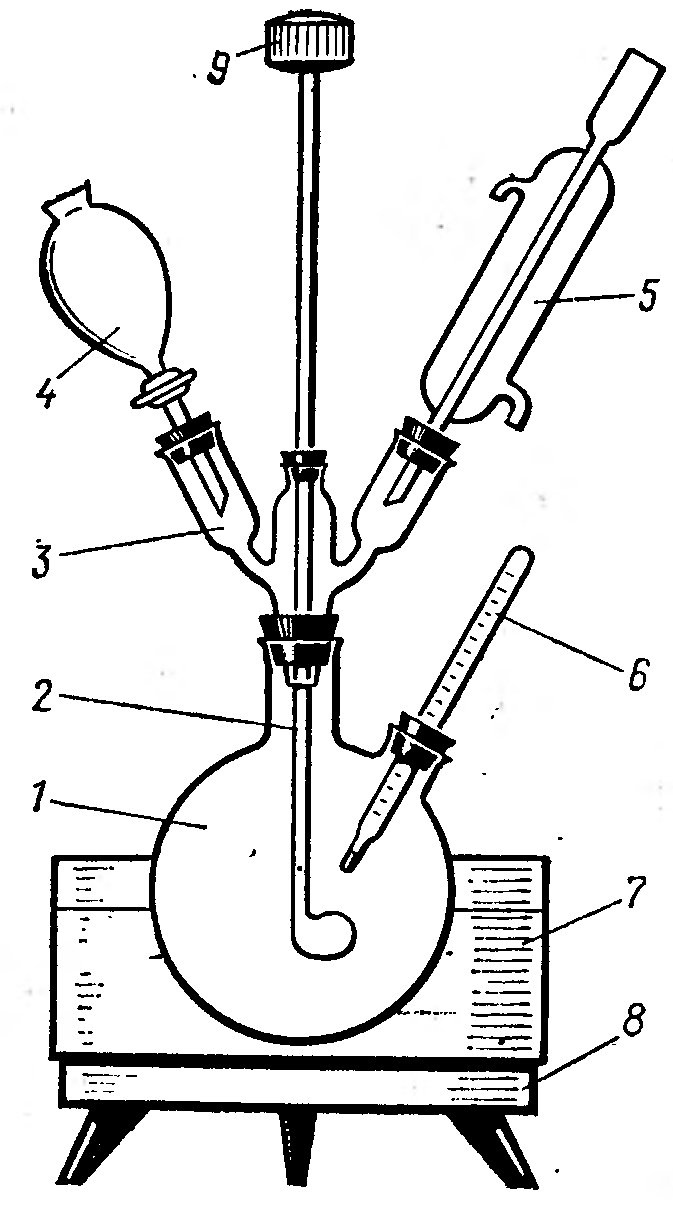
Взвешивают 0,2 моль фенола, загружают в реакционную колбу (рис.1), туда же при перемешивании на холоде вводят такой объем формалина, который содержит 0,235 моль формальдегида. После полного растворения фенола вводят катализатор (1,5% аммиак от массы фенола). Реакционную смесь постепенно нагревают на водяной бане до температуры 363-368 К и выдерживают при этой температуре 30-45 мин. После окончания конденсации жидкость в колбе разделяется на 2 слоя. Реакцию ведут до тех пор, пока объем выделяющегося водного слоя не перестанет изменяться. После охлаждения водный слой сливают. Смолу сушат при температуре 333-338К до получения прозразного продукта. Смолу выливают в предварительно взвешенную фарфоровую чашку, взвешивают и рассчитывают выход смолы.
Оформление результатов: составьте уравнения химических реакций (по стадиям – резол, резитол, резит). Запишите расчет загрузки мономеров и выхода смолы на фенол и формальдегид. Результаты работы и расчетов занесите в таблицу:
Масса реагентов | Масса реагентов | Выход | Скорость отверждения |
Фенола (г) | Фенола (г) | На фенол (%) | На формальдегид (%) |
Вопросы для самоконтроля:
Каково строение новолака, резола, резита? Какие катализаторы используются для получения новолака? В чем особенность получения новолака?Лабораторное занятие 13 – Поликонденсация фенола и формальдегида в кислой среде (получение новолака)
Цель работы: 1) получение фенолоформальдегидного олигомера новолачного типа, определение скорости его отверждения; 2) определение растворимости олигомера до и после отверждения.
|
Рис.1. Прибор для синтеза смол: 1- колба, 2 – мешалка, 3 – крестовина, 4 – капельная воронка, 5 – обратный холодильник, 6 – термометр, 7 – водяная баня, 8 – электрическая плитка, 9 - мотор |
В круглодонную колбу (рис.1) емкостью 100 см3, снабженную обратным холодильником и термометром, помещают 9,4 г (0,5 моль) фенола, нагревают колбу до 40-500С для расплавления фенола и добавляют 8,5 см3 (0,085 моль) 36%-го формалина. После перемешивания содержимого колбы добавляют 5 см3 (0,0005 моль) 1н. раствора HCl. Затем смесь в течение 10-15 мин нагревают с обратным холодильником до 800С. Через 10-20 мин после начала кипения смесь начинает мутнеть и затем расслаиваться. В пробирку поместить 2,5 г фенола кристаллического, 5 мл формалина, кипятильный камешек, кипятить 2 минуты, влить 0,3 мл концентрированной соляной кислоты, встряхнуть (смесь начинает кипеть) через две минуты смесь расслаивается. Подогревать еще две минуты реакционную смесь, водный слой слить, добавить столько же дистиллированной воды, нагреть и снова слить. Смолу вылить на часовое стекло, высушить фильтровальной бумагой. Получена термопластическая смола – новолак.
Отверждение новолачных смол проводят на металлической плите, помещенной на электрическую плитку и нагретой до температуры 433 К. 0,5 г предварительно измельченной в порошок смолы предварительно смешивают в ступке с уротропином (15% от массы смолы), а затем помещают на плиту так, чтобы площадь соприкосновения не была больше 1см3. Порошок начинают перемешивать стеклянной палочкой и замечают время по секундомеру. За конец отверждения принимают то время, когда смола перестает тянуться за палочкой и образуется твердая корка.
Испытать растворимость смолы в спирте. При хранении смола твердеет, становится хрупкой.
Обработка результатов: Составьте реакции образования термопластичного полимера (новолак). Рассчитайте выход смолы. Результаты работы и расчетов занесите в таблицу.
Масса реагентов | Масса реагентов | Выход | Скорость отверждения |
Фенола (г) | Фенола (г) | На фенол (%) | На формальдегид (%) |
Вопросы для самоконтроля:
Какое вещество используется для отверждения фенолформальдегидной смолы. Привести схемы реакций поликонденсации фенола с формальдегидом с образованием линейного, разветвленного и сетчатого полимеров. В каких случаях образуются только линейные полимеры? Какие условия необходимы для получения разветвленных и трехмерных полимеров?Лабораторное занятие 14, 15 – Получение полиэфирной смолы поликонденсацией фталевого ангидрида и глицерина
Цель работы: 1)получение полиэфира на основе фталевого ангидрида и глицерина; 2) определение состава, молекулярной массы полиэфира и его растворимости в различных растворителях.
В фарфоровый стакан помещают 22,0 г фталевого ангидрида и 13,3 г глицерина и прикрывают его опрокинутой стеклянной воронкой. Смесь нагревают на масляной бане (или воздушной) до 1800С и поддерживают эту температуру в течение 2 ч. Затем реакционную смесь нагревают до 200-2200С и выдерживают при этой температуре до образования полимера, труднорастворимого в ацетоне. В процессе синтеза полиэфира отбирают пробы реакционной смеси для определения кислотного числа. Первую пробу отбирают сразу после плавления фталевого ангидрида, следующие – через 15, 30, 45 мин и через 1, 2, 3ч. Фталевый ангидрид при нагревании возгоняется и кристаллизуется на холодных стенках воронки. Перед отбором пробы его счищают в реакционный сосуд и тщательно перемешивают реакционную смесь.
Определение кислотного числа
Кислотное число (К. Ч.) характеризуется количеством мг КОН, необходимым для нейтрализации карбоксильных групп, содержащихся в 1 г анализируемого вещества.
Две навески исследуемого полимера (0,3-1г), взвешенного с точностью до 0,0002 г, помещают в колбы, приливают 20-30 см3 растворителя (вода, спирт, ацетон, диоксан, смеси органических растворителей), после растворения оттитровывают 0,1н. раствором КОН в присутствии фенолфталеина до появления розовой окраски. Параллельно ставят контрольный опыт и рассчитывают К. Ч.:
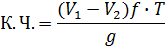
Где V1 и V2 – объем 0,1н. раствора КОН, израсходованного на тирование пробы с навеской полимера и контрольной пробы, см3; f – поправочный коэффициент 0,1н. раствора КОН; Т – титр 0,1н. раствора КОН, г/см3; g – навеска вещества, г.
Затем определяют растворимость, число омыления и эфирное число полученного полиэфира.
Определение растворимости.
В пробирку с пришлифованной пробкой помещают 0,5г полимера, приливают 5 см3 растворителя и оставляют стоять в штативе на 2ч при комнатной температуре, изредко встряхивая содержимое пробирки. По истечении 2 часов отмечают изменения, происшедшие в пробирке. При этом возможно либо полное растворение, либо ограниченное набухание полимера. В случае частичного растворения или набухания полимера следует проверить его растворимость при повышенной температуре. Для этого пробирку с испытуемой смесью нагревают на водяной бане с обратным холодильником в течение 30 мин, после чего вновь отмечают происшедшие изменения.
Определение числа омыления и эфирного числа.
Число омыления характеризуется числом мг КОН, необходимым для нейтрализации свободных карбоксильных групп, содержащихся в 1г исследуемого полимера. В сложных эфирах, не содержащих свободных карбоксильных групп, число омыления совпадает с эфирным числом.
В 2 конические колбы емкостью 250 см3, снабженные обратными холодильниками, помещают точно взвешенные навески (0,5-1г) исследуемого полимера и приливают пипеткой по 25 см3 0,5н спиртового раствора КОН. Параллельно ставят контрольный опыт. Колбы с обратными холодильниками нагревают на водяной бане в течение 3 ч. По истечении этого времени содержимое колбы, не охлаждая, титруют 0,5н. раствором HCl в присутствии фенолфталеина до исчезновения розовой окраски. Эфирное число (Э. Ч.) рассчитывают по формуле:
Э. Ч. = (a - b)T.1000 /g
Где а – объем 0,5н. раствора HCl, израсходованного на титрование контрольной пробы, см3; b – объем 0,5н. раствора HCl, израсходованного на титрование анализируемой пробы, см3; Т – титр кислоты, выраженной в мг КОН; g – навеска вещества, г.
Вопросы для самоконтроля:
В чем заключаются основные закономерности реакций поликонденсации глицерина и фталевого ангидрида? Привести реакции поликонденсации глицерина и фталевого ангидрида с образованием линейного, разветвленного и трехмерного полимеров Что характеризует число омыления?Самостоятельная работа студентов
Методы синтеза полимеров (4 неделя) [7.2.3, стр. 183-334]
Методы получения синтетических полимеров Радикальная полимеризация и сополимеризация Ионная полимеризация Поликонденсация Химическая модификация полимеровТиповые процессы синтеза полимеров (7 неделя) [7.2.3, стр. 183-334]
Полимеризация в массе Полимеризация в растворителе Суспензионная полимеризация Эмульсионная полимеризация Поликонденсация в дисперсионной средеФизическая структура полимеров (10 неделя) [7.1.2, стр. 19-39]
1. Гибкость цепей полимеров
2. Агрегатные и фазовые состояния полимеров
3. Надмолекулярная структура полимеров
4. Основы реологии полимеров
5. Пластификация полимеров
Основные процессы переработки полимеров (13 неделя) [7.1.2, стр. 273-304]
Экструзия Литье под давлением Виброформование Прессование Механическая обработка

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 |