U(h) = ((64c0RT)/c)×g2e-ch ×(-A*/12ph2),
где c0 - концентрация противоионов в дисперсной среде; g - постоянная, определяемая величиной jd.
Суммарная потенциальная энергия взаимодействия частиц отрицательна на близких и далеких расстояниях. Она может быть положительна на средних расстояниях (преобладает энергия отталкивания). Максимум потенциальной кривой (рис. 1.) отвечает потенциальному барьеру DE. Первый минимум (1) соответствует непосредственному соприкосновению частиц, между которыми имеются прослойки среды.
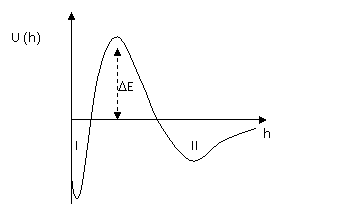

Рис. 1. Зависимость энергии взаимодействия U двух частиц от расстояния между ними h.
Коагуляция лиофобных дисперсных систем может происходить в результате различных внешних воздействий, например при механическом воздействии (ультразвука), действии электрического поля, при нагревании и замораживании системы. Коагуляция лиофобных золей может быть вызвана также их сильным разбавлением или концентрированием. Наиболее часто коагуляция дисперсных систем происходит при добавлении электролитов. Различают два типа электролитной коагуляции коллоидных систем: 1) нейтрализационную, происходящую в результате снижения поверхностного потенциала частиц; 2) концентрационную, протекающую вследствие сжатия диффузной части двойного электрического слоя.
Нейтрализационная электролитная коагуляция характерна для коллоидных систем, содержащих слабо заряженные частицы. Концентрационная коагуляция обычно наблюдается в сильно заряженных дисперсных системах.
Введение электролитов снижает высоту потенциального барьера (рис. 1), но при небольших концентрациях электролита энергетический барьер остается достаточно велик и коагуляция частиц не происходит. Агрегация наступает при введении определенного для данной системы количества электролита, соответствующего порогу коагуляции. Порог быстрой коагуляции Ск определяет количество электролита, необходимое для коагуляции единицы объема коллоидной системы при полном исчезновении потенциального барьера DE. При сохранении небольшого потенциального барьера в системе протекает медленная коагуляция.
Порог коагуляции зависит от валентности коагулирующего иона. Эта зависимость выражается правилом значности (правилом Шульце – Гарди). Более строгую, теоретически обоснованную количественную связь между порогом быстрой коагуляции Ск и валентностью иона выражает правило Дерягина – Ландау:
Ск = К e3 (kT)5 / А2е6z6,
где К – константа, слабо зависящая от соотношения валентности катиона и аниона электролита; e - диэлектрическая проницаемость раствора; kТ – энергия теплового движения одной частицы; А – постоянная ван-дер-ваальсовых сил притяжения; е – заряд электрона; z – валентность противоиона.
Правило Дерягина – Ландау, выведенное авторами на основе представлений физической теории коагуляции, позволяет определить значение порога быстрой коагуляции, которое соответствует исчезновению энергетического барьера на кривой общего взаимодействия коллоидных частиц в зависимости от расстояния между ними. Рассчитанные по данному правилу значения порога коагуляции не всегда совпадают с экспериментальными значениями вследствие того, что коагулирующее действие ионов зависит не только от валентности, но и от специфической адсорбции, не учитываемой приведенным выше уравнением.
При электролитной коагуляции по концентрационному механизму (для сильно заряженных частиц) порог коагуляции Ск в соответствии с правилом Дерягина-Ландау (обоснование эмпирического правила Шульце-Гарди) обратно пропорционально заряду z противоионов в шестой степени, т. е.
Ск = const/z6, (1)
При нейтрализации коагуляции (при малых потенциалах поверхности j0 частиц) показатель степени при z в уравнение (1) уменьшается до двух (правило. Эйлерса-Корфа).
Установлено, что коагулирующим действием в электролите обладают не все ионы, а только те, которые несут заряд, противоположный по знаку заряду поверхности коллоидных частиц. Таким образом, для золей с отрицательно заряженными частицами коагулирующими ионами являются катионы, а для золей с положительными частицами – анионы.
Шульце установил, что коагулирующая сила ионов тем больше, чем больше заряд коагулирующего иона. Это правило было затем подтверждено Гарди и получило название правило Шульце-Гарди.
Иными словами, ионы-коагуляторы с большим зарядом вызывают явную коагуляцию при значительно меньших концентрациях (снижают порог коагуляции), чем ионы с меньшим зарядом. Правило Шульце-Гарди носит приближенный характер, так как коагулирующее действие электролита зависит не только от зарядности ионов, но и от размеров ионов и степени их гидратации. По величине коагулирующей способности ионы щелочных металлов можно расположить в следующий ряд:
Cs+>Rb+>NH4+>K+>Na+>Li+
Анионы можно расположить в соответствующий ряд:
J->NO3->Br->Cl-.
Эти ряды ионов получили название лиотропных рядов.
Коагуляцию гидрофобного золя можно вызвать и при помощи смеси электролитов. При этом возможны три случая:1) коагулирующее действие смеси электролитов суммируется (аддитивность); 2) коагулирующее действие смеси электролитов меньше, чем у чистых электролитов. Это явление называется антагонизмом ионов. Оно характерно для смеси ионов, имеющих различную валентность; 3) в ряде случаев имеет место усиление коагулирующего действия смешиваемых ионов. Это явление называется синергизмом ионов.
Коагуляция гидрофобных электролитов может произойти при смешивании в определенных количествах золей, имеющих различный заряд коллоидных частиц. Это явление называется взаимной коагуляцией и может рассматриваться как частный случай электролитной коагуляции. При сливании двух противоположно заряженных золей коагуляция наступает при условии и концентрациях, когда общее число зарядов одного коллоида нейтрализует общее количество противоположных зарядов другого коллоида.
Гидрозоль гидроксида железа синтезируют методом конденсации путем проведения гидролиза FeCl3 при 1000С:
FeCl3 + 3H2O®Fe(OH)3 + 3HCl
Реакция гидролиза FeCl3 идет интенсивно с образованием высокодисперсных нерастворимых в воде частиц Fe(OH)3.
Агрегативная устойчивость золя Fe(OH)3 обеспечивается прежде всего наличием на поверхности дисперсных частиц двойных электрических слоев. Элементарная частица такого золя называется мицеллой. В основе мицеллы лежит нерастворимый в данной дисперсной среде агрегат, состоящий из множества молекул (атомов): m[Fe(OH)3], где m – число молекул (атомов), входящих в агрегат.
Поверхность агрегата может заряжаться благодаря избирательной адсорбции ионов из дисперсионной среды или диссоциации молекул в поверхностном слое агрегата. В соответствие с правилом Пескова-Фаянса адсорбируются преимущественно ионы, входящие в состав агрегата, либо специфически взаимодействующие с ним. Ионы, сообщающие агрегату поверхностный заряд, называются потенциалопределяющими. Заряженный агрегат составляет ядро мицеллы. При данном методе получения золя гидрооксида железа Fe(OH)3 ядро m[Fe(OH)3]nFe3+ - имеет положительный поверхностный заряд за счет адсорбции ионов Fe3+ из среды (n – число адсорбированных ионов). Заряд ядра компенсируется эквивалентным зарядом противоположно заряженных ионов – противоионов, расположенных в объеме среды. Противоионы, находящиеся непосредственно у поверхности ядра (на расстояниях, близких к диаметрам ионов), помимо электростатических сил испытывают силы адсорбционного притяжения поверхности. Поэтому они особо прочно связаны с ядром мицеллы и носят название противоионов адсорбционного слоя (их число n-x). Остальные противоионы составляют диффузно построенную ионную оболочку и называются противоионами диффузного слоя (их число х).
Мицелла гидрофобного золя является электронейтральной. Формулы мицеллы ионостабилизированного золя Fe(OH)3 можно записать следующим образом:
мицелла
6444444474444448
{m[Fe(OH)3]nFe3+3(n – x)Cl-}3х+ 3xCl-
агрегат
1444442444443
ядро мицеллы
144444244443
коллоидная частица
nFe3+ - потенциалопределяющие ионы (ПОИ);
3(n – x)Cl - - противоионы адсорбционного слоя;
3xCl - - ионы диффузного слоя.
В формуле мицеллы границы коллоидной частицы обозначены фигурными скобками. Толщина адсорбционного слоя d мала (<1нм) и постоянна. Толщина диффузного слоя l существенно больше (может быть >10нм) и сильно зависит от концентрации электролитов в системе. При высоких концентрациях электролитов или при введении многозарядных ионов, ионный фактор c становится большим, а толщина l=1/c мала и стремится к нулю. В пределе l=0 и частица незаряжена. В этом случае противоионы адсорбционного слоя полностью компенсируют поверхностный заряд ядра. В результате достигается так называемое изоэлектрическое состояние, часто сопровождающееся потерей агрегативной устойчивости системы.
Написанная выше формула мицеллы является только качественной, она позволяет судить о структуре поверхностных ионных слоев, но непригодна для количественной характеристики состава коллоидных частиц.
Минимальную концентрацию электролита, при которой начинается быстрая коагуляция, называют порогом коагуляции Ск. Порог коагуляции определяют титрованием золя растворами электролитов до начала быстрой коагуляции или по зависимости оптической плотности золя от концентрации электролита.
Пороги коагуляции вычисляют на основе экспериментальных данных по формуле
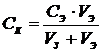 , (2)
, (2)
где СК – порог коагуляции, моль/л; СЭ – концентрация исходного раствора электролита, моль/л; VЭ – объем электролита, вызвавшего коагуляцию, мл; VЗ - объем золя, мл.
Величину, обратную порогу коагуляции, называют коагулирующей способностью

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
