Поверхностно-инактивные вещества обладают следующими характерными особенностями: большим по сравнению с растворителем поверхностным натяжением и более высокой растворимостью. К таким веществам относятся все неорганические электролиты: кислоты, щелочи, соли, а также некоторые органические соединения, например муравьиная НСООН и аминоуксусная Н2NCH2COOH кислоты. Адсорбция поверхностно-инактивных веществ отрицательная.
Математическая зависимость между поверхностным натяжением (Н/м), концентрацией растворенного вещества С (моль/м3) и адсорбцией Г (моль/м2) была установлена Гиббсом и выражается следующей формулой:
![]() (1)
(1)
ds/dC – изменение поверхностного натяжения раствора с изменением концентрации; R – универсальная газовая постоянная; Т – температура.
Из уравнения Гиббса видно, что адсорбция положительна, если ds/dC<0, т. е. когда при повышении концентрации поверхностное натяжение понижается. Если ds/dC>0, то концентрация растворенного вещества в поверхностном слое будет меньше, чем в объеме раствора: Г<0. Когда ds/dC=0, то Г=0, т. е. адсорбции нет.
Величина ds/dC является мерой способности вещества понижать поверхностную энергию; она называется поверхностной активностью. Поверхностную активность определяют, измеряя поверхностное натяжение для разных концентраций растворов ПАВ при постоянной температуре. Строят изотерму поверхностного натяжения в виде кривой s=f(C) (рис.2, кривая 1). Используя уравнение Гиббса, получают зависимость Г от концентрации раствора при постоянной температуре, т. е. изотерму адсорбции Г=f(С) (рис. 2, кривая 2).
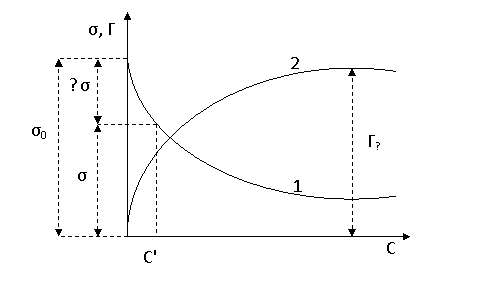

Рис. 2. Зависимость поверхностного натяжения (1) и адсорбции (2) от концентрации ПАВ.
Значение ds/dC и С в уравнении (1) находят с помощью изотермы поверхностного натяжения (рис. 2, кривая 1); в приближенных расчетах ds/dC заменяют величиной Ds/DC:
![]() (2)
(2)
тогда:
![]() (3)
(3)
На основе графиков изотермы поверхностного натяжения и уравнения Гиббса вычисляют удельную адсорбцию Г двумя способами:
1 способ:
а) Находят значения 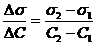 для растворов 4-5 концентраций, где
для растворов 4-5 концентраций, где
s2 – поверхностное натяжение раствора, s1 – поверхностное натяжение воды; С2 – концентрация раствора, С1=0 (т. е. все расчеты проводят относительно воды). Подставляют найденные значения в уравнение 3, в котором
![]() (4)
(4)
б) Находят значения Ds/DC для растворов 4-5 концентраций, как показано на рис. 3а. Для этого на начальном, наиболее крутом участке изотермы через равные интервалы концентраций берут ряд значений С1, С2, С3 и находят соответствующие значения s1, s2, s3 Рассчитывают разности Ds1=s2-s1, Ds2=s3-s2 и DС1=С2-С1, DС2=С3-С2. Подставляют их в уравнение (3).
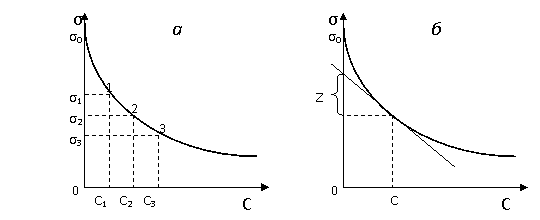

Рис.3. Графические методы определения величины ds/dC: а) - первый способ;
б) - второй способ.
2 способ:
Из 5-6 произвольных точек на начальном участке изотермы поверхностного натяжения проводят касательные и горизонтальные линии до пересечения с осью ординат рис. 3б. Отрезки оси ординат, ограниченные горизонтальными линиями, касательными и обозначаемые Z, имеют следующее математическое выражение: Z= - С(ds/dC).
Величину Z измеряют в единицах поверхностного натяжения. При подстановке Z в уравнение Гиббса получают:
Г=Z/RT (5)
Определив числовые значения отрезков Z для каждой из взятых на кривой точек, находят величину Г для соответствующих этим точкам концентраций. Строят график изотермы адсорбции ПАВ (рис.2, кривая 2).
Кривая изотермы адсорбции показывает, что накопление избытка ПАВ на границе жидкость-газ стремится к некоторому пределу Г¥. Адсорбционный слой достигает насыщения. Изотерма адсорбции описывается уравнением Ленгмюра. При малой концентрации молекулы ПАВ на поверхности располагаются плашмя к поверхности (рис. 4а), что отвечает большей энергии взаимодействия с водой.
При большей концентрации в результате отталкивания углеводородные части молекул ПАВ поднимаются вверх (рис. 4б). При полном заполнении мономолекулярного слоя молекулы образуют более плотную упаковку. При этом полярные группы обращены к воде, а неполярные углеводородные радикалы располагаются вертикально к поверхности, образуя так называемый «частокол Ленгмюра» (рис. 4в).
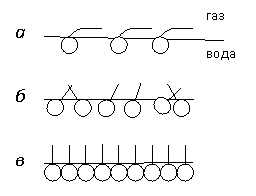

Рис. 4. Расположение адсорбируемых молекул в ненасыщенном поверхностном слое (а и б) и в насыщенном (в); кружком обозначена гидрофильная часть молекул, линией гидрофобная углеводородная часть.
Каждая молекула занимает минимальную площадь на поверхности. Такое состояние адсорбционного слоя отвечает предельной адсорбции Г¥. Уравнение Ленгмюра имеет вид:
![]() (6)
(6)
где Г¥ - предельная адсорбция, (моль/м2); в - константа равновесия, равная отношению констант скоростей процессов адсорбции и десорбции.
Для того чтобы найти константы уравнения Ленгмюра, последнее преобразуют путем деления единицы на обе его части:
![]()
Если обозначить ![]() и
и ![]() , то получаем уравнение прямой:
, то получаем уравнение прямой:
![]() (7)
(7)
При значительном разбросе точек затрудняется выбор правильного наклона прямой. От этого будет зависеть точность определения величин а и d. В таких случаях применяют метод наименьших квадратов, который позволяет проверить линейность зависимости у=f(x), где у=1/Г, а х=1/С. Вычисленные таким путем величины а и d наиболее близки к их истинным значениям. Предельную адсорбцию находят из равенства:
Г¥=1/а (8)
Адсорбционную константу в уравнения Ленгмюра определяют графически следующим образом. На графике 1/Г=f(1/С) вверх от точки пересечения прямой с осью ординат откладывают отрезок, равный а (рис.5).
Через полученную точку А¢ проводят горизонтальную линию до пересечения с прямой зависимости 1/Г=f(1/С). Из полученной точки Д¢ опускают перпендикуляр на ось абсцисс (точка Д). Отрезок ОД представляет собой величину, равную в. По величине отрезка ОД, выраженной в единицах 1/С, находят численное значение константы:
в=ОД (9)
Размерность в обратная размерности концентрации. Численно константа в равна величине, обратной концентрации, при которой достигается 1/2 предельной адсорбции.
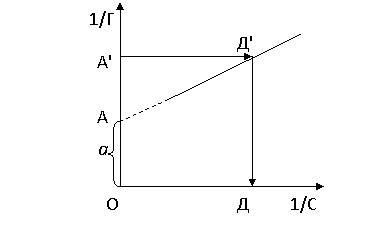

Рис.5. График 1/Г – 1/С.
Как следствие из теории Ленгмюра принимается, что при достижении предела адсорбции на границе раздела раствор-газ образуется насыщенный монослой из молекул ПАВ, ориентированных перпендикулярно к поверхности водной фазы и плотно прижатых друг к другу. На этом основано вычисление размеров молекул ПАВ. Зная величину Г¥, находят площадь (м2) поперечного сечения полярной группы (S0) и длину d (м) молекулы ПАВ:
S0=1/(Г¥Na) (10)
d=(Г¥М)/r (11)
где Na - постоянная Авогадро, Na = 6,02×1023 моль-1; М – молекулярная масса ПАВ, кг/моль; r - плотность ПАВ, кг/м3.
Значения М и r для некоторых веществ приведены в таблице 1 (см. приложение).
Методы определения поверхностного натяжения
На практике наиболее часто используют статические или полустатические методы, позволяющие измерять равновесные значения поверхностного натяжения жидкостей. К статическим относятся методы капиллярного поднятия жидкости и висячей (лежащей) капли. Полустатическими являются методы максимального давления в капле (пузырьке), отрыва кольца или пластины и сталагмометрический метод.
1. Метод капиллярного поднятия
В основе метода лежит зависимость высоты поднятия жидкости h в узком капилляре от ее поверхностного натяжения. В соответствии с уравнением Лапласа избыточное давление связано с высотой h жидкости в капилляре соотношениями: Dp=2s/rм и Dp=Dρgh
rм – радиус кривизны мениска жидкости в капилляре;
Dρ – разность плотностей жидкости и газовой фазы;
g – ускорение свободного падения.
Вводя так называемую капиллярную постоянную а: а2=2s/(Dρg)=rмh
и учитывая угол смачивания θ жидкостью стенок капилляра радиусом r получаем: s=Dρgrh/(2cosθ)=a2Dρg/(2cosθ). Это соотношение известно как уравнение Жюрена. Таким образом, для определения поверхностного натяжения жидкостей этим методом экспериментально находят высоту поднятия h, радиус капилляра и угол смачивания θ. Метод капиллярного поднятия является одним из наиболее точных (относительная погрешность менее 0,01 %).
2. МЕТОД МАКСИМАЛЬНОГО ДАВЛЕНИЯ В ПУЗЫРЬКЕ
Метод максимального давления в пузырьке основан на измерении давления, при котором происходит отрыв пузырька газа (воздуха), выдуваемого в жидкость через капилляр.
При медленном продавливании пузырька из капилляра в жидкость в нем возникает избыточное внутреннее давление Dp, которое согласно закону Лапласа определяется поверхностным натяжением и кривизной поверхности пузырька Dp=2s/rм.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
