![]() (15)
(15)
![]() – удельная адсорбция, моль/г
– удельная адсорбция, моль/г
С1 – начальная концентрация спирта, моль/л
С0 – равновесная концентрация спирта, моль/л
V – объем раствора спирта, взятого для адсорбции, мл
m – масса угля, г
Результаты работы представить в виде таблицы 4:
Таблица 4.
№ | C | C0 | (x/m) |
Используя данные таблицы начертить на миллиметровой бумаге изотерму адсорбции спирта в координатах (х/m)=f(С0).
В отчете должны быть приведены названия ПАВ; состав системы; температура опыта; способ измерения поверхностного натяжения; примеры расчетов: постоянной прибора, поверхностного натяжения, Г, Г¥, S0, d, x/m; таблицы 2, 3, 5 или 1, 4, 5.
К отчету прилагают графики s=f(C), Г=f(C), 1/Г=f(1/C), x/m=f(C0), выполненные на миллиметровой бумаге.
ВОПРОСЫ ДЛЯ САМОПРОВЕРКИ
1. Что такое поверхностное натяжение, и в каких единицах оно измеряется?
2. Как зависит поверхностное натяжение от природы вещества, образующего поверхность?
3. На чем основано измерение поверхностного натяжения жидкостей методом наибольшего давления пузырька воздуха?
4. Что называется адсорбцией, и как количественно ее характеризуют?
5. Напишите фундаментальное адсорбционное уравнение Гиббса и его анализ.
6. Что такое предельная адсорбция?
7. Уравнение Ленгмюра.
8. Как найти постоянные в уравнении Ленгмюра?
9. Что такое поверхностная активность? Какие вещества называются поверхностно активными?
ЛАБОРАТОРНАЯ РАБОТА № 2
ИЗУЧЕНИЕ АДСОРБЦИИ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ НА УГЛЕ
Цель работы
Изучить адсорбцию уксусной кислоты на активированном угле статическим методом.
Задачи работы
1. Определить концентрацию уксусной кислоты до и после адсорбции.
2. Рассчитать удельную адсорбцию ПАВ на угле.
3. Построить изотерму адсорбции.
4. Графически определить константы уравнения Фрейндлиха и проверить его применимость к адсорбции органических кислот из растворов на угле.
Приборы и материалы
· Колбы конические емкостью 200 мл. – 12 шт.
· Стеклянные воронки – 6 шт.
· Пипетки вместимостью 10, 5, 2 мл.
· Бюретка для титрования – 25 мл.
· Технические весы.
· Аппарат для встряхивания растворов в колбах.
· Фарфоровая ступка.
· Активированный уголь БАУ.
· Раствор уксусной кислоты 0,4 моль/л.
· Раствор гидроксида натрия 0,1 и 0,02 моль/л.
· Раствор фенолфталеина спиртовой.
· Вода дистиллированная.
ТЕОРЕТИЧЕСКОЕ ПОЯСНЕНИЕ
Адсорбцией называют концентрирование веществ на поверхности раздела фаз. Вещество, которое адсорбирует другое вещество, называют адсорбентом. Название адсорбируемого вещества зависит от его положения по отношению к адсорбенту. Если вещество находится в объеме и может адсорбироваться, то его называют адсорбтивом. Это же вещество в адсорбционном состоянии будет называться адсорбатом. Иными словами, для обозначения положения адсорбируемого вещества используют термины адсорбтив (до адсорбции) и адсорбат (после адсорбции).
Молекулы (атомы, ионы, радикалы) адсорбтива соприкасаются с поверхностью адсорбента и, вследствие нескомпенсированности молекулярного взаимодействия на границе фаз, молекулами адсорбента удерживаются на его поверхности. Поэтому концентрация молекул на поверхности становиться больше, чем в объеме соприкасающейся с ней жидкости или газа. Часть молекул с поверхности может перейти обратно в объем. Поверхностные атомы и молекулы любого тела заметно отличаются от атомов и молекул внутри фазы. На поверхности они энергетически ненасыщенны, поэтому поверхность любого тела обладает поверхностным натяжением и стремится уменьшить запас свободной энергии DF. Попадая на поверхность твердого тела, частица оказывается связанной с граничными атомами, теряя, по крайней мере, одну степень свободы. Следовательно, процесс адсорбции сопровождается уменьшением энтропии, т. е. DS<0. Поскольку DH=DF+TDS, то и величина энтальпии DH<0. Это означает, что любой адсорбционный процесс экзотермичен. Различают физическую адсорбцию, вызываемую в основном вандервaальсовыми силами, и хемосорбцию, сопровождающуюся химической реакцией. Поскольку поглощение вещества адсорбентом сопровождается выделением тепла, то в соответствии с принципом Ле-Шателье с повышением температуры количество адсорбированного вещества уменьшается. Процесс обратный адсорбции называют десорбцией. Адсорбционное равновесие характеризуется равенством скоростей адсорбции и десорбции.
На процесс адсорбции влияют такие факторы, как природа поглотителя и поглощаемого вещества, состояние поверхности, температура, давление газа или концентрация раствора. Твердые адсорбенты - это природные и искусственные материалы с большой наружной или внутренней поверхностью, на которой происходит адсорбция из граничащих с ней газов или растворов
Количество поглощенного вещества на единицу поверхности адсорбента называют удельной адсорбцией. Так как измерить поверхность адсорбента трудно, то на практике адсорбцию Г выражают в молях на единицу массы адсорбента (Г, моль/кг).
Для описания процесса адсорбции, в частности мономолекулярной, помимо фундаментального уравнения адсорбции Гиббса применяют ряд других аналитических уравнений, которые называют по имени их авторов.
При незначительном заполнении адсорбента адсорбатом отношение концентраций веществ в адсорбционном слое и в объеме стремится к постоянному значению, равному Кг. Эту закономерность можно выразить аналитически следующим образом,
Г=Кг С (1)
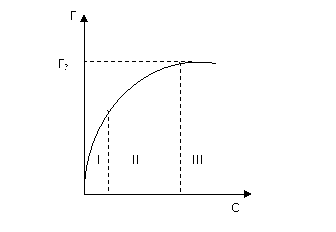

Рис. 1. Изотерма адсорбции
Уравнение (1) характеризует изотерму адсорбции при малых концентрациях адсорбтива (рис. 1, участок I) и является аналитическим выражением закона Генри. Коэффициент Кг не зависит от концентрации и представляет собой константу распределения, характеризующую распределение вещества в адсорбционном слое по отношению к его содержанию в объемной фазе. Полученное на основе закона Генри уравнение (1) и, соответствующая ему линейная зависимость адсорбции от концентрации на начальном участке изотермы адсорбции (участке I), соблюдается лишь приближенно, но это приближение бывает достаточным для практики. В более общем виде зависимость адсорбции от концентрации адсорбтива можно определить при помощи уравнения Фрейндлиха (2):
Г=x/m=kС1/n, (2)
где x - количество адсорбированного вещества, моль; m - масса адсорбента, кг; k и n - коэффициенты.
Это уравнение было получено на основе результатов обработки опытных данных по адсорбции ПАВ при концентрации адсорбтива, равной единице, когда С=1, k=Г. Постоянная k зависит от природы адсорбента и адсорбата и колеблется в широких пределах. Ее физический смысл состоит в том, что она дает величину адсорбции при равновесной концентрации, равной единице. Коэффициент n характеризует отличие участка изотермы адсорбции (рис. 1, участок II.) от прямой. Значение адсорбционного показателя 1/n лежит в пределах 0,1–1 и зависит от температуры и природы адсорбата. Коэффициенты уравнения Фрейндлиха не трудно определить графически. Для этого логарифмируют уравнение (2), преобразуя его в уравнение прямой (3).
lg(x/m)= lgk+(1/n)lgC (3)
Определив экспериментально ряд значений x/m, строят график в координатах lg(x/m) – lgC (рис. 2).
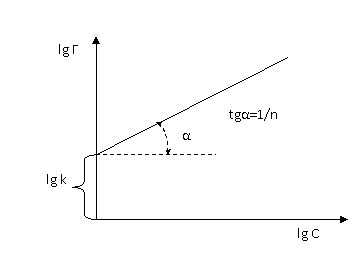

Рис. 2. Графическое определение коэффициентов k и n уравнения Фрейндлиха.
Отрезок прямой, отсекаемый на оси ординат, представляет собой величину lgk, а тангенс угла наклона прямой – величину 1/n.
Изотерма адсорбции, которая соответствует аналитическому выражению уравнения Фрейндлиха (3) не определяет предельного значения адсорбции (участок 3, на рис. 1).
Аналитическое выражение адсорбции в зависимости от концентрации адсорбтива в виде изотермы адсорбции дано в теории Ленгмюра. В основу теории положены кинетические представления о процессе адсорбции, определяющие скорости адсорбции и десорбции в условиях равновесия.
Физическая адсорбция протекает практически мгновенно (10-12–10-6 с) продолжительность процесса хемосорбции значительно больше (>102 c).
Ленгмюр предложил молекулярно–кинетический вывод изотермы адсорбции для случая локализованной адсорбции на однородной поверхности в отсутствии сил притяжения между молекулами адсорбата (уравнение 4):
![]() (4)
(4)
где Г – удельная адсорбция, (моль/м2); Г¥ – предельная адсорбция, т. е. величина адсорбции при мономолекулярном заполнении поверхности, (моль/м2); в – константа равновесия, равная отношению констант скоростей процессов адсорбции и десорбции, С – равновесная концентрация адсорбируемого вещества в растворе
Проведем анализ уравнения Ленгмюра (4) и сопоставим его с уравнениями Генри (1) и Фрейндлиха (2). В начале процесса адсорбции, когда С®0 и 1>>вС, в соответствии с уравнением (4) Г= Г¥вС. Произведение Г=Г¥вС –величина постоянная, что соответствует коэффициенту Кг в законе Генри, т. е. участку 1 изотермы адсорбции (рис. 1). Уравнение Фрейндлиха справедливо лишь для средней части изотермы адсорбции (участок 2). При С®¥, вС>>1 из уравнения (4) следует, что Г=Г¥, это соответствует участку 3 изотермы адсорбции. Таким образом, уравнение Ленгмюра определяет все участки изотермы мономолекулярной адсорбции, в том числе и предельную адсорбцию.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
