3. Подготовка к прохождению тестирования (модули 1, 2, 3, по лабораторным работам, по коллоидным терминам, по курсу «Коллоидная химия»).
4. Подготовка к сдаче пяти коллоквиумов по теории курса, используя рекомендуемую литературу.
5.Подготовка к итоговой контрольной работе, включающей решение задач и ответы на теоретические вопросы.
Решение типовых задач
1. Рассчитайте работу адгезии Wа ртути к стеклу при 293 К, если известен краевой угол q =1300. Поверхностное натяжение ртути s=475 мДж/м2. Найдите коэффициент растекания ртути по поверхности стекла.
Решение: Выражение для работы адгезии через краевой угол дается уравнением Дюпре – Юнга:
Wа= sж-г(1+cosq)=475(1+ cos1300)=475(1-0,64)=171 мДж/м2
Коэффициент растекания рассчитывают по соотношению f=Wа-Wк, где Wк=2sHg представляет работу когезии; f=171-2×475=-779 мДж/м2, т. е. растекания нет.
2. Экпериментально получена зависимость общего числа частиц гидрозоля золота в 1 м3 nS от времени коагуляции t, вызванной электролитом NaCl:
Время коагуляции t, с | 0 | 125 | 250 | 375 | 425 |
Общее число частиц в 1 м3 nS × 10-14, част./м3 | 20,2 | 8,08 | 5,05 | 3,67 | 3,31 |
Вязкость среды h =1×103 Па×с, температура 293 К.
Покажите применимость уравнения Смолуховского для описания кинетики коагуляции данного золя. Рассчитайте время половинной коагуляции Q и константу скорости быстрой коагуляции Кб. Сравните значение константы скорости быстрой коагуляции, рассчитанной теоретически, с экспериментальной величиной.
Решение: Кинетика изменения общего числа частиц nS в теории Смолуховского представлена уравнением: nS=n0/(1+t/Q), где время половинной коагуляции Q=1/n0Кб, Кбтеор=4kТ/3h.
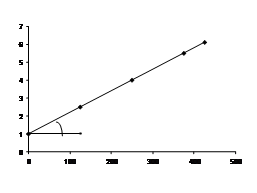
Уравнение Смолуховского можно представить в виде n0/nS=1+(t/Q)
Рассчитываем значения n0/nS при различном времени коагуляции:
t, с 0 125 250 375 425
n0/nS 1 2,5 4,0 5,5 6,1
|
|
 |
|
|
Тогда Кбэксп=1/n0Q=1/(20,2×1014×83,33)=5,94×10-18 м3/с
Кбтеор=4kТ/3h=4×1,38×10-23×293/3×10-3=5,39×10-18 м3/с
Значения констант Кбэксп и Кбтеор близки, следовательно, коагуляция гидрозоля золота является быстрой.
3. Постройте график зависимости приведенного осмотического давления от концентрации раствора сополимера стирола и метакриловой кислоты в толуоле ( Т = 300 К ) по следующим данным:
Концентрация раствора C×10-3, г/м3 | 1,1 | 2,8 | 5,4 | 7,6 |
Осмотическое давление p, Па | 9,8 | 37.3 | 106,4 | 187,4 |
По графической зависимости p/С=¦(С) определите относительную молекулярную массу М полимера и значение второго вириального коэффициента А2.
Решение: Приведенное осмотическое давление растворов полимеров описывается уравнением:
p/С=RT(1/М + А2С + А3С2)
При малых концентрациях полимера в растворе коэффициент А3 равен нулю. Рассчитываем значения p/С и строим их зависимость от С.
С×10-3, г/м3 1,1 2,8 5,4 7,6
|
|
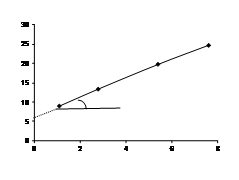 |
(p/С)×103, Па×м3/г 8,91 13,32 19,70 24,66
|
|
Вириальный коэффициент А2 определяется по тангенсу угла наклона полученной прямой:
А2=tg a/RT=2,5×10-6/8,31×300=1,003×10-9 м3×моль/г2
Положительное значение второго вириального коэффициента указывает на хорошее термодинамическое сродство между полимером и данным растворителем.
4. Постройте кривую кинетики набухания каучука в четыреххлористом углероде в координатах a - t по следующим экспериментальным данным:
Время набухания t, мин | 5 | 30 | 90 | 150 | 210 | 240 | 270 | 300 |
Степень набухания at | 0,33 | 1,15 | 2,33 | 2,91 | 3,25 | 3,41 | 3,58 | 3,58 |
Определите графическим способом константу скорости набухания К.
Решение: При ограниченном набухании полимеров степень набухания изменяется во времени в соответствии с уравнением
dat/dt=К(aмакс-at)
Интегрируя это уравнение, получаем:
ln [aмакс/(aмакс-at)]=Кt
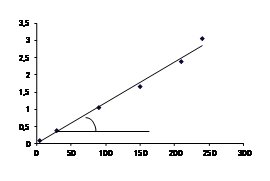 |
Зависимость ln [aмакс/(aмакс-at)] от t является линейной. Согласно исходным данным aмакс=3,58. Рассчитываем данные для построения графика этой зависимости:
t, мин | 10 | 30 | 90 | 150 | 210 | 240 | ||
aмакс/(aмакс-at) | 1,1 | 1,47 | 2,86 | 5,34 | 10,85 | 21,06 | ||
ln [aмакс/(aмакс-at)] | 0,097 | 0,387 | 1,052 | 1,676 | 2,38 |
|
|
|
Из графика находим: К=tg j =0,012 мин-1
5. При изменении вязкости растворов полистирола в толуоле с помощью капиллярного вискозиметра (типа вискозиметра Оствальда) получены следующие данные:
Концентрация раствора С, г/л | 0 | 1,70 | 2,12 | 2,52 | 2,95 | 3,40 |
Время истечения раствора t, с | 97,6 | 115,6 | 120,2 | 124,5 | 129,8 | 134,9 |
Рассчитайте значения относительной, удельной, приведенной вязкости растворов полимеров и постройте график зависимости hуд/С=¦(С). Определите характеристическую вязкость [h] и значение вискозиметрической константы
Решение: Относительная вязкость определяется как отношение вязкости раствора h к вязкости чистого растворителя h0:
hотн=h/h0
Удельная вязкость раствора представляет собой приращение вязкости за счет растворенного вещества, отнесенное к вязкости растворителя:
hуд=(h-h0)/h0=hотн-1
Согласно уравнению Пуазейля можем записать:
hотн=rt/r0t»t/t0 и hуд=t/t0-1
где r и r0 – соответственно плотность раствора и растворителя; t и t0 – время истечения раствора и растворителя.
Приведенная вязкость hпр есть отношение удельной вязкости к концентрации раствора С:
hпр=hуд/С
Результаты расчета приведены ниже:
Концентрация раствора
Концентрация раствора С, г/л | 1,70 | 2,12 | 2,52 | 2,95 | 3,40 |
hотн | 1,184 | 1,231 | 1,276 | 1,330 | 1,382 |
hуд | 0,184 | 0,231 | 0,276 | 0,330 | 0,382 |
hуд/С, л/г | 0,108 | 0,109 | 0,110 | 0,111 | 0,112 |
|
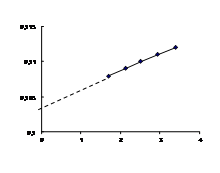 |
Строят график в координатах hуд/С – С. Экстраполируя зависимость на нулевую концентрацию, определяем значение характеристической вязкости:
|
Согласно Хаггинсу при малых концентрациях раствора
hуд/С=[h]+К[h]2С
Вискозиметрическую константу Хаггинса К находим по тангенсу угла наклона прямой:
tg a=К[h]2=0,0023
К=0,0023/0,1042=0,216
6. Определите коэффициент диффузии D и среднеквадратичный сдвиг Dср частицы гидрозоля за время t =10 с, если радиус частицы r =50 нм, температура опыта 293 К, вязкость среды h= 1×10-3 Па×с.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
