1. Сохранность антигена
2. Специфичность окрашивания
3. Хорошо охарактеризованный препарат антител
4. Удобная метка
Для успешного окрашивания необходимо сделать тканевые антигены нерастворимыми, но при этом антигенные участки их молекул должны более или менее сохранять свою пространственную структуру и быть доступными антителами. Помимо этого нужно зафиксировать общую структуру ткани, чтобы после окрашивания на препарате можно было идентифицировать иммунореактивную клетку и органеллу.
Методы фиксации используются самые разнообразные. Можно использовать альдегидные фиксаторы. Пептидные гормоны и нейропептиды хорошо сохраняются при высушивании замороженной ткани с последующей обработкой формальдегидом. Можно использовать парафиновые и криостатные свежезамороженные срезы. Выбор метода фиксации определяется спецификой конкретной реакции антиген-антитело и предполагаемой локализацией антигена.
Парафиновые срезы, приготовленные для окрашивания антителами нельзя сильно нагревать, т. к. могут пострадать антигенные детерминанты.
Иммунофлуоресцентные методы
Прямой метод
Флуоресцеинтиоционат присоединяют прямо к специфичеким антителам. Меченную антисыворотку разводят физиологическим раствором, забуференным с помощью фосфата, а затем наносят на срез ткани и после инкубации несвязавшиеся антитела удаляют, промывая срез забуференным фосфатом физиологическим раствором. Окрашенные срезы просматривают в микроскоп с УФ оптикой, при этом в точке связывания наблюдается яблочно зеленая флуоресценция.
Непрямой метод
Имеет более широкое распространение. В этом случае за первыми специфическими немеченными антителами следует второй слой, содержащий антитела к g - глобулинам животного, донора первых антител (например, козьи антитела к g - глобулинам кролика, меченные флуоресцеинтиоционатом). Первые антитела (кроличьи) связавшиеся с участками среза ткани, содержащими нужный антиген, в свою очередь служат антигеном для вторых флюоресцентных антител.
Иммуноферментные методы
Пероксидаза впервые была использована для мечения антител в 1966 г и теперь во многих случаях применяется вместо флюоресцеина. Принцип метода непрямого окрашивания тот же, но антитела визуализируют при помощи гистохимической реакции на пероксидазу, в качестве субстрата (красителя) обычно используют диаминобензидин.
Метод дает возможность иметь постоянные препараты, поскольку интенсивность окраски со временем не падает как при флуоресцентном мечении. Препарат можно просматривать в обычный световой микроскоп и фотографировать.
Метод «немеченных» антител
Если непрямой метод является «двухслойным», то метод «немеченных» антител, предложенный L. A. Sternberger и соавт. “трехслойный”. Первый слой образован немеченными антителами (обычно кроличьими) к тканевому антигену. Второй слой – немеченными антителами (обычно овцы или козы) к иммуноглобулинам животного, у которого выработаны первые (специфические) антитела. Третий слой представляет собой антитела к метке, выработанные в животном того же вида, в котором получены антитела к тканевому антигену (обычно кролик). Таким образом, в третьем слое антитела связаны с меткой иммунологически. Следует отметить, что вторые антитела способны выполнять функцию мостика между первыми и третьими только при условии их избыточной концентрации по отношению к первым антителам. Метод немеченных антител, наиболее широко применяемый в иммуноцитохимии, имеет несколько модификаций в зависимости от используемой метки третьего уровня и характера ее связи с третьими антителами, одна из модификаций – пероксидаза-антипероксидазный метод (ПАП-метод).
Пероксидаза-антипероксидазный метод
В начале 70-х годов L. A.Sternberger и соавт. предложили использовать в качестве третьего уровня в технике немеченных антител пероксидаза-антипероксидазный (ПАП) комплекс. Этот комплекс образован молекулами пероксидазы, связанными с антителами к пероксидазе, выработанными в животном того же вида, которое было использовано для получения первых антител (обычно кролик).
Этот метод характеризуется черезвычайно высокой чувствительностью, так как на каждую молекулу первого антитела приходится три молекулы пероксидазы (Рис.6), причем при иммунологическом образовании ПАП - комплекса активность пероксидазы полностью сохраняется. С другой стороны, такая высокая концентрация пероксидазной метки позволяет существенно увеличить разведение первой антисыворотки, что, в свою очередь, приводит к резкому снижению концентрации
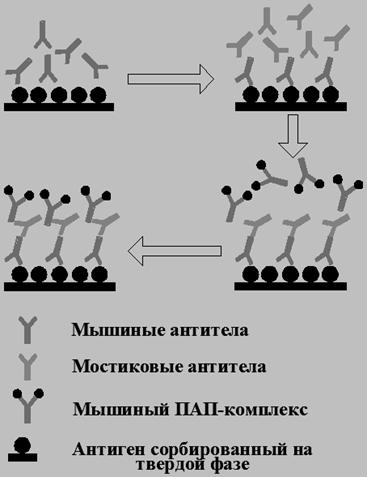
Рис. 6. Схема проведения анализа с использованием
ПАП - комплекса
побочных антител (например, антител к примесям иммуногена) и падению фона. Низкий фон при использовании ПАП - метода также обусловлен высокой очисткой коммерческого ПАП - комплекса и блокированием потенциальных мест его неспецифического связывания тканью путем предварительной инкубации материала с нормальной сывороткой того вида животного, у которого были выработаны вторые антитела. Единственным недостатком ПАП - метода является его относительная трудоемкость и расходование некоторых дополнительных реактивов.
Конечным этапом иммуноцитохимической реакции является выявление маркерного фермента – пероксидазы хрена (ПХ) с помощью субстрата ферментативной реакции – перекиси водорода и хромогена. В процессе реакции образуется комплекс пероксидазы с перекисью, взаимодействующий с донором электронов, в результате чего образуется нерастворимый окрашенный продукт реакции и вода. В процессе этой реакции пероксидаза хрена не расходуется, то есть одна и та же молекула фермента может участвовать в образовании многих молекул конечного окрашенного продукта.
ПХ + Н2 О2 ® ПХ. Н2 О2 ® ПХ. Н2 О2 + электрон донора ®
® нерастворимый продукт + Н2 О + ПХ
В качестве донора электрона чаще всего используются 3,3/ –диаминобензидинтетрагидрохлорид (ДАБ), обеспечивающий образование темно-коричневого нерастворимого осадка в месте реакции (Рис.7).
Важным преимуществом ПАП - метода, с последующим выявлением ДАБ-продукта гистохимической реакции, является возможность увеличения его оптической плотности (в основном за счет осаждения в местах реакции таких металов, как кобальт, никель, серебро, золото, осьмий). Такого рода интенсификация позволяет: с одной стороны, существенно увеличить разрешающую способность иммуноцитохимического метода, а с другой – использовать его для «двойного» мечения (выявить на одном и том же срезе два или более антигена, содержащихся как в разных клетках, так и в пределах одной и той же клетки).
Двойное мечение прямым методом
В этом случае два антигена выявляют с помощью двух первых антител, меченных различными флуорохромами, например, флуоресцеином и родамином. Дальнейшее использование соответствующих красителям фильтров позволяет различить метки и, таким образом, локализовать оба антигена на срезах. Этот метод, однако, малоэффективен в случае значительного преобладания внутриклеточного содержания одного антигена над другим, так как при этом одна метка маскирует другую.
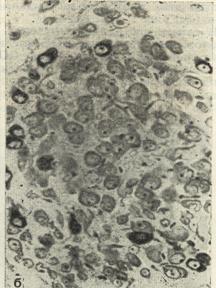
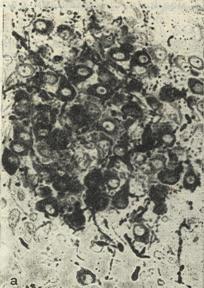
А Б
Рис. 7. Гормонреактивные структуры в дорсолатеральной
части паравентрикулярного ядра гипоталамуса
крысы, выявленные ПАП – методом с коньюгацией
ДАБ.
А – реакция с антисывороткой к вазопрессину;
Б - реакция с антисывороткой к окситоцину
Двойное мечение непрямым методом
Непрямой метод предполагает использование двух видов первых антител соответственно к двум разным антигенам. Первые антитела выявляются вторыми антителами с различной меткой. Необходимым условием применения этого метода является использование первых антител, полученных у различных видов животных, и отсутствие перекрестной реакции у вторых – меченных антител.
В этом методе в качестве первых антител можно также использовать моноклональные антитела, относящиеся к различным классам иммуноглобулинов.
Комбинация иммуноцитохимии с другими гистохимическими методами
Использование комбинации иммуноцитохимии с другими гистологическими и физиологическими подходами позволяет решить принципиально важные проблемы фундаментальной и прикладной науки. Например, комбинация иммуноцитохимии с гистофлюоресцентным или радиоавтографическим выявлением моноаминов широко используется для двойного мечения пептид - и моноаминергических структур мозга с целью изучения их структурно-функциональных взаимоотношений. Сочетание иммуноцитохимии с техникой маркеров аксоплазматического транспорта обогатило нейронауки в познании специфических нервных связей между различными отделами головного и спинного мозга.
Вопросы для самоконтроля
1. Какова особенность иммуноцитохимических методов?
2. История развития иммуноцитохимических методов.
3. Какой краситель использован первым для коньюгации
с антителами в иммуноцитохимии?
4. Иммунофлюорисцентные методы: прямой и непрямой.
5. Какой цвет флюоресценции наблюдается при использовании
антител, меченных флюоресцеинизоционатом в местах их
коньюгации с антигеном?
6. Иммуноферментные методы и их преимущества.
7. Какие ферменты используют в качестве метки антител в
иммуноцитохимии?
8. Пероксидазо-антипероксидазный метод (ПАП - метод).
9. Как получают антитела?
10. Как провсти тестирование антител?
11. Какими свойствами должны обладать хорошие антитела?
12. В чем преимущество моноклональных антител?
13. Что такое авидность антител?
Раздел 5. КОЛИЧЕСТВЕННЫЕ МЕТОДЫ
Количественные оценки клеточных параметров не только помогают глубже понять уже известные процессы, но и открывают принципиально новые явления. Можно вспомнить хотя бы пример установления различий в содержании ядерной ДНК у разных организмов, за которым последовала многочисленная серия работ, доказавших генетическую роль ДНК.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



