15. Хромофоры и их характеристика.
16. Какие группы в молекуле красителя способствуют углублению
и усилению окраски?
17. Принцип поглощения света веществами.
18. Классификации красителей.
19. Активные красители и их преимущества.
20. Основные, кислотные амфотерные красители.
21. Нейтральные, индифирентные красители.
22. Интеркалирующие красители, механизм их действия.
23. К какому типу красителей относится судан черный?
24. Флюоресцентные красители и их преимущества.
25. Какие вещества клетки обладают собственной видимой
флюоресценцией?
26. Метахромазия, механизм ее возникновения.
27. В какой форме должен присутствовать в растворе
толуидиновый синий, чтобы наблюдалось красное
окрашивание?
28. Какие компоненты клетки выявляют с помощью реактива
Шиффа?
29. Для чего при окраске по Фельгену или ШИК-реакции после
реактива Шиффа препарат промывают в водой, содержащей
сернистый газ, а затем проточной водой? Можно ли
пренебречь промывкой в сернистой воде?
30. Для определения каких веществ в клетке используется метод
Браше?
31. Контроль специфичности окрашивания.
Раздел 2. БИОХИМИЧЕСКИЕ МЕТОДЫ
При использовании биохимических методов исследования анализируемый материал находится в условиях, при которых сохраняется подвижность и реакционная способность составляющих его молекул в течение всего длительного времени, необходимого для проведения многочисленных процедур. Об этом следует постоянно помнить и проводить все манипуляции как можно быстре и при температуре 0 – 4оС, обеспечивающей отсутствие деятельности ферментов.
Предосторожности нужны уже на первом этапе – доставки материала в лабораторию, особенно если речь идет о животных. В этом случае следует максимально сократить время между забоем и исследованием ткани. Извлеченную ткань или орган как можно быстрее охлаждают, помещая в заранее охлажденную среду (например, жидкий азот). Более эффективно охлаждение мелких кусочков ткани.
Биохимические методы анализа клеточных структур складываются из трех последовательных этапов:
1. Гомогенизация клеток.
2. Фракционирование.
3. Анализ фракций.
Гомогенизация клеток
Гомогенат должен удовлетворять следующим требованиям:
1. Должно быть достигнуто разрушение максимального количества клеток. Так как в противном случае неразрушенные клетки будут флотировать при центрифугировании, и их содержимое будет загрязнять фракции на всех этапах очистки, кроме того, уменьшится выход органоидов.
2. Внутриклеточные структуры должны остаться неповрежденными; это даст некоторую гарантию того, что не будет перераспределения веществ между ними.
3. Необходимо создавать условия, предотвращающие агглютинацию частиц, которая способствует потере веществ и загрязннию фракций.
Контроль за степенью гомогенизации осуществляется с помощью либо фазово-контрастного, либо темнопольного микроскопов, которые позволяют довольно надежно узнавать только клеточные ядра. Несовершенство такого контроля очевидно. В настоящее время имеется множество способов гомогенизации, основанных на различных принципах: от осмотического шока до применения ультразвука или детергентов. Однако самым распространенным является способ механического разрушения клеток в гомогенизаторах. Существует большое количество гомогенизаторов разной конструкции. Самые простые - это обычные стеклянные гомогенизаторы и ступки со стеклянными шариками и песком. Есть и более сложные установки, в которых можно регулировать скорость движения и силу давления.
Способ гомогенизации и тип гомогенизатора выбирается в зависимости от целей исследования. Так, при выделении плазматических мембран эритроцитов млекопитающих лучшим способом оказывается осмотический шок. Если предполагается изучение митохондрий из клеток печени, то методы гомогенизации должны быть более жесткие, чем в случае выделения плазматических мембран тех же клеток. Разные ткани также требуют различных условий гомогенизации. Кроме того, условия гомогенизации варьируют при переходе с одного объекта на другой. Следует учитывать даже возраст животного, так как показано, например, что плазматические мембраны клеток животных разных возрастных групп отличаются по хрупкости и склонности к образованию пузырьков.
Таким образом, условия гомогенизации подбирается эмпирически для каждого конкретного случая, причем у любого исследователя имеются свои излюбленные приемы.
Большую трудность представляет выбор подходящей среды для гомогенизации. Среды можно подразделить на водные и безводные. Основой водной среды традиционно является сахароза. Чаще всего используют 0.25 М раствор сахарозы. Существует бесчисленное множество рецептов, различающихся по концентрации сахарозы, рН, добавлению буфера, ЭДТА, катионов, макромолекулярных веществ.
При выборе концентрации тех или иных составляющих среды приходится учитывать самые разные условия. Так, например, установлено, что при выделении мембран ЭПС лучшая морфологическая сохранность мембран достигается применением 1.46 М сахарозы в качестве среды для гомогенизации и центрифугированием в 0.88 М сахарозе. Однако, одновременно показано, что высокие концентрации сахарозы подавляют активность некоторых ферментов при дальнейшем анализе. При концентрации сахарозы 1.2 М активность АТФазы шероховатых микросом снижена на 75% по сравнению с той, которая выявляется при концентрации сахарозы 0.15 М. В то же время низкая концентрация сахарозы может вызывать необратимую агрегацию микросом. Учитывая все сказанное выше, исследователь эмпирически подбирает концентрацию, которая наилучшим образом удовлетворяет целям исследования.
Клетки различных тканей одного и того же вида неодинаково реагируют на одни и те же растворы. Например, лизосомы печени агглютинируют в солевых растворах, а лизосомы селезенки сильнее агглютинируют в 0.25 М растворе сахарозы, чем в 0.2 М хлористом калии.
Важную роль играют двухвалентные катионы. Высокая концентрация ионов магния и кальция (1 – 3 мМ) необходима для стабилизации хроматина. Концентрация двухвалентных ионов определяет морфологическое состояние мембран. При выделении мембранных структур, в частности плазматической мембраны, можно получить мембраны либо в виде листочков, либо в виде пузырьков. Последнее менее желательно, так как во фракцию мембран попадает и содержимое пузырьков, что затрудняет анализ. Повышение концентрации двухвалентных ионов позволяет выделять плазматические мембраны в виде листочков. Этого же эффекта можно добиться, вводя реактивы, связывающие мембранные SH-группы.
Для предотвращения агглютинации очень важно соблюдать соотношение между количеством гомогенизируемого материала и объемом используемой среды.
На качество гомогената могут оказать влияние самые неожиданные факторы, на первый взгляд незначительные: фармакологические вещества, введенные животным незадолго до взятия материала, различные дезинфицирующие вещества, применяемые в виварии.
Водные среды широко распространены и легко доступны. К недостаткам их относятся потеря и перераспределение водорастворимых компонентов, в основном белков. Так, долгое время активность ДНК-полимеразы I обнаруживалась только в цитоплазме. И лишь использование безводных сред при выделении ядер позволило обнаружить ее в ядре.
Основой безводной среды являются органические растворители. Обычно используют смесь двух растворителей разной плотности: высокой и низкой. Для того, чтобы варьируя их относительную концентрацию, получать растворы нужной плотности. Безводные среды получили гораздо меньшее распространение. Они более сложны в работе и плохо воспроизводятся. А главное, их применение, вызывает потерю липидов – одного из основных компонентов мембран. Это, в свою очередь, также ведет к перераспределению белков между мембранами и внутри мембран, что вызывает нарушение ферментативных комплексов и потерю активности ферментов.
Фракционирование
Следует сразу подчеркнуть, что степень выделения и степень очистки – это разные вещи. Если нужно сохранить наиболее полный состав фракции, то приходится мириться с загрязнениями, если же главная задача – тщательная очистка от примесей, то неизбежны потери части компонентов. При проведении цитохимических исследований чистота фракций должна быть максимальной. Если это невозможно, то необходимо точно оценить количество примесей.
Основным методом фракционирования является центрифугирование, которое проводится в несколько этапов.
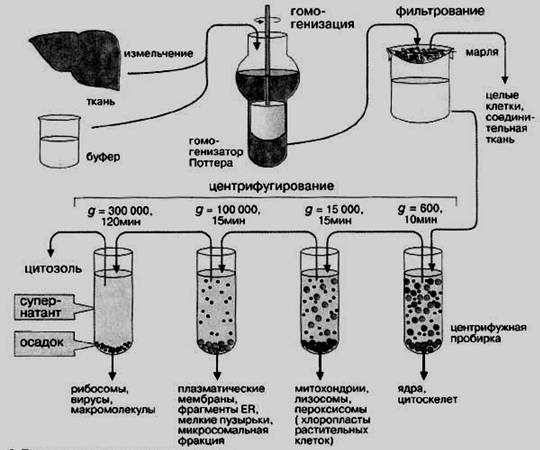
Первый этап – это грубое разделение гомогената на три фракции (Рис. 2): ядерную (600 – 1000 g, в течение 10 – 20 мин), митохондриальную (здесь же лизосомы и пероксисомы) (4 000 – 15 000 g, 5 – 20 мин) и микросомальную (надосадочная жидкость при выделении митохондрий). Ускорение, время центрифугирования, так же как и вязкость среды, подбирают для каждого конкретного случая.
|
Рис. 2. Выделение клеточных органелл
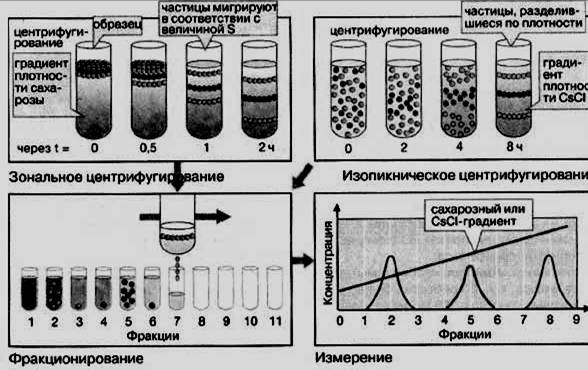
Второй этап фракционирования заключается в следующем. Полученная фракция наслаивается на градиент плотности (сахарозы) и центрифугируется в соотвтствии с плотностью и скоростью седиментации в течение различного времни (Рис. 3). Равновесное центрифугирование в градиенте плотности позволяет частично разделить митохондрии (плавучая плотность r=1.228), лизосомы (r=1.238 – 1.245) и пероксисомы (r =1.255 – 1.260). Для лучшего разделения процедуру повторяют.
|
Рис. 3. Центрифугирование в градиенте плотности
Иногда прибегают к дополнительным обработкам для того, чтобы добиться лучшего разделения. Например, если речь идет о лизосомах, то используют присущую им особенность захватывать in vivo чужеродные вещества. Если в качестве такого вещества использовать тритон WR-1339, то «нагруженные» лизосомы будут флотировать. Если вводить животным предварительно декстран, препараты железа или коллоидное золото, то плотность лизосом будет значительно выше плотности других органелл.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |