Методы центрифугирования постоянно совершенствуются и модифицируются. Кроме того, применяют и другие методы фракционирования: электрофорез, хроматографию, разделение в двухфазных системах, противоточное распределение.
Для определения степени чистоты полученной фракции используют биохимический и морфологический контроль.
Для морфологического контроля осадок фракции подвергают фиксации и последующей обработке согласно методам приготовления препаратов для электронно-микроскопического анализа. Главные трудности связаны тем, что в большинстве случаев отсутствуют четкие морфологичские критерии различных фракций. Если речь идет о целых органоидах, то хорошо идентифицируются ядра, неплохо – митохондрии. Если же необходимо оценить чистоту субфракций органоидов, в частности мембран, то возможности идентификации ограничены небольшим числом специфических структур: поровых комплексов для ядерной оболочки, десмосом и ворсинчатых отростков для плазматической мембраны, рибосом для шероховатых микросом. Однако очень часто, особенно если фракция содержит обрывки мембран, определить их принадлежность по морфологическим признакам практичски невозможно. То же касается и пузырьков, которые образуются при разрыве мембран. В этом случае неидентифицированные пузырьки могут служить источником сильного загрязнения, так как мембраны, выворачиваясь, захватывают самое разное содержимое гомогената.
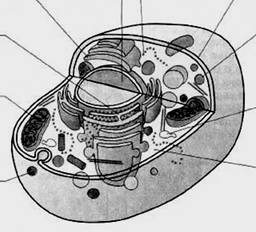
Более полное представление о чистоте и однородности фракции дает биохимический контроль. Маркер данной субклеточной структуры может служить такой фермент, который локализован исключительно в этой структуре, прочно с ней связан и при разделении фракций не ингибируется и не подвергается активации. В настоящее время достаточно надежно установлена локализация некоторых ферментов, которые принято использовать в качестве маркеров (Рис. 4) Определяя активность таких ферментов, можно оценить полноту выделения фракции и степень ее загрязнения.
Обычно фракция считается годной к работе, если степень ее обогащения маркером по сравнению с другими фракциями составляет 5 – 50 крат (для разных тканей, разных органоидов это отношение различное). Фракция считается чистой, если активность маркеров других фракций не превышает 1-5%.
При определении активности маркера учитывают, что она может меняться под действием различных компонентов среды: сахарозы (о ее влиянии на АТФазную активность шероховатых микросом говорилось выше), детергентов, ионов и т. п. Необходимо учитывать
аппарат Гольджи ядро рибосомы плазматическая α-маннозидаза II ДНК РНК мембрана
фосфодиэстераза
глюкозо-6-фосфатаза лизосомы β-галактозидаза
митохондрии цитохромоксидаза эндосома сукцинатдегидро - пероксидаза
пероксисома цитозоль
|
Рис. 4. Молекулы-маркеры субклеточных структур
также изменение активности в результате хранения материала, таких процедур, как замораживание-оттаивание.
Выявление маркерного фермента можно проводить не только по его активности, но и используя принципиально другой подход – иммунологический. Кроме того, маркерами могут служить наряду с
естественными компонентами структур и искусственные метки. Так, маркером плазматических мембран могут являться так называемые метки – реактивы, которые ковалентно связываются лишь с поверхностными мембранами интактных клеток.
Анализ фракций
На этом этапе очень важно оценить все возможности возникновения ошибок на предыдущих этапах: гомогенизации и фракционирования. Кроме того, здесь чрезвычайно полезным оказывается сравнение результатов, полученных разными способами выделения, очистки, а также сопоставление с электронно-микроскопическими картинами. В свою очередь, и на этом этапе применяются такие методы разделения фракций на составляющие их белки, липиды, полисахариды, нуклеиновые кислоты, такие как электрофорез, изоэлектрическая фокусировка, гель-фильтрация, ионообменная и афинная хроматография и другие. При их проведении также следует учитывать состав используемой среды, степень насыщения ионами, детергентами.
Условия разделения определяется задачами исследования. Если нужно определить молекулярную массу составляющих компонентов, то необходимо как можно более тщательное их разделение (чтобы не идентифицировать какой-либо надмолекулярный комплекс как отдельную молекулу). При этом можно пренебречь изменением конформации белков. Если изучается биологическая активность молекулы (или ее выявление основано на определении этой активности), то условия выделения должны быть направлены на сохранение межмолекулярных связей, определяющих конформацию молекулы и ее реакционную способность.
Существенным недостатком биохимических методов является их трудоемкость и плохая воспроизводимость при переходе на новый объект. Этим, в значительной мере, объясняется тот факт, что до настоящего времени изучению подлежит лишь ограниченное число тканей немногих видов организмов. Обычно исследователи предпочитают работать с «модельными» объектами. Например, при анализе свойств плазматических мембран используют «тени» эритроцитов. При изучении митохондрий – как правило, митохондрии сердечной мышцы крупного рогатого скота. Для мембран ЭПС источником служат клетки печени крысы или мыши. Данные, полученные на ограниченном количестве объектов, распространяются на другие, при этом совсем не очевидно, что такое распространение правомочно. Не известно, какие из установленных фактов являются общими для всех организмов, а какие ткане - и видоспецифичны.
Все описанные выше сложности и недостатки биохимических методов – следствие собственно этих методов. Они в большей или меньшей степени будут преодолеваться по мере совершенствования методик и оборудования. Но есть и принципиальный недостаток метода в целом – это усреднение полученных результатов.
Одна из особенностей биологического материала – его неоднородность. Прежде всего, неоднородность, связанная с наличием в ткани разных типов клеток. Так, излюбленный объект биохимиков – печень млекопитающих, содержит примерно в равном количестве клетки двух типов: паранхиматозные (гепатоциты) и ретикуло-эндотелиальные (купферовские). Клетки одного морфологического типа также неоднородны. Уместнее говорить о них как о популяции клеток одного типа. И, наконец, существует внутриклеточная неоднородность различных структур, например, лизосомы - первичные и вторичные. Если говорить о гепатоцитах, в частности об их плазматической мембране, то она также структурно неоднородна: на границе между соседними гепатоцитами она содержит многочисленные десмосомы, в то время как в просвет канальцев обращена мембрана с множественными впячиваниями длинных ворсинчатых отростков, и, наконец, мембрана, граничащая с лакуной, имеет лишь небольшие выступы и впячивания.
Если исследователя интересуют не усредненные характеристики «печеночной клетки», а вполне конкретные клетки и внутриклеточные структуры, то необходимо научиться сортировать анализируемый материал и хорошо идентифицировать его в первую очередь по морфологическим критериям. Например, можно подобрать такие условия гомогенизации, при которых будут преимущественно разрушаться более крупные и менее утойчивые к механическим воздействиям гепатоциты. Отделив неразрушенные клетки, мы получим гомогенат в основном из гепатоцитов. Используя особенность лизосом купферовских клеток накапливать коллоидный йодид серебра в течение первого часа после инъекции, можно выделить фракцию лизосом только из этих клеток.
Следует отметить, что нарушение организации клетки в результате гомогенизации не всегда приводит к необратимой потере информации о ее неоднородности. Если гомологичные компоненты разных клеток или органоидов значительно различаются по своим свойствам, то можно попробовать разделить, а потом идентифицировать их принадлежность к исходным структурам. Такой подход в свое время позволил установить, что гомогенаты селезенки содержат несколько популяций лизосом, по-видимому происходящих из клеток разного типа. Аналогичная ситуация обнаружена при анализе плазматической мембраны эпителиальных клеток проксимальных извитых канальцев почки. Удалось выделить две фракции: со щеточной каемкой и без нее. Дальнейший анализ показал, что первая фракция содержит щелочной фосфатазы и мальтазы в 15 раз больше, чем вторая. На этом основании сделан вывод о том, что маркерные ферменты клеточной мембраны относятся не ко всей ее поверхности, а только к специализированным участкам.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |





 геназа
геназа



 лактатдегидрогеназа
лактатдегидрогеназа